Лечение нарушений углеводного обмена (предиабет, сахарный диабет)
Разновидности нарушений углеводного обмена
Все патологические состояния, связанные с обменом углеводов, можно разделить на две большие группы: гипергликемию (повышение уровня глюкозы крови) и гипогликемию (ее понижение). В процессе превращения углеводов в энергию активное участие принимает эндокринная система, почки, печень, желудочно-кишечный тракт и др. Выключение в цепи превращения сложных углеводов хоть одного звена сказывается на работе всего организма.
Гипергликемия: характеристика, проявления
Состояние, которое развивается при превышении порогового значения уровня глюкозы в крови натощак (6,1 ммоль/л), называется гипергликемия (преддиабет).
Основной причиной гипергликемии остается сахарный диабет 2 типа. Из-за нарушения функции специальных клеточных рецепторов, которые связываются с инсулином, глюкоза не может попасть из плазмы крови внутрь клетки. В результате запускаются альтернативные механизмы энергетического обмена (без участия глюкозы), что приводит к накоплению токсичных продуктов (например, кетоновых тел или молочной кислоты). Кроме того, стабильно высокий уровень глюкозы приводит к поражению кровеносных сосудов, чем объясняется возникновение осложнений диабета: ангиопатии, нефропатии, ретинопатии, инсультов и инфарктов.
Кроме сахарного диабета, гипергликемия может быть проявлением метаболического синдрома, эндокринных нарушений с избыточным выделением контринсулярных гормонов (акромегалия, тиреотоксикоз, болезнь/синдром Иценко-Кушинга, феохромоцитома).
Гипергликемия – полисимптомное состояние. Классической триадой признаков можно считать увеличенное образование мочи (полиурия), жажду (полидипсия) и потерю веса. Также повышенный уровень сахара в крови проявляется плохим заживлением ран, сухостью во рту, зябкостью ног (особенно ночью), усталостью, снижением зрения, характерна низкая эффективность лечения вялотекущих инфекций стандартными методами терапии.
Диагностика гипергликемии
Основными методами диагностики гипергликемии и сахарного диабета являются определение глюкозы в крови и моче, гликированного гемоглобина, инсулина в крови. Определенную диагностическую ценность имеет проведение перорального глюкозотолерантного теста, который показывает, насколько эффективно организм утилизирует глюкозу. Если через 2 часа после нагрузки глюкозой (75 грамм растворяют в стакане теплой воды и выпивают) показатель сахара в крови составит менее 7,8 ммоль/л, то это считается нормой. Нарушение толерантности – от 7,8 до 11,0 ммоль/л, а выше 11,0 – наличие сахарного диабета.
При подозрении на другие эндокринные патологии определяют уровень соответствующих гормонов в крови, основываясь на клинической картине патологии. Также по показаниям проводят УЗИ брюшной полости и щитовидной железы.
При длительной гипергликемии определяют состояние органов-мишеней: осмотр глазного дна, ЭКГ, измерение скорости клубочковой фильтрации почек, уровня холестерина в крови и белка в моче.
Лечение гипергликемии
При сахарном диабете основу лечения составляет специальная диета. Важно исключить из рациона легкоусвояемые углеводы и увеличить употребление продуктов с большим содержанием клетчатки. Регулярные физические нагрузки повышают степень «захвата» глюкоза мышцами и уменьшению гипергликемии.
При сахарном диабете 2 типа назначаются препараты, снижающие абсорбцию глюкозы в кишечнике, ее синтез в печени, а также повышающие чувствительность клеток к инсулину. Важно учитывать сопутствующие метаболические нарушения и проводить соответствующую коррекцию липидного профиля, уровня мочевой кислоты, лечить вторичную артериальную гипертензию, а также по показаниям врача принимать корригирующие гормональные препараты (при других эндокринных нарушениях).
Инсулинотерапия при СД 2 типа может применяться в стадии декомпенсации при отсутствии эффекта от других сахароснижающих препаратов, диабетической гиперосмолярной, кетоацидотической комах, при беременности и родах.
Преимущества нашей клиники
Эндокринолог клиники «УРО-ПРО» имеет богатый опыт в лечении нарушений углеводного обмена. Использование современных лечебных и диагностических протоколов позволяет достигать максимально возможных результатов.
При появлении симптоматики нарушений углеводного обмена важно обратиться за медицинской помощью как можно раньше, только в этом случае лечение будет наименее затратным и максимально эффективным.
Нарушение углеводного обмена — диагностика и лечение в медицинском центре «Андреевские больницы
У каждого человека в норме уровень содержания глюкозы в крови должен быть от 3,3 до 5,5 ммоль/л. Конечно, глюкоза — очень важная постоянная гомеостаза. При расстройствах углеводного обмена (гипогликемия) в организме происходят необратимые изменения, которые связаны с деятельностью центральной нервной системы.
Понижение глюкозы в крови до 2.2 ммоль/л может спровоцировать судороги и нарушения сознания, человек может впасть гликемическую кому. При незначительном отклонении от нормы больной будет испытывать недомогание, а также снизится его работоспособность.
Причины нарушения углеводного обмена
Основными причинами нарушений процессов, связанных с углеводным обменом, могут стать:
- Нарушение фосфорилирования глюкозы в стенке кишечника (обычно это происходит в том случае, если воспаляется кишечная стенка, при отравлениях флоридзином и монойодацетагом).
- Нарушение нервно-гормональной регуляции.
- Нарушение углеводной функции печени.
- Нарушение нейрогормональной регуляции углеводного обмена.
Симптомы нарушения углеводного обмена
При нарушении разных видов углеводного обмена наблюдается снижение глюкокиназы. Возрастает активность глюко-фосфатазы, следовательно, глюкофосфат поступает в кровь в виде глюкозы. Через мембраны клеток глюкоза практически не проходит, вследствие чего она не способна усваиваться тканями.
Человек при пониженном уровне глюкозы в крови чувствует общую слабость, быстро утомляется, ему тяжело выполнять обычную ежедневную работу. При сильных отклонениях от нормы начинаются судороги, помутнения сознания. Самый страшный симптом этого заболевания – гликемическая кома.
Диагностика нарушения углеводного обмена
Чтобы правильно диагностировать заболевание, вам необходимо обратиться к врачу, который предложит вам пройти следующие анализы и обследования:
- В первую очередь нужно сдать анализ крови.
- Затем биохимический анализ крови.
- Сделать глюкозотолерантный тест.
- Липидный профиль.
- Гликированный гемоглобин.
- Определить уровень секреции инсулина, а также С-пептида.
- Провести иммунологические анализы.
- Проверить, расположены ли вы к возникновению развития нарушений углеродного обмена вследствие наследственности.
- Диагностика нефропатии.
- ЭКГ и УЗИ.
- Сканирование ультразвуком сосудов.
Врач, который специализируется на нарушениях углеводного обмена, – эндокринолог.
Лечение нарушений углеводного обмена
Для восстановления углеводного обмена можно воспользоваться медикаментозным лечением – препаратами, которые снижают сахар в крови. Это бигуаниды, ингибиторы альфа-глюкозидаза. Однако препараты не принесут пользы, если вы не будете соблюдать правильный режим жизни. Сюда входят: правильное питание, физические нагрузки, сахароснижающая терапия.
Профилактика нарушений углеводного обмена
В связи с нарушением обмена веществ могут развиться довольно сложные и серьезные заболевания, поэтому необходимо предпринять все меры для того, чтобы нарушения не начали развиваться. В первую очередь необходимо сбалансированно и правильно питаться. Это основной залог здоровья. Также существует множество витаминных препаратов, биологических пищевых добавок. Если вы – сладкоежка, от продуктов, содержащих много глюкозы, придется отказаться. Оптимальное употребление воды – 2 л в день.
Также существует множество витаминных препаратов, биологических пищевых добавок. Если вы – сладкоежка, от продуктов, содержащих много глюкозы, придется отказаться. Оптимальное употребление воды – 2 л в день.
Питание при нарушении углеводного обмена
Длительность прочтения: 3 мин.
Причина избыточного веса не всегда кроется в неправильном пищевом поведении и отсутствии физической активности. Иногда лишние килограммы появляются как результат нарушения обмена веществ, в частности, углеводного. При этом человек может принимать пищу в умеренных количествах, но организм не может ее полноценно усвоить. Решить проблему можно, если придерживаться специального рациона, который поможет нормализовать эти процессы.
Нарушение углеводного обмена
Углеводы возмещают затраты энергии после физических и умственных нагрузок, а также стрессовых ситуаций. Выработка энергии не происходит без глюкозы – одного из самых главных углеводов, и нарушения возникают при повышении или, наоборот, понижении ее уровня в крови. Таким образом, патологии можно разделить на два вида: нехватка или избыток.
Узнать больше о правилах питания, принципах формирования разумного рациона возможно на 7-модульном сертификационном курсе по диетологии и нутрициологии
Нарушения обмена углеводов возникают по следующим причинам:
- наследственные факторы, из-за которых в организме не синтезируются определенные ферменты;
- сбои в функционировании печени;
- нарушение гормонального фона;
- наличие опухолей в организме;
- патологии кровеносной системы;
- отравления токсичными веществами;
- неправильное питание;
- частые стрессовые ситуации;
- непосильные физические нагрузки.

Симптоматика
|
Избыточный тип нарушений |
Недостаточный тип нарушений |
|
Высокая эмоциональная и физическая активность |
Постоянная сонливость, общая слабость |
|
Гипертония, заболевания сердца и сосудов |
Дрожь в пальцах |
|
Тремор конечностей, дрожь в теле |
Одышка |
|
Высокий уровень глюкозы в крови |
Головокружения |
|
Постоянная жажда, сухость во рту |
Повышенная концентрация кетоновых тел и ацетона, которая сопровождается рвотой и иногда комой |
|
|
Депрессия, равнодушие к происходящему вокруг |
|
|
Пониженный уровень глюкозы в крови |
Бесплатная консультация по вопросам обучения
Наши консультанты всегда готовы рассказать о всех деталях!При избытке углеводов часто развиваются сахарный диабет, ожирение, гипергликемия, при недостатке – гипогликемия и болезнь Гирке, при которой организм не в состоянии перерабатывать глюкозу.
Что такое диета при нарушении углеводного обмена?
Для восстановления углеводного обмена необходимо придерживаться особого рациона. Категорически запрещено «сидеть» на строгих диетах, которые запрещают необходимые для нормальной жизнедеятельности продукты. Такой подход лишь усугубит ситуацию, при этом проблема лишнего веса не устранится.
Категорически запрещено «сидеть» на строгих диетах, которые запрещают необходимые для нормальной жизнедеятельности продукты. Такой подход лишь усугубит ситуацию, при этом проблема лишнего веса не устранится.
Специальная диета предполагает введение в рацион вполне доступных продуктов и ограничение употребления некоторой пищи. Соблюдение несложных правил поможет восстановить обмен углеводов, а также запустить процесс сжигания жировой прослойки.
Питание при нарушении углеводного обмена у пациентов с ожирением
На диете для нормализации углеводного обмена все продукты делятся на разрешенные и запрещенные:
|
Запрещенные продукты |
Разрешенные продукты |
|
Хлебобулочные изделия из муки высшего сорта, сдобного и слоеного теста |
Хлебобулочные изделия из пшеничной или ржаной муки |
|
Супы молочные, крупяные, бобовые и картофельные |
Овощные супы с небольшим количеством картофеля |
|
Мясо утки, гуся |
Борщ, свекольник, окрошка |
|
Колбаса, сосиски, копчености |
Нежирные мясные и рыбные бульоны |
|
Консервы |
Нежирное мясо (говядина, телятина, индюшатина, курица) |
|
Жирная рыба, икра, соленая рыба |
Нежирная рыба в отварном или запеченном виде |
|
Жирная молочная продукция, топленое молоко |
Нежирная кисломолочная продукция |
|
Соленые и жирные сыры |
Нежирные сыры |
|
Яичница |
Куриные яйца (не более 2 шт. |
|
Манка, овсянка, рис |
Крупы (гречка, перловка) |
|
Макаронные изделия |
Сырые свежие овощи |
|
Бобовые |
Квашеная капуста |
|
Жирные соусы, майонез, пряности |
Салаты из овощей, рыбы и мяса |
|
Сладкие фруктовые соки |
Кисло-сладкие ягоды и фрукты |
|
Кулинарные и мясные жиры |
Желе, компоты, муссы из фруктов и ягод |
|
Бананы, виноград, финики, инжир, сладкие фрукты |
Сливочное масло |
|
Кондитерские изделия |
Неострые соусы |
|
Мед, варенье |
Овощные и ягодные соки |
|
Мороженое |
Чай, кофе |
|
Кисели |
|
Диета при нарушении углеводного обмена
Примерное меню диеты может выглядеть следующим образом:
- Завтрак: овощной салат, заправленный небольшим количеством растительного масла, нежирный творог, чай;
- Перекус: яблоко;
- Обед: вегетарианский борщ со сметаной, отварное мясо с тушеной капустой, компот из сухофруктов без сахара;
- Перекус: нежирный творог, стакан молока;
- Ужин: отварная рыба с рагу из овощей, чай;
- Перед сном: стакан кефира.

Хотите знать больше?
Академия Медицинского Образования приглашает на семинар «Актуальные вопросы диетотерапии при избыточном весе и ожирении». Мероприятие состоится 1 и 9 августа. Спикер семинара – Ирышкин Олег Евгеньевич, кандидат медицинских наук, врач спортивной медицины и спортивной диетологии. Слушатели получат знания об причинах возникновения и патогенезе ожирения, а также современных методах лечения избыточного веса. Подробности о семинаре вы можете узнать, перейдя по ссылке.
Бесплатная консультация по вопросам обучения
Наши консультанты всегда готовы рассказать о всех деталях!Нравится материал?
Углеводный обмен — ПроМедицина Уфа
— Как известно, глюкоза является главным энергетическим субстратом (топливом) для всех жизненных процессов в организме человека. От баланса углеводного обмена (процессы превращения глюкозы) зависит жизнедеятельность всего организма. Основными индикаторами нарушения/несостоятельности системы обмена углеводов могут выступать следующие анализы крови человека:— Измерение глюкозы в крови является основным лабораторным тестом в диагностике диабета. Так же данный вид исследования выявляет заболевания печени, патологию щитовидной железы, надпочечников, гипофиза, определяет толерантность к глюкозе у лиц из групп риска развития сахарного диабета, и ожирение.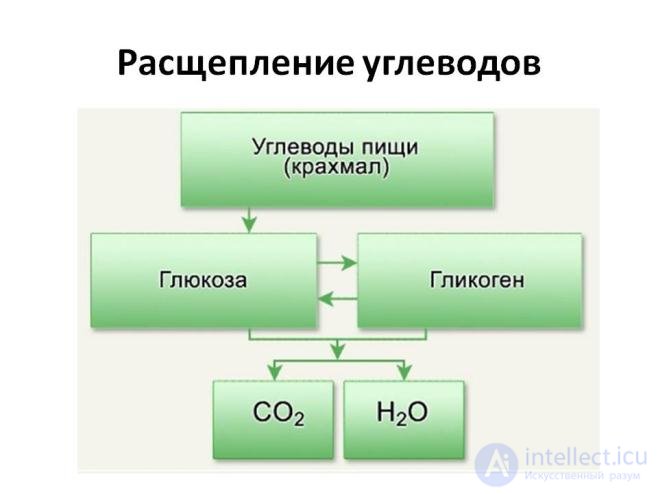
— Гликированный гемоглобин – это соединение гемоглобина с глюкозой, позволяющее оценивать уровень гликемии за 1 — 3 месяца, предшествующих исследованию. Данный вид исследования проводится при диагностике сахарного диабета, долговременном мониторинге и контроле за лечением больных сахарным диабетом и при обследовании беременных женщин на скрытый диабет.
— Инсулин — гормон, продуцирующийся бета-клетками поджелудочной железы, является основным регулятором углеводного обмена. Повышение инсулина в сыворотки крови вызывает усиленное поглощение глюкозы тканями, что приводит к снижению уровня глюкозы в крови и в свою очередь приводит к снижению уровня инсулина. Назначается для исследования больных с сахарным диабетом и другими нарушениями толерантности к глюкозе.
— С-пептид образуется при расщеплении проинсулина. Вместе с образованным инсулином, С-пептид секретируются в кровоток. Его аномально низкий уровень может указывать на снижение выработки инсулина, слишком высокий — говорить о возможном присутствии инсулиномы (гормонально-активная опухоль поджелудочной железы, в избыточном количестве секретирующая инсулин). Может так же указывать на почечную недостаточность.
— Проинсулин является прогормоном — предшественником инсулина, синтезируется в бета-клетках островков Лангерганса поджелудочной железы. Данный вид анализа назначается при диагностике гипогликемических состояний, подозрений на инсулиному (гормонально-активная опухоль поджелудочной железы, в избыточном количестве секретирующая инсулин) и оценке функционирования бета-клеток поджелудочной железы. Увеличение концентрации проинсулина в крови можно наблюдать у пациентов с почечной недостаточностью, циррозом печени, и гипертиреоидизмом.
Из-за чего нарушается метаболизм и как его восстановить?
Метаболизм – это комплекс энергетических и биохимических процессов превращения веществ, обеспечивающих жизнедеятельность и здоровье организма. Цепочка превращений может нарушиться при изменениях в работе щитовидной и половых желез, надпочечников, гипофиза.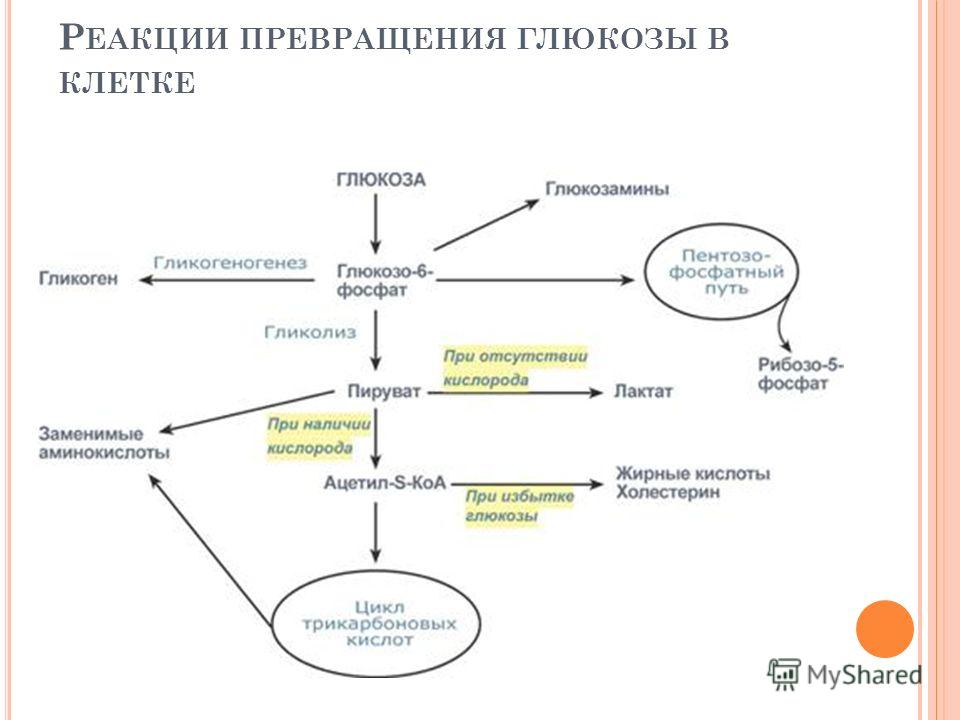 На обмен веществ также негативно влияет избыточное, некачественное или недостаточное питание. Рассмотрим способы его восстановления.
На обмен веществ также негативно влияет избыточное, некачественное или недостаточное питание. Рассмотрим способы его восстановления.
Нарушение метаболизма – виды и признаки
Выделают несколько основных разновидностей метаболизма: белковый, жировой, углеводный, витаминный, минеральный, кислотно-щелочной. Каждый из них может пострадать при гормональных сбоях, из-за жестких диет и других негативных факторов. Чем чреваты различные обменные нарушения?
Белковый метаболизм нарушается при дефиците или избытке белков в рационе. Две основополагающие причины нарушения жирового обмена – истощение и ожирение. В первом случае происходит гормональный дисбаланс, падает иммунитет, начинают выпадать волосы и крошиться ногти. Во втором – возрастет риск сахарного диабета, атеросклероза, сердечно-сосудистых болезней.
Нарушение углеводного метаболизма приводит к гипо- или гипергликемии – к снижению или повышению уровня сахара в крови. При неполадках в водном обмене либо в организме задерживается жидкость, либо он обезвоживается. Последнее состояние чревато сгущением крови, повышением давления и развитием болезней сердечно-сосудистой и выделительной системы.
Нарушение витаминного метаболизма приводит к авитаминозу или гиповитаминозу. Минерального – к снижению иммунитета, болезням тканей и органов. Дисбаланс кислот и щелочей чреват разными исходами – от агрессивности до смерти.
К важным признакам нарушения обмена веществ относят низкий гемоглобин, избыток холестерина, повышение сахара. Выявляют их только лабораторным путем.
Внимание! Внешне проблему можно распознать по слабости, выпадению волос, мигреням, расстройствам сна, апатии, резкому снижению или набору веса, отсутствию аппетита, сыпи. Это основные проявления. У каждого человека метаболические нарушения протекают и проявляются индивидуально.
Восстановление метаболизма
Чтобы восстановить метаболизм, необходимо выяснить причину его нарушения. При гормональном сбое следует пропить курс определенных препаратов, которые должен назначить врач. При изменении кислотно-щелочного баланса – посетить гастроэнтеролога. При истощении – увеличить в рационе количество легкоусвояемого белка. Справиться с метаболическим нарушением можно, только искоренив его причину.
Как ускорить после диеты?
Метаболизм часто замедляется, когда человек пытается похудеть, поскольку организм старается защититься от истощения, сохранив максимум питательных веществ и энергии. Чтобы восстановить его, нужно плавно выходить из диеты, употреблять белковые продукты, сократить количество углеводов, больше двигаться, пить не менее 3 л воды в день, перейти на дробное питание – часто, небольшими порциями.
Как замедлить после диеты?
Если наоборот наблюдается истощение организма из-за слишком ускоренного обмена веществ, старайтесь употреблять исключительно горячую пищу, больше спите, введите в рацион жирные продукты, разграничьте питание – ешьте отдельно белковую и углеводную еду, повысьте калорийность ежедневого меню на 25%.
Продукты для восстановления метаболизма
Некоторые продукты также способны нормализовать метаболизм. Они влияют на скорость пищеварения и восстанавливают баланс метаболических процессов.
Продукты, богатые клетчаткой, восстанавливают полноценное усвоение продуктов. К ним относят зеленый и репчатый лук, томаты, кокос, огурцы, авокадо, редис, белую и цветную капусту.
Многие продукты с высоким содержанием витамина C смещают анаболический-катаболический баланс в правильную сторону. Это лимон, грейпфрут, ананас, арбуз, клубника, смородина, малина. Таким же действием обладает пища с быстрым комплексом белков – молоко и произведенные из него продукты.
Таким же действием обладает пища с быстрым комплексом белков – молоко и произведенные из него продукты.
Сложные углеводы с низкой степенью всасываемости: манная каша и изделия из нее – снижают секрецию поджелудочной железы. Источники полиненасыщенных жирных кислот омега изменяют холестериновый баланс. Среди них – рыбий жир, нефильтрованные масла, свиное сало.
Внимание! Острые специи ускоряют метаболизм на 20%. Добавляйте в блюда перец, имбирь, карри и другие пряности.
Таблетки для здорового метаболизма
Многие мечтают восстановить обмен веществ с помощью «волшебных пилюль». Такие средства существуют, но они способны ускорить или замедлить метаболизм лишь на время. Нормализовать его раз и навсегда можно только с помощью правильного питания и образа жизни.
Углеводная недостаточность
Углеводная недостаточность
Углеводная недостаточность – болезненное состояние, связанное с недостаточным поступлением и усвоением углеводов либо с их интенсивным расходованием.
Так как углеводы играют роль быстрого источника энергии, относительный углеводный дефицит может сопровождать любое физическое перенапряжение и считается вариантом нормы. Уровень углеводов в этом случае быстро восполняется за счет резервов организма без негативных последствий. При длительном дефиците питания, а также при некоторых заболеваниях может развиваться хроническая углеводная недостаточность, последствия которой бывают необратимыми. Наиболее чувствительны к дефициту углеводов клетки нервной и мышечной ткани, которые являются основными потребителями энергии. При нехватке углеводов для восполнения энергии начинают использоваться жиры и даже белок, что может вызывать серьезные изменения в обмене веществ и влиять на работу печени и почек.
Синонимы русские
Дефицит углеводов, гипогликемия.
Синонимы английские
A Carbohydrate Deficiency, Deficiency Of Carbohydrates.
Симптомы
Симптомы углеводной недостаточности во многом зависят от ее длительности и степени выраженности. При кратковременном падении уровня сахара в крови в периоды физического или умственного перенапряжения могут отмечаться легкая слабость и усиленное чувство голода. Длительный дефицит углеводов, сопровождающийся истощением их запаса в печени, может приводить к нарушению ее функций и развитию дистрофии (нарушению питания тканей).
Основные проявления углеводной недостаточности:
- общая слабость,
- головокружение,
- головная боль,
- голод,
- тошнота,
- обильная потливость,
- дрожь в руках,
- сонливость.
- потеря веса.
Кто в группе риска?
- Население стран с низким уровнем жизни.
- Те, кто голодает с целью снизить вес или долго придерживается низкокалорийных диет.
- Пациенты с заболеваниями поджелудочной железы, печени и почек.
- Инсулинозависимые пациенты.
- Лица, родственники которых страдают наследственными формами нарушений углеводного обмена.
Общая информация о заболевании
Наряду с жирами и белком углеводы относятся к основным компонентам пищевого рациона. Они удовлетворяют потребность организма в энергии, участвуют в расщеплении жиров и белка.
Многие люди, пытаясь сбросить вес, ошибочно урезают количество углеводов в рационе до минимума, однако полноценная утилизация жиров возможна только при достаточном количестве углеводов.
Основные функции углеводов
- Энергетическая. При расщеплении углеводов образуется значительное количество энергии, обеспечивающей практически все процессы жизнедеятельности.
- Питание мозга. Головной мозг является основным потребителем глюкозы.

- Синтетическая. Углеводы участвуют в образовании многих необходимых организму веществ. Совместно с белками они образуют некоторые ферменты, гормоны, входят в состав слюны и пищеварительных соков.
- Регуляторная. Углеводы участвуют в процессе расщепления жиров и белка.
- Пищеварительная. Стимулируют процесс пищеварения, создавая объем пищевого комка.
- Сорбирующая. Способствуют выведению из организма избытков холестерина и вредных веществ.
Разнообразие выполняемых функций обеспечивается за счет особенностей химического строения углеводов. Принято различать следующие их виды.
- Простые сахара: глюкоза, фруктоза, лактоза, сахароза. Выполняют функцию источников «быстрой» энергии, главным из которых является глюкоза. Именно она используется клетками в первую очередь и является основой питания мозга. Уровень глюкозы в крови регулируется с помощью инсулина – особого белка (гормона), вырабатываемого поджелудочной железой, – и в норме относительно постоянен. При значительном поступлении углеводов с пищей часть их используется на поддержание уровня глюкозы, а остальные резервируются в печени и мышечной ткани.
- Сложные сахара: крахмал, гликоген клетчатка и пектины.
- Крахмал – основной углевод, поступающий с пищей. Содержится в крупах, картофеле, хлебе. В процессе переваривания расщепляется до глюкозы.
- Гликоген, или «животный крахмал», является формой хранения углеводов в организме. Основная масса гликогена содержится в печени, где и происходит его расщепление до глюкозы при необходимости восстановления ее уровня в крови.
- Клетчатка (целлюлоза) – практически неперевариваемый углевод, образующий оболочки семян и плодов. Клетчатка практически не участвует в углеводном обмене, но необходима организму для нормального пищеварения: создавая объем пищевого комка, она способствует насыщению и, кроме того, выведению холестерина и вредных веществ.
Таким образом, для обеспечения потребностей организма в первую очередь расходуются простые углеводы (глюкоза), уровень которых восполняется либо за счет поступления с пищей, либо за счет собственных запасов при расщеплении гликогена.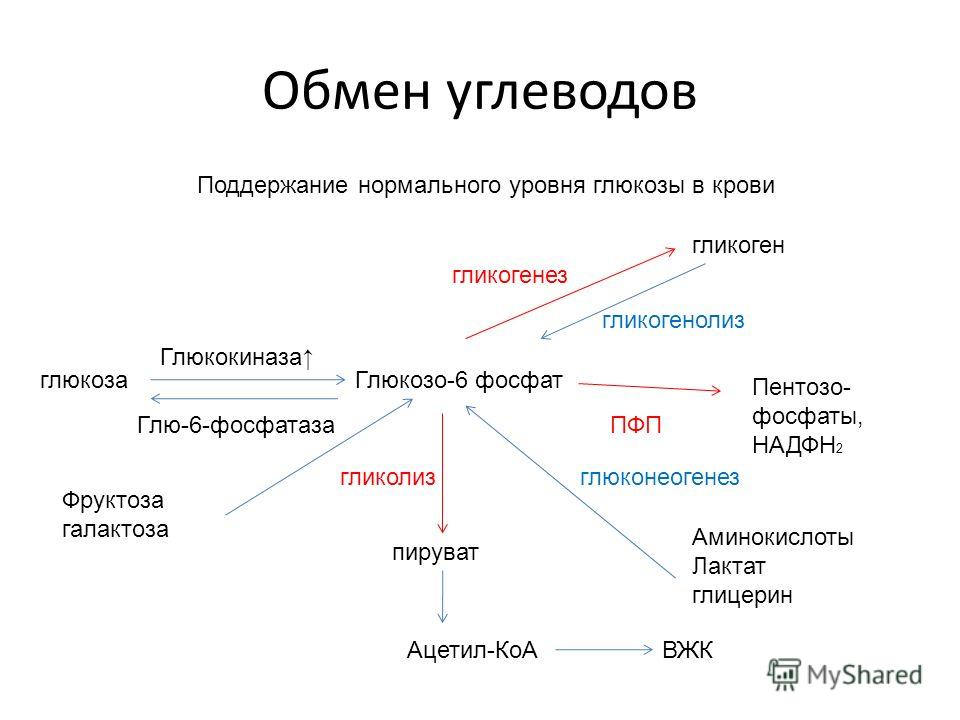 Если же собственный углеводный резерв исчерпан, организм начинает использовать имеющийся жир и белки, поэтому длительная нехватка углеводов приводит к серьезным нарушениям обмена и образованию целого ряда вредных веществ, постепенно накапливающихся в крови. К числу таких веществ относятся продукты неполного расщепления жира: кетоновые тела и ацетон. Этот процесс представляет серьезную опасность и даже может привести к коме. Избыточный расход белка вызывает уменьшение мышечной массы, нарушение целого ряда жизненно важных процессов, таких как продукция гормонов, основных белков крови, пищеварительных ферментов, что чревато тяжелыми формами дистрофии, снижением работоспособности и интеллекта.
Если же собственный углеводный резерв исчерпан, организм начинает использовать имеющийся жир и белки, поэтому длительная нехватка углеводов приводит к серьезным нарушениям обмена и образованию целого ряда вредных веществ, постепенно накапливающихся в крови. К числу таких веществ относятся продукты неполного расщепления жира: кетоновые тела и ацетон. Этот процесс представляет серьезную опасность и даже может привести к коме. Избыточный расход белка вызывает уменьшение мышечной массы, нарушение целого ряда жизненно важных процессов, таких как продукция гормонов, основных белков крови, пищеварительных ферментов, что чревато тяжелыми формами дистрофии, снижением работоспособности и интеллекта.
Главное проявление углеводного дефицита – это гипогликемия – низкий уровень глюкозы в крови.
Основные причины углеводной недостаточности
- Сахарный диабет – основная причина гипогликемии. Падение уровня глюкозы чаще всего связано с передозировкой инсулина (гормона, регулирующего уровень глюкозы), таблетированных сахароснижающих препаратов или же может явиться следствием нарушений режима питания, стресса или физического перенапряжения у этих пациентов.
- Физиологическая гипогликемия представляет собой незначительное кратковременное падение сахара в крови у лиц, занимающихся тяжелым физическим трудом, спортсменов в период максимальных нагрузок, а также при стрессовых ситуациях.
- Алиментарная (пищевая) углеводная недостаточность развивается при длительном голодании, например с целью снизить вес, при избыточном приеме алкоголя. Кроме того, сахар может падать из-за значительного перерыва между приемами пищи. Обычно это проявляется слабостью чувством голода.
- Инсулинома – опухоль поджелудочной железы, затрагивающая клетки, продуцирующие инсулин. По мере роста опухоли содержание инсулина в крови увеличивается и падения уровня глюкозы могут быть весьма значительными.
- Злокачественные опухоли могут стать причиной углеводной недостаточности за счет потребления глюкозы опухолевой тканью, а также при развитии синдрома опухолевой интоксикации.
 При распаде опухоли в кровь попадают чужеродные белки, вызывающие отравление организма. Это может приводить к снижению аппетита и к алиментарной углеводной недостаточности. Кроме того, некоторые опухоли способны производить вещества, воспринимаемые организмом как инсулин.
При распаде опухоли в кровь попадают чужеродные белки, вызывающие отравление организма. Это может приводить к снижению аппетита и к алиментарной углеводной недостаточности. Кроме того, некоторые опухоли способны производить вещества, воспринимаемые организмом как инсулин. - Надпочечниковая недостаточность. Одной из функций гормонов, вырабатываемых надпочечниками (в основном кортизола и адреналина), является регуляция углеводного обмена, в частности образования гликогена и его обратного расщепления до глюкозы. Поэтому недостаточная функция надпочечников, а также регулирующего их работу гипофиза иногда сопровождается гипогликемией.
- Почечная недостаточность. Приводит к падению уровня глюкозы как из-за снижения аппетита (почечная интоксикация), так и из-за более длительной циркуляции инсулина в крови вследствие нарушенной почечной фильтрации.
- Заболевания печени – нарушение образования и распада гликогена в клетках печени. Например, гепатиты, цирроз печени, жировая дистрофия.
- Пищеварительные нарушения углеводного обмена объединяют врождённые и приобретенные состояния, при которых нарушается расщепление и всасывание углеводов в пищеварительном тракте.
а) Приобретенные нарушения чаще всего носят временный характер и устраняются лечением. Наиболее распространенными являются:
- снижение уровня амилазы (основной фермент пищеварительного сока, ответственный за расщепление углеводов) у пациентов с хроническим панкреатитом и опухолями поджелудочной железы;
- снижение ферментативной активности кишечного содержимого при острых и хронических кишечных инфекциях, а также после операций на тонкой кишке.
б) Врождённые ферментопатии характеризуются отсутствием или низким уровнем отдельных ферментов, отвечающих за расщепление сложных углеводов. Наиболее известным примером является врождённая недостаточность лактазы – фермента, отвечающего за усвоение молочного сахара. Заболевание выявляется у новорождённых и характеризуется вздутием живота, жидким стулом, потерей веса. В качестве лечения предлагается переход на смеси, не содержащие лактозу.
В качестве лечения предлагается переход на смеси, не содержащие лактозу.
Диагностика
Углеводная недостаточность может быть заподозрена у пациентов с дефицитом массы тела, а также у лиц, входящих в группу риска: страдающих сахарным диабетом, заболеваниями печени, почек, поджелудочной железы. Для подтверждения диагноза назначаются следующие исследования.
Лабораторные исследования
- Общий анализ крови относится к числу базовых исследований, позволяющих получить представление об общем состоянии организма. Так как нарушения углеводного обмена не оказывают непосредственного влияния на клеточный состав крови, возможные изменения будут являться следствием основного процесса. Эритроциты и гемоглобин могут быть понижены. Лейкоциты. Изменение числа лейкоцитов для углеводной недостаточности нехарактерно, их количество может уменьшаться на фоне общего истощения.
- Скорость оседания эритроцитов (СОЭ). Значительное повышение СОЭ в сочетании с гипогликемией может указывать на наличие опухоли.
- Глюкоза (сахар крови). Определение уровня глюкозы является базовым исследованием в диагностике углеводной недостаточности. Стабильно низкие показатели глюкозы бывают вызваны врождённым гиперинсулинизмом и опухолями поджелудочной железы. При сахарном диабете и передозировке сахароснижающих препаратов уровень сахара при повторных исследованиях будет повышен.
- Инсулин в крови. Инсулин является одним из основных регуляторов углеводного обмена, отвечающим за уровень сахара в крови и обеспечивающим накопление гликогена в клетках печени. Повышенный уровень инсулина как причина низкого сахара крови может наблюдаться у пациентов с инсулиномой (злокачественной инсулинпродуцирующей опухолью поджелудочной железы) и с врождённым гиперинсулинизмом, а также при передозировке инсулина у пациентов с сахарным диабетом.
- Определение уровня проинсулина в крови может назначаться при подозрении на инсулинпродуцирующую опухоль поджелудочной железы.
 Проинсулин – белок – предшественник инсулина и в значительном количестве может определяться в крови пациентов с инсулиномой, гипогликемией, почечной и печеночной недостаточностью.
Проинсулин – белок – предшественник инсулина и в значительном количестве может определяться в крови пациентов с инсулиномой, гипогликемией, почечной и печеночной недостаточностью. - С-пептид. Представляет собой фрагмент белка – предшественника инсулина. Количество его пропорционально количеству образующегося инсулина, но так как С-пептид не участвует в обменных процессах, то его определение дает более достоверную информацию об уровне секреции этого гормона поджелудочной железой. Повышенный уровень С-пептида у пациентов после удаления гормонально активных опухолей поджелудочной железы может указывать на рецидив.
- Глюкозотолерантный тест. Определение уровня глюкозы крови до приема раствора глюкозы и через полчаса, 1 час и через 2 часа после него назначается пациентам при подозрении на нарушенное усвоение углеводов.
- Белок в сыворотке крови бывает понижен при углеводной недостаточности из-за использования белка в качестве источника энергии.
- Белковые фракции сыворотки крови. Исследование количественного состава и соотношения различных видов белка в сыворотке крови. Общий белок сыворотки представлен альбуминами и глобулинами, выполняющими в организме различные функции. Основную часть составляет альбумин – основной строительный белок организма. Так как при углеводной недостаточности альбумины начинают использоваться для восполнения энергозатрат, уровень их в плазме может снижаться при сохраненном показателе глобулинов.
- Мочевина и креатинин в сыворотке крови. Мочевина и креатинин являются веществами, образующимися в процессе распада белков. При выраженной углеводной недостаточности, сопровождающейся разрушением белка, их количество в крови может увеличиваться. Показатель следует оценивать вместе с уровнем мочевины в суточной моче.
- Мочевина в суточной моче отражает эффективность работы почек. При интенсивном распаде белка и сохраненной почечной функции может существенно повышаться.
- Лактаза (LCT).
 Выявление мутации C(-13910)T (регуляторная область гена). Исследование может быть назначено при подозрении на врождённый недостаток лактазы – пищеварительного фермента, обеспечивающего усвоение молочного сахара в желудочно-кишечном тракте. Представляет собой генетический анализ на измененные гены в соскобе щечной области. Положительный тест позволяет отличить врождённый дефицит фермента от приобретенных нарушений усвоения углеводов, как, например, при дисбактериозе.
Выявление мутации C(-13910)T (регуляторная область гена). Исследование может быть назначено при подозрении на врождённый недостаток лактазы – пищеварительного фермента, обеспечивающего усвоение молочного сахара в желудочно-кишечном тракте. Представляет собой генетический анализ на измененные гены в соскобе щечной области. Положительный тест позволяет отличить врождённый дефицит фермента от приобретенных нарушений усвоения углеводов, как, например, при дисбактериозе. - Кортизол. Гормон коры надпочечников, при недостаточной продукции которого уровень глюкозы в крови может снижаться. Исследование назначается при подозрении на надпочечниковую недостаточность как причину гипогликемии.
- Общий анализ мочи с микроскопией осадка при углеводной недостаточности назначают для определения уровня ацетона в моче. При углеводном дефиците организм начинает использовать запасы жира для восполнения энергозатрат. Так как расщепление жира при этом механизме происходит не полностью, в крови накапливаются промежуточные вещества, в том числе и ацетон, в дальнейшем выделяемый с мочой.
- Копрограмма – исследование кала, позволяющее выявить возможные нарушения основных этапов переваривания углеводов. Оценивается химический состав каловых масс, его цвет, запах консистенция, наличие отдельных видов микроорганизмов (дисбактериоз). Исследование позволяет оценить работу основных ферментов печени, желудочного и кишечного сока, поджелудочной железы. При углеводной недостаточности, вызванной нарушенным усвоением углеводов, в каловых массах могут определяться зерна крахмала.
Дополнительные (инструментальные) методы исследования
Объем диагностических исследований зависит от предполагаемой причины углеводной недостаточности и должен определяться лечащим врачом.
- Ультразвуковое исследование печени, почек, надпочечников и поджелудочной железы относится к базовым методикам, позволяющим оценить состояние этих органов. В отличие от рентгенологических методов исследования оно не сопряжено с лучевой нагрузкой и безопасно для пациента.
 Ультразвук проходит сквозь мягкие ткани до исследуемого органа и, отразившись, возвращается обратно. Полученное изображение передается на монитор. Исследование позволяет оценить размеры указанных органов, структуру тканей, выявить опухолевое поражение или кисту, исключить наличие жидкости в брюшной полости. При необходимости исследование может быть дополнено взятием биопсии под УЗИ-контролем.
Ультразвук проходит сквозь мягкие ткани до исследуемого органа и, отразившись, возвращается обратно. Полученное изображение передается на монитор. Исследование позволяет оценить размеры указанных органов, структуру тканей, выявить опухолевое поражение или кисту, исключить наличие жидкости в брюшной полости. При необходимости исследование может быть дополнено взятием биопсии под УЗИ-контролем. - Эзофагогастродуоденоскопия – непосредственный осмотр пищевода, желудка и двенадцатиперстной кишки с помощью специального зонда, на дистальном конце которого размещена видеокамера. Оценивается проходимость верхних отделов пищеварительного тракта, состояние слизистой оболочки, степень ее воспаления или атрофии. В процессе исследования может быть взят фрагмент ткани на анализ (биопсия). Наряду с ультразвуковым исследованием гастроскопия является обязательной при подозрении на алиментарный характер углеводной недостаточности.
- Энтероскопия (интестиноскопия). Осмотр тонкой кишки. Исследование по своим возможностям аналогично гастроскопии, но технически более сложно, так как предусматривает осмотр всей тонкой кишки. Оно позволяет оценить состояние слизистой оболочки, исключить эрозивное поражение, а также взять содержимое для исключения инфекционного процесса или определения уровня отдельных ферментов, например амилазы – основного фермента, участвующего в расщеплении углеводов.
- Эндосонография поджелудочной железы (эндоскопическое УЗИ) представляет собой разновидность ультразвукового исследования поджелудочной железы. Выполняется с помощью специального датчика, размещенного на конце эндоскопа. Считается «золотым стандартом» в диагностике гормонпродуцирующих опухолей, так как с его помощью можно диагностировать образования менее 1 сантиметра, не выявляемые другими методами.
- Компьютерная томография органов брюшной полости позволяет получить послойные срезы поджелудочной железы и может быть назначена пациентам с подозрением на опухоль этого органа.

- Рентгенологическое исследование может быть назначено пациентам, перенесшим операцию на тонкой кишке, для оценки ее длины и просвета. Удаление значительной части тонкого кишечника способно явиться причиной тяжелых расстройств пищеварения, в том числе и углеводной недостаточности.
Лечение
Лечение углеводной недостаточности направлено на восстановление уровня углеводов, а в более тяжелых случаях на нормализацию белкового и жирового обмена.
- Сбалансированное питание, обеспечивающее суточную потребность в углеводах. В рационе должно быть достаточное количество овощей, фруктов, зерновых продуктов (хлеба, круп). Пациенты с углеводной недостаточностью, обусловленной избыточной продукцией инсулина, должны носить с собой содержащие глюкозу таблетки, конфеты или обычный сахар. Такая коррекция режима питания может оказаться единственной необходимой мерой у пациентов с легкими формами гипогликемии. При углеводной недостаточности, обусловленной заболеваниями печени и почек, врождёнными ферментативными нарушениями, диета должна подбираться лечащим врачом с учетом особенностей течения основного заболевания.
- Медикаментозные средства:
- Отдельные пищеварительные ферменты или комплексные ферментные препараты могут быть назначены пациентам с приобретенным ферментным дефицитом.
- Специальные смеси для питания со строго подобранным углеводным составом могут назначаться пациентам с врождённым и приобретенным нарушением усвояемости отдельных углеводов. При углеводной недостаточности, сопровождающейся потерей белка, могут быть рекомендованы соответствующие белково-углеводные смеси.
- Внутривенное введение глюкозы иногда требуется пациентам с тяжелой степенью гипогликемии, особенно при наличии инсулинпродуцирующей опухоли.
- Хирургическое лечение бывает необходимо пациентам, у которых углеводная недостаточность обусловлена опухолевым процессом
Профилактика
- Полноценное питание с включением в рацион достаточного количества углеводной пищи (свежие фрукты и овощи более предпочтительны, бобовые продукты и зерновые).

- Обязательный врачебный контроль при подборе ограничительной диеты или проведении курсов лечебного голодания.
- Своевременное выявление и лечение заболеваний, увеличивающих риск нарушений углеводного обмена.
Рекомендуемые анализы
- Общий анализ крови
- Лейкоцитарная формула
- Скорость оседания эритроцитов (СОЭ)
- Глюкоза в плазме
- Инсулин
- Проинсулин
- С-пептид в сыворотке
- Глюкозотолерантный тест
- Кортизол
- Лактозная непереносимость у взрослых
- Мочевина в суточной моче
- Белок общий в сыворотке
- Белковые фракции в сыворотке
- Общий анализ мочи с микроскопией осадка
- Копрограмма
Диагностика нарушений обмена веществ
Обмен веществ
— набор химических реакций, которые возникают в живом организме для поддержания жизни. Благодаря обмену веществ у человека выделяется энергия, происходят процессы восстановления, обновления. При некоторых неблагоприятных условиях нарушаются эти важные обменные процессы, что может привести к возникновению ряда заболеваний, таких как сахарный диабет, ожирение, снижение иммунитета и других.
Все заболевания, связанные с нарушением обменных процессов в организме, условно делятся на 4 группы:
- Патологии, связанные с нарушением белкового, углеводного и жирового обмена. К ним относятся ожирение, миоглобулинурия, кетоз, алиментарная дистрофия.
- Заболевания, причиной которых является нарушение минерального обмена.
- Патологии, вызванные нехваткой или избытком минералов.
- Гиповитаминозы
Основными причинами этих нарушений являются: наследственность, гиподинамия, отравления, стрессы, неправильное питание, регулярный прием лекарственных препаратов.
Нарушение обменных процессов в организме проявляется следующими признаками: ухудшение внешнего вида, нездоровый цвет кожи, нарушение процессов пищеварения, разрушение зубов, изменение структуры волос и ногтей, отеки, одышка, изменение веса (резкий набор или снижение), повышенная потливость, хруст в суставах, судороги в икроножных мышцах. В более тяжелых случаях возможны изменения со стороны психики (депрессия, плаксивость, раздражительность), бесплодие и другое. Нарушение обмена веществ бывает не только у взрослых, но и у детей. Опасность этого заключается в том, что у детей обменные процессы протекают очень интенсивно и происходит формирование жизненно важных органов, поэтому нарушение режима питания, сна и отдыха приводят к таким опасным заболеваниям как рахит, анемия, амилоидоз, нарушение умственного развития.
Для того чтобы поставить правильный диагноз и назначить лечение, проводится комплексное обследование пациента, которое может включать следующие этапы:
- Консультация врача
- Опрос и осмотр пациента (выяснение истории болезни, измерение роста, взвешивание, полное физическое обследование, измерение АД и другое)
- ЭКГ
- УЗИ и КТ
- Лабораторные методы исследования (анализы крови, мочи, волос)
Анализы крови включают в себя исследование жирового обмена (холестерин, триглицериды, ЛПНП, ЛПВП, Омега-3, лептин, кортизол и др.), углеводного обмена (глюкоза, гликированый гемоглобин, инсулин, индекс НОМА) и белкового обмена (общий белок, альбумин, креатинкиназа и др.). С помощью анализа крови на витамины и минералы можно выявить дефицит витаминов группы В, жирорастворимых витаминов А, Д, Е, К, витамина С, а также нарушение содержания минералов (калия, кальция, магния и других).
Возврат к списку
Осуществление и регуляция углеводного обмена
Prog Mol Biol Transl Sci. Авторская рукопись; доступно в PMC 2016 26 января.
Опубликован в окончательной редакции как:
PMCID: PMC4727532
NIHMSID: NIHMS752019
Joram D. Mul
* Секция интегративной физиологии и метаболизма, Jos Гарвардская медицинская школа, Бостон, Массачусетс, США
Кристин И. Стэнфорд
* Секция интегративной физиологии и метаболизма, Центр диабета Джослина, Гарвардская медицинская школа, Бостон, Массачусетс, США
Майкл Ф.Hirshman
* Секция интегративной физиологии и метаболизма, Центр диабета Джослина, Гарвардская медицинская школа, Бостон, Массачусетс, США
Laurie J. Goodyear
* Секция интегративной физиологии и метаболизма, Центр диабета Джослина, Гарвардский медицинский центр School, Бостон, Массачусетс, США
† Департамент медицины, Бригам и женская больница, Гарвардская медицинская школа, Бостон, Массачусетс, США
* Секция интегративной физиологии и метаболизма, Центр диабета Джослина, Гарвардская медицинская школа , Бостон, Массачусетс, США
† Департамент медицины, Бригам и женская больница, Гарвардская медицинская школа, Бостон, Массачусетс, США
См. Другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Углеводы являются предпочтительным субстратом для сокращения скелетных мышц во время упражнений высокой интенсивности, а также легко используются во время упражнений средней интенсивности. Такое использование углеводов во время физической активности, вероятно, сыграло важную роль во время выживания первых Homo sapiens , а гены и черты, регулирующие физическую активность, углеводный обмен и накопление энергии, несомненно, выбирались на протяжении всей эволюции. В отличие от жизни начала г.sapiens , современный образ жизни преимущественно малоподвижный. В результате потребление чрезмерного количества углеводов из-за легкой и постоянной доступности современных высокоэнергетических продуктов питания и напитков не только стало ненужным, но и привело к метаболическим заболеваниям при отсутствии физической активности. Возникающим в результате метаболическим заболеванием является диабет 2 типа, сложное эндокринное заболевание, характеризующееся аномально высокими концентрациями циркулирующей глюкозы. Эта болезнь сейчас поражает миллионы людей во всем мире.Упражнения оказывают благотворное влияние, помогая контролировать нарушенный гомеостаз глюкозы при метаболических нарушениях, и являются хорошо зарекомендовавшим себя средством предотвращения и борьбы с диабетом 2 типа. В этой главе основное внимание уделяется влиянию физических упражнений на метаболизм углеводов в скелетных мышцах и системный гомеостаз глюкозы. Мы также сосредоточимся на молекулярных механизмах, которые опосредуют эффекты физических упражнений по увеличению поглощения глюкозы скелетными мышцами. В настоящее время хорошо установлено, что существуют различные проксимальные сигнальные пути, которые опосредуют влияние упражнений и инсулина на поглощение глюкозы, и эти различные механизмы согласуются со способностью физических упражнений увеличивать поглощение глюкозы в условиях инсулинорезистентности у людей с типом 2. сахарный диабет.Текущие исследования в этой области направлены на определение точного механизма, с помощью которого упражнения увеличивают усвоение глюкозы и чувствительность к инсулину, а также типы упражнений, необходимые для этой важной пользы для здоровья.
Возникающим в результате метаболическим заболеванием является диабет 2 типа, сложное эндокринное заболевание, характеризующееся аномально высокими концентрациями циркулирующей глюкозы. Эта болезнь сейчас поражает миллионы людей во всем мире.Упражнения оказывают благотворное влияние, помогая контролировать нарушенный гомеостаз глюкозы при метаболических нарушениях, и являются хорошо зарекомендовавшим себя средством предотвращения и борьбы с диабетом 2 типа. В этой главе основное внимание уделяется влиянию физических упражнений на метаболизм углеводов в скелетных мышцах и системный гомеостаз глюкозы. Мы также сосредоточимся на молекулярных механизмах, которые опосредуют эффекты физических упражнений по увеличению поглощения глюкозы скелетными мышцами. В настоящее время хорошо установлено, что существуют различные проксимальные сигнальные пути, которые опосредуют влияние упражнений и инсулина на поглощение глюкозы, и эти различные механизмы согласуются со способностью физических упражнений увеличивать поглощение глюкозы в условиях инсулинорезистентности у людей с типом 2. сахарный диабет.Текущие исследования в этой области направлены на определение точного механизма, с помощью которого упражнения увеличивают усвоение глюкозы и чувствительность к инсулину, а также типы упражнений, необходимые для этой важной пользы для здоровья.
1. ВВЕДЕНИЕ
Уникальная способность людей к бегу на выносливость, вероятно, способствовала эволюции Homo sapiens от других приматов. 1 Высокий уровень физической активности требовался для того, чтобы избегать хищников и добывать пищу.Чтобы поддерживать такой высокий уровень физической активности, работающим скелетным мышцам требуется повышенное количество субстратов для выработки аденозинтрифосфата (АТФ). Основным субстратом для работающих мышц являются углеводы, одним из которых является сама мышца в виде гликогена, а другим источником глюкозы является кровь. Распад гликогена в мышцах (гликогенолиз) и регуляция поглощения глюкозы мышцами из крови — это строго регулируемые процессы, и в этой главе будут обсуждаться современные знания об этих функциях.
Поскольку использование углеводов способствует выживанию человека, гены и черты, регулирующие метаболизм углеводов во время физических упражнений и накопление энергии, выбирались на протяжении всей эволюции. 2 Однако нынешний образ жизни преимущественно малоподвижный, что в сочетании с чрезмерным потреблением углеводов привело к метаболическим заболеваниям, таким как диабет 2 типа. С другой стороны, упражнения благотворно влияют на метаболизм углеводов, и, как следствие, упражнения являются хорошо зарекомендовавшим себя средством предотвращения и борьбы с диабетом 2 типа.Также будут обсуждаться молекулярные механизмы, которые опосредуют эффекты физических упражнений на увеличение поглощения глюкозы скелетными мышцами и повышение чувствительности к инсулину у здоровых людей и людей с диабетом 2 типа.
2. ИСПОЛЬЗОВАНИЕ УГЛЕВОДОВ ВО ВРЕМЯ ОТДЫХА И ТРЕНИРОВКИ
В состоянии покоя энергия, используемая человеческим телом, в основном получается за счет окисления углеводов и жиров. Глюкоза в крови, свободные от плазмы жирные кислоты, мышечный гликоген и внутримышечные триглицериды являются основными источниками субстрата для производства энергии в скелетных мышцах. 3,4 Вклад белков в запас полезной энергии очень ограничен, так как окисление аминокислот обычно строго регулируется потреблением аминокислот.
В состоянии покоя прием углеводов приводит к высвобождению инсулина из поджелудочной железы, и, как следствие, повышение концентрации инсулина в плазме имеет множество метаболических эффектов. Одним из важных эффектов инсулина является ускорение транспорта глюкозы в скелетные мышцы. Инсулин также подавляет высвобождение жирных кислот из жировой ткани, увеличивая накопление жира за счет активации липопротеинлипазы. 5,6 Потребление физиологически нормальных уровней углеводов не влияет на уровни жировой ткани через de novo липогенез, 7 , что позволяет предположить, что человеческий организм может приспособиться к потреблению относительно большого количества углеводов без необходимости хранить углеводы в виде жира .
Сокращение скелетных мышц во время физических упражнений приводит к увеличению потребности мышц в энергии. Задача работающих мышц — увеличить производство АТФ, и несколько клеточных процессов функционируют для удовлетворения этой потребности.Соответственно, метаболические пути, которые окисляют как углеводы, так и жиры, должны активироваться одновременно. 3,4 Интенсивность, продолжительность и тип упражнения определяют механизмы, через которые поступает эта дополнительная энергия.
Фермент АТФаза способствует расщеплению АТФ до АДФ + неорганический фосфат (Pi) для выработки энергии для быстрого использования; однако в мышечных клетках присутствует лишь небольшое количество АТФ. 8 Дополнительным, но еще меньшим источником накопленной энергии является креатинфосфат, который может повторно синтезироваться в АТФ с помощью фермента креатинкиназы для восполнения истощенных уровней АТФ.Таким образом, основными источниками энергии во время упражнений являются углеводы и жиры. Источники углеводов для мышц включают глюкозу в крови, мышечный гликоген и гликоген печени. 9
Глюкоза и гликоген превращаются в глюкозо-6-фосфат, прежде чем их можно будет использовать для выработки энергии. Одна судьба глюкозо-6-фосфата — превращение в молочную кислоту, что приводит к образованию трех молекул АТФ на молекулу гликогена или двух молекул АТФ на молекулу глюкозы (анаэробный гликолиз).АТФ, генерируемый анаэробным гликолизом, недостаточно велик, чтобы поддерживать мышечную активность в течение длительного времени. При субмаксимальных упражнениях потребление кислорода увеличивается, и в течение нескольких минут достигается устойчивое состояние. Это устойчивое состояние указывает на то, что аэробные процессы обеспечивают большую часть энергии, необходимой для сокращающихся мышц. Аэробная генерация АТФ из молекулы глюкозы во много раз эффективнее анаэробной реакции гликолиза. Во время аэробной реакции гликолиза гликоген превращается в пировиноградную кислоту, которая затем превращается в ацетил-КоА и используется для производства АТФ в цикле Кребса в митохондриях. Хотя основными видами топлива, участвующими в окислительном метаболизме во время упражнений, являются жиры и углеводы, в экстремальных условиях аминокислоты также могут использоваться в качестве источника окисления субстрата. 9
Хотя основными видами топлива, участвующими в окислительном метаболизме во время упражнений, являются жиры и углеводы, в экстремальных условиях аминокислоты также могут использоваться в качестве источника окисления субстрата. 9
В голодном состоянии и во время упражнений с низкой интенсивностью основная часть энергии, требуемой мышцам, обеспечивается за счет окисления свободных жирных кислот, которые преимущественно получают из плазмы. 10 Когда физическая нагрузка увеличивается до умеренного уровня интенсивности (60–70% VO 2 пик), источником жирных кислот для окисления также является внутримышечный триглицерид.Хотя оба источника жирных кислот способствуют потребности мышц в энергии, даже в сочетании их недостаточно для удовлетворения потребности в энергии. Таким образом, во время упражнений средней интенсивности около половины всей энергии, получаемой за счет окисления углеводов, поступает как из мышечного гликогена, так и из глюкозы в крови. 11 Во время упражнений высокой интенсивности вклад окисления жирных кислот плазмы становится еще меньше, а окисление углеводов обеспечивает примерно две трети общей потребности в энергии.Углеводный обмен является предпочтительным источником топлива в этих условиях, поскольку скорость производства АТФ в два раза выше, чем у жирных кислот. 9
3. МЫШЕЧНЫЙ ГЛИКОГЕН
Как отмечалось выше, гликоген является важным топливом для производства энергии в сокращающихся скелетных мышцах. Гликоген представляет собой разветвленный полимер глюкозы со смесью α-1,4- и α-1,6-связей между звеньями глюкозы. В печени самая высокая концентрация накопленного гликогена; тем не менее, скелетная мышца, в результате ее общей массы, является самым большим запасом гликогена в организме.Внутримышечный гликоген связан с несколькими органеллами, включая сарколемму, саркоплазматический ретикулум, митохондрии и миофибриллы. 3,12 Гранулы гликогена или гликосомы также физически связаны с несколькими белками, включая гликогенфосфорилазу, фосфорилазокиназу, гликогенсинтазу, гликогенин, протеинфосфатазы и протеинкиназу, активированную аденозинмонофосфатом (AMP). 3,12 В синтезе гликогена участвует множество ферментов, а гликогенсинтаза является ферментом, ограничивающим скорость.Распад гликогена (гликогенолиз) также контролируется мультиферментной системой, и это будет обсуждаться более подробно ниже.
3,12 В синтезе гликогена участвует множество ферментов, а гликогенсинтаза является ферментом, ограничивающим скорость.Распад гликогена (гликогенолиз) также контролируется мультиферментной системой, и это будет обсуждаться более подробно ниже.
Использование гликогена быстро начинается в начале тренировки и экспоненциально увеличивается с интенсивностью тренировки. 13 Регуляция гликогенолиза очень чувствительна к скорости метаболизма скелетных мышц во время физических упражнений. 14,15 Гликогенфосфорилаза — это фермент, ответственный за лимитирующую стадию во время мышечного гликогенолиза. 3,16 В состоянии покоя гликогенфосфорилаза существует в основном в неактивной форме b, тогда как с началом физической нагрузки киназа фосфорилазы фосфорилирует форму b до активной формы a. 3 Активация киназы фосфорилазы возникает в результате повышенного уровня кальция и связывания адреналина с β-адренорецепторами сарколеммы. Активация киназы фосфорилазы путем стимуляции β-адренорецепторов на сарколемме опосредуется циклическим АМФ. Повышенные уровни адреналина увеличивают активность гликогенфосфорилазы и гликогенолиз в перфузированных задних конечностях крыс и гликогенолиз у людей во время умеренных физических нагрузок. 16,17
Гликогенолиз мышц не всегда тесно коррелирует с уровнями киназы фосфорилазы а. 18 Это говорит о том, что посттрансляционные факторы увеличивают скорость гликогенолиза во время упражнений различной интенсивности. Действительно, уровни АМФ и аденозиндифосфата (АДФ), а также повышенные уровни Pi могут аллостерически регулировать активность a и b форм киназы фосфорилазы. 3 При увеличении продолжительности упражнений наблюдается снижение доступности гликогена параллельно со снижением активности фосфорилазы, в то время как увеличивается доступность других субстратов для окисления, таких как глюкоза плазмы и свободные жирные кислоты.
Тип мышечного волокна также может быть фактором, определяющим регуляцию мышечного гликогенолиза. Во время упражнений средней интенсивности гликогенолиз мышц происходит преимущественно в мышечных волокнах I типа. По мере увеличения продолжительности упражнений или увеличения их интенсивности волокна типа I истощаются, и увеличивающееся количество гликогена расщепляется в мышечных волокнах типа II. Таким образом, по мере увеличения интенсивности упражнений, соответственно увеличивается набор волокон типа II. При кратковременных упражнениях с интенсивностью, приближающейся и превышающей VO 2max , гликогенолиз происходит во всех волокнах, но самые высокие показатели — в волокнах типа II. 3
Во время упражнений средней интенсивности гликогенолиз мышц происходит преимущественно в мышечных волокнах I типа. По мере увеличения продолжительности упражнений или увеличения их интенсивности волокна типа I истощаются, и увеличивающееся количество гликогена расщепляется в мышечных волокнах типа II. Таким образом, по мере увеличения интенсивности упражнений, соответственно увеличивается набор волокон типа II. При кратковременных упражнениях с интенсивностью, приближающейся и превышающей VO 2max , гликогенолиз происходит во всех волокнах, но самые высокие показатели — в волокнах типа II. 3
Когда гликоген в мышцах истощается или почти истощается, наступает усталость и снижается способность к физической нагрузке. 14,15 Хотя продолжительность и интенсивность упражнений играют роль в регулировании распада гликогена в мышцах, история диеты и статус тренировок также регулируют гликогенолиз мышц во время упражнений. В целом, повышенное потребление углеводов связано с большей утилизацией гликогена в мышцах, тогда как увеличение потребления жиров приводит к снижению утилизации гликогена в мышцах во время упражнений. 3 Это ослабление мышечного гликогенолиза во время упражнений после приема диеты с высоким содержанием жиров, по-видимому, зависит от метаболических адаптаций, возникающих в результате диеты с высоким содержанием жиров, и не зависит от наличия мышечного гликогена, которое было аналогичным в начале упражнения. 19 После тренировки активируется гликогенсинтаза, и концентрация мышечного гликогена увеличивается в мышцах в состоянии покоя. 20,21 Несмотря на это увеличение уровня гликогена в мышцах в состоянии покоя, гликогенолиз мышц снижается во время динамических упражнений после краткосрочных тренировок на выносливость. 22 Это снижение гликогенолиза мышц способствует хорошо описанному увеличению окислительной способности мышц. 22
4. ТРАНСПОРТИРОВКА ГЛЮКОЗЫ
Другим важным источником углеводов во время физических упражнений является циркулирующая в крови глюкоза.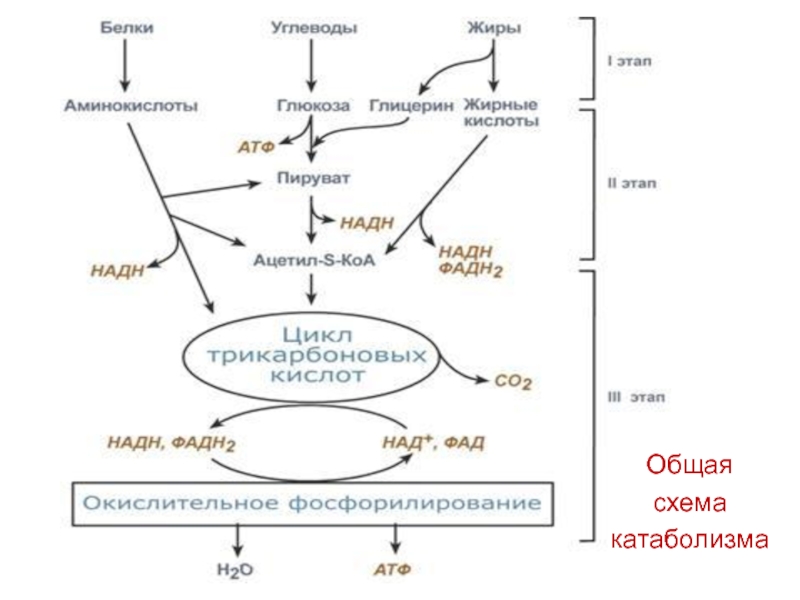 Концентрация глюкозы в крови во время упражнений контролируется точным регуляторным механизмом, а источником циркулирующей глюкозы в первую очередь является печень. В состоянии покоя потребление пищи также регулирует концентрацию глюкозы в крови, и удаление глюкозы из кровообращения в ответ как на потребление пищи, так и на физические упражнения, является критическим фактором для поддержания нормальной гликемии у людей.
Концентрация глюкозы в крови во время упражнений контролируется точным регуляторным механизмом, а источником циркулирующей глюкозы в первую очередь является печень. В состоянии покоя потребление пищи также регулирует концентрацию глюкозы в крови, и удаление глюкозы из кровообращения в ответ как на потребление пищи, так и на физические упражнения, является критическим фактором для поддержания нормальной гликемии у людей.
Транспорт глюкозы в скелетные мышцы важен для гомеостаза тканей, и в нормальных физиологических условиях процесс транспорта ограничивает скорость утилизации глюкозы. 23 Транспорт происходит за счет облегченной диффузии, при этом максимальная скорость транспорта увеличивается без заметного изменения концентрации субстрата, при которой транспорт глюкозы наполовину максимален. 24 Транспорт глюкозы использует специфические белки-носители, называемые переносчиками глюкозы, которые представляют собой семейство структурно родственных белков, которые экспрессируются тканеспецифическим образом. 25 В скелетных мышцах грызунов и людей GLUT4 является основной экспрессируемой изоформой, тогда как экспрессия изоформ GLUT1, GLUT5 и GLUT12 намного ниже. 26–28 Исследования, в которых было генетическое устранение GLUT4 в скелетных мышцах мышей, показывают, что GLUT4 необходим для нормальной скорости базального, инсулинового и стимулируемого физической нагрузкой транспорта глюкозы. 29,30
Механизм, с помощью которого упражнения увеличивают транспорт глюкозы через транспортер GLUT4, является областью интенсивных исследований в течение многих лет.Точно так же был большой интерес к пониманию механизма воздействия инсулина на транспорт глюкозы. Ранние исследования с использованием субклеточного фракционирования скелетной мышечной ткани, 31,32 и недавние работы с использованием конфокальной микроскопии in vivo, , 33,34 четко установили, что как упражнения, так и инсулин увеличивают транспорт глюкозы в скелетных мышцах за счет перемещения GLUT4 из внутриклеточного компартмента в сарколемму и поперечные канальцы. Процесс транслокации GLUT4 очень сложен и включает множество клеточных процессов. В скелетных мышцах перемещение переносчиков происходит посредством экзоцитоза, доставки, стыковки и слияния GLUT4-содержащих отсеков хранения или «пузырьков» с мембранами клеточной поверхности. Наши знания о составе, специфичности и перемещении везикул GLUT4 увеличились в последние годы, хотя они все еще не полностью изучены. 35 Имеются убедительные доказательства того, что множественные растворимые белки рецептора белка прикрепления N -этилмалеимида (SNARE) регулируют стыковку и слияние GLUT4-содержащих везикул.При стимуляции, такой как упражнения, сокращение мышц или инсулин, ассоциированные с везикулами белки SNARE (v-SNARE), включая ассоциированный с везикулами мембранный белок-2 (VAMP-2), связываются с белками SNARE мембраны-мишени (t-SNARE). ), которые включают синтаксин 4 и SNAP23. Считается, что этот комплекс способствует слиянию везикул, содержащих GLUT4, с мембраной клеточной поверхности. В исследованиях на мышах с гетерозиготным нокаутом по синтаксину 4 было показано, что синтаксин 4 является основной молекулой, ответственной за регуляцию индуцированного инсулином перераспределения GLUT4 и транспорта глюкозы в скелетных мышцах. 36 Роль белков SNARE в транслокации GLUT4, стимулированной физической нагрузкой, менее изучена, хотя было показано, что VAMP2 перемещается на поверхность клетки в ответ на физическую нагрузку. 37
Процесс транслокации GLUT4 очень сложен и включает множество клеточных процессов. В скелетных мышцах перемещение переносчиков происходит посредством экзоцитоза, доставки, стыковки и слияния GLUT4-содержащих отсеков хранения или «пузырьков» с мембранами клеточной поверхности. Наши знания о составе, специфичности и перемещении везикул GLUT4 увеличились в последние годы, хотя они все еще не полностью изучены. 35 Имеются убедительные доказательства того, что множественные растворимые белки рецептора белка прикрепления N -этилмалеимида (SNARE) регулируют стыковку и слияние GLUT4-содержащих везикул.При стимуляции, такой как упражнения, сокращение мышц или инсулин, ассоциированные с везикулами белки SNARE (v-SNARE), включая ассоциированный с везикулами мембранный белок-2 (VAMP-2), связываются с белками SNARE мембраны-мишени (t-SNARE). ), которые включают синтаксин 4 и SNAP23. Считается, что этот комплекс способствует слиянию везикул, содержащих GLUT4, с мембраной клеточной поверхности. В исследованиях на мышах с гетерозиготным нокаутом по синтаксину 4 было показано, что синтаксин 4 является основной молекулой, ответственной за регуляцию индуцированного инсулином перераспределения GLUT4 и транспорта глюкозы в скелетных мышцах. 36 Роль белков SNARE в транслокации GLUT4, стимулированной физической нагрузкой, менее изучена, хотя было показано, что VAMP2 перемещается на поверхность клетки в ответ на физическую нагрузку. 37
Когда скелетные мышцы стимулируются одновременно сокращением и лечением инсулином, есть аддитивные или частично аддитивные эффекты на транспорт глюкозы. 24,38 В соответствии с этими выводами, комбинация физических упражнений и инсулина может иметь аддитивный эффект на транслокацию GLUT4 в сарколемму. 38 Эти данные подтверждают идею о том, что существуют различные механизмы, приводящие к стимуляции транспорта глюкозы в мышцах с помощью упражнений и инсулина. 39
5.
 СИГНАЛЫ ТРЕНИРОВКИ, РЕГУЛИРУЮЩИЕ ТРАНСПОРТ ГЛЮКОЗЫ
СИГНАЛЫ ТРЕНИРОВКИ, РЕГУЛИРУЮЩИЕ ТРАНСПОРТ ГЛЮКОЗЫВнутриклеточные сигнальные белки, которые регулируют увеличение транслокации GLUT4 и транспорта глюкозы в скелетных мышцах при упражнениях, также были областью интенсивных исследований в течение последних 10 лет. Поскольку инсулин и физические упражнения стимулируют транслокацию GLUT4, было высказано предположение, что в процессе транслокации могут быть задействованы сходные сигнальные белки.Передача сигналов инсулина включает быстрое фосфорилирование рецептора инсулина, субстрата-1/2 рецептора инсулина (IRS-1/2) по остаткам тирозина и активацию фосфатидилинозитол-3-киназы (PI3-K). 40,41 Напротив, упражнения не приводят к фосфорилированию тирозина рецептора инсулина и IRS-1, и нет увеличения активности PI3-K. 42,43 Дополнительные доказательства того, что упражнения могут увеличивать транспорт глюкозы в отсутствие инсулиновой передачи сигналов, получены из исследования мышей, у которых отсутствуют рецепторы инсулина в скелетных мышцах (мышечные специфические рецепторы инсулина KO; MIRKO). 44,45 В то время как эти мыши имеют притупленный инсулино-стимулированный транспорт глюкозы, 45 они имеют нормальный стимулируемый физической нагрузкой транспорт глюкозы. 44 Взятые вместе, эти исследования показывают, что инсулин и физические упражнения опосредуют транслокацию GLUT4 в скелетных мышцах посредством различных проксимальных сигнальных механизмов.
Хорошо известно, что одна тренировка активирует несколько сигнальных путей 46–48 ; однако точный сигнальный механизм, который обеспечивает транспорт глюкозы, стимулируемый физической нагрузкой, до сих пор полностью не изучен.Сократительная активность мышц приводит к многочисленным изменениям в мышечных волокнах, включая изменения энергетического статуса (например, повышение АМФ / АТФ), повышение внутриклеточной концентрации Ca 2+ , увеличение количества активных форм кислорода и растяжение мышечных волокон. Эти модификации могут активировать различные сигнальные каскады, некоторые из которых вовлечены в стимулируемый физической нагрузкой транспорт глюкозы 49,50 ().
Эти модификации могут активировать различные сигнальные каскады, некоторые из которых вовлечены в стимулируемый физической нагрузкой транспорт глюкозы 49,50 ().
Предлагаемая модель сигнальных путей, опосредующих транспорт глюкозы в скелетных мышцах, индуцированный физической нагрузкой и инсулином.Инсулин инициируется связыванием с его рецептором клеточной службы, что приводит к каскаду реакций фосфорилирования с участием IRS-1, PI 3-киназы и Akt среди других белков. Упражнения работают через проксимальный сигнальный механизм, отличный от механизма инсулина, и он менее четко определен. Вероятно, что проксимальный сигнальный механизм при физической нагрузке имеет избыточность, поскольку в этот процесс вовлечено множество стимулов, включая изменения внутриклеточного Ca 2+ , соотношение АМФ: АТФ, образование активных форм кислорода и механические стрессы.Считается, что сигнальные пути инсулина и физических упражнений сходятся на уровне белков Rab GAP TBC1D1 и AS160, которые позволяют высвобождать содержащие GLUT4 везикулы из внутриклеточных хранилищ, перемещаться в поперечные канальцы и сарколемму и повышать уровень глюкозы. поглощение. Адаптировано из Ref. 50.
5.1 AMPK и LKB1
AMPK представляет собой гетеротримерный белок, состоящий из каталитической α-субъединицы и регуляторных β- и γ-субъединиц. Каждая из α- и β-субъединиц существует в двух изоформах (α1, α2 и β1, β2), а γ-субъединица существует в трех изоформах (γ1, γ2 и γ3).AMPK активируется путем фосфорилирования одной или несколькими вышестоящими киназами, включая LKB1. 52–54
AMPK и LKB1 были широко изучены на предмет их потенциальной роли в транспорте глюкозы, стимулированном физической нагрузкой. 55 Первоначальные доказательства роли AMPK в транспорте глюкозы, стимулированном физической нагрузкой, были получены в исследованиях с использованием аналога AMP, 5-аминоимидазол-4-карбоксамид рибонуклеозида (AICAR). 56,57 Эти исследования показали, что AICAR увеличивает транспорт глюкозы в скелетных мышцах, 56,57 и, подобно сокращению мышц, эффекты AICAR являются аддитивными с инсулином и независимыми от PI 3-киназы. 56,58 Некоторые исследования показали, что у мышей со сверхэкспрессией доминантно-негативной конструкции AMPK α2 в мышцах или у мышей α1 и α2 KO наблюдается нарушение стимулированного физической нагрузкой поглощения глюкозы. 24,59–63 Напротив, другие исследования, в которых использовались мышиные модели с удаленной активностью AMPK, демонстрируют, что ингибирование AMPK мало или не влияет на потребление глюкозы, вызванное физической нагрузкой, 62,64,65 или на потребление глюкозы, стимулированное физической нагрузкой in vivo , 66 , предполагая избыточность в системе.Таким образом, вопрос о том, необходим ли АМФК для стимулированного физической нагрузкой усвоения глюкозы, до сих пор остается спорным.
56,57 Эти исследования показали, что AICAR увеличивает транспорт глюкозы в скелетных мышцах, 56,57 и, подобно сокращению мышц, эффекты AICAR являются аддитивными с инсулином и независимыми от PI 3-киназы. 56,58 Некоторые исследования показали, что у мышей со сверхэкспрессией доминантно-негативной конструкции AMPK α2 в мышцах или у мышей α1 и α2 KO наблюдается нарушение стимулированного физической нагрузкой поглощения глюкозы. 24,59–63 Напротив, другие исследования, в которых использовались мышиные модели с удаленной активностью AMPK, демонстрируют, что ингибирование AMPK мало или не влияет на потребление глюкозы, вызванное физической нагрузкой, 62,64,65 или на потребление глюкозы, стимулированное физической нагрузкой in vivo , 66 , предполагая избыточность в системе.Таким образом, вопрос о том, необходим ли АМФК для стимулированного физической нагрузкой усвоения глюкозы, до сих пор остается спорным.
Роль LKB1 в транспорте глюкозы, стимулированном физической нагрузкой, также не ясна. Было показано, что у мышей с KO LKB1, особенно в скелетных мышцах, наблюдается серьезное притупление транспорта глюкозы, стимулированного сокращением. 51,67 Это снижение транспорта глюкозы может быть связано со снижением активации AMPK и одной или нескольких киназ, связанных с AMPK, которые являются субстратами LKB1.Одним из возможных субстратов LKB1, который может регулировать транспорт глюкозы, стимулируемый физической нагрузкой, является неферментирующая сахарозу AMPK-родственная киназа (SNARK). Было показано, что снижение активности SNARK в скелетных мышцах снижает транспорт глюкозы, стимулируемый физической нагрузкой. 68
В то время как было показано, что транспорт глюкозы, стимулированный сокращениями, нарушен у мышей LKB-1 KO 51,67 и со сниженной активностью SNARK, 68 другое недавнее исследование показало, что поглощение глюкозы во время бега на беговой дорожке было аналогичным, если не выше у мышей LKB-1 KO по сравнению с контролем дикого типа. 69 В еще одном исследовании мышечно-специфическая делеция LKB1 только частично ингибировала стимулируемый физической нагрузкой транспорт глюкозы. 51 Эти данные предполагают, что, хотя AMPK, SNARK и LKB1 могут играть важную роль в регуляции потребления глюкозы, стимулированного физической нагрузкой, эта система должна иметь высокую степень избыточности, и вполне вероятно, что существует несколько перекрывающихся сигнальных систем, которые могут контролировать транспорт глюкозы в скелетных мышцах, стимулируемый физической нагрузкой. Эта теория согласуется с важностью использования углеводов во время упражнений для выживания.
69 В еще одном исследовании мышечно-специфическая делеция LKB1 только частично ингибировала стимулируемый физической нагрузкой транспорт глюкозы. 51 Эти данные предполагают, что, хотя AMPK, SNARK и LKB1 могут играть важную роль в регуляции потребления глюкозы, стимулированного физической нагрузкой, эта система должна иметь высокую степень избыточности, и вполне вероятно, что существует несколько перекрывающихся сигнальных систем, которые могут контролировать транспорт глюкозы в скелетных мышцах, стимулируемый физической нагрузкой. Эта теория согласуется с важностью использования углеводов во время упражнений для выживания.
5.2 Ca
2+ / кальмодулин-зависимые протеинкиназы Сократительная активность скелетных мышц требует увеличения внутриклеточных концентраций Ca 2+ , а некоторые исследования показали, что Ca 2+ / передача сигналов кальмодулина и Ca 2 + / кальмодулин-зависимые протеинкиназы являются важными сигналами, опосредующими стимулируемый физической нагрузкой транспорт глюкозы в скелетных мышцах. Инкубация скелетных мышц крысы с ингибитором Ca 2+ / кальмодулина KN-93 снижала стимулируемый сокращением транспорт глюкозы. 70 KN-93 также ингибировал индуцированное физической нагрузкой фосфорилирование CaMKII в отсутствие ингибирования AMPK, предполагая, что CaMK регулируют транспорт глюкозы независимо от передачи сигналов AMPK. 70,71 Эти исследования также показали, что избыточная экспрессия конститутивно активного CaMKKα в скелетных мышцах мышей увеличивает фосфорилирование AMPK Thr-172 и поглощение глюкозы скелетными мышцами. 71 Электропорация специфического ингибитора CaMKII в переднюю большеберцовую мышцу мыши снижает потребление глюкозы, стимулированное физической нагрузкой, на 30%. 72 Однако отдельное исследование показало, что увеличение концентрации Ca 2+ в мышцах вызывает очень небольшое увеличение поглощения глюкозы при нарушении сократительной реакции мышцы. 73 Эти данные указывают на косвенный эффект Ca 2+ на усвоение глюкозы мышцами, и изучение передачи сигналов кальция в регуляции транспорта глюкозы, стимулированного физической нагрузкой, требует дальнейшего изучения.
73 Эти данные указывают на косвенный эффект Ca 2+ на усвоение глюкозы мышцами, и изучение передачи сигналов кальция в регуляции транспорта глюкозы, стимулированного физической нагрузкой, требует дальнейшего изучения.
5.3 Нижестоящие сигналы, опосредующие транспорт глюкозы, стимулируемый физической нагрузкой
Было высказано предположение, что сигнальные белки, расположенные ниже в сигнальных путях физической нагрузки и инсулина, сходятся на субстрате Akt белков Rab GAP с массой 160 кДа (AS160 / TBC1D4) и Tre-2 / USP6 , BUB2, член 1 семейства доменов cdc16 (TBC1D1).AS160 и TBC1D1 связаны с транслокацией GLUT4 через белки Rab (ras, гомологичные из мозга). Белки Rab являются членами суперсемейства Ras small GTPases 74 и, как было показано, участвуют во многих событиях мембранного переноса. Активные Rab привлекают различные эффекторные белки, которые участвуют в почковании, связывании и слиянии пузырьков. 49,74,75 В дополнение к хорошо установленным ролям белков Rab, есть доказательства, что GTPase Rac1 семейства Rho участвует в транслокации GLUT4, стимулированной как инсулином, так и физической нагрузкой. 76,77 У мышей, дефицитных по Rac1 (Rac1 KO), снижена стимулированная инсулином транслокация GLUT4, у 71,76 и ингибирование Rac1 снизилось стимулированное сокращением захвата глюкозы в скелетных мышцах мышей. 77
5.4 AS160 и TBC1D1
Первоначально было продемонстрировано, что AS160 регулирует инсулино-стимулированную транслокацию GLUT4 в адипоцитах 3T3LI. 78–80 AS160 имеет множество сайтов фосфорилирования, а активность Rab GAP контролируется фосфорилированием.Наиболее изученными сайтами фосфорилирования является группа из шести отдельных сайтов, которые были идентифицированы как субстраты для Akt. Их вместе называют сайтами фосфо-Akt-субстрата (PAS), и как инсулин, так и упражнения увеличивают фосфорилирование AS160 PAS в скелетных мышцах.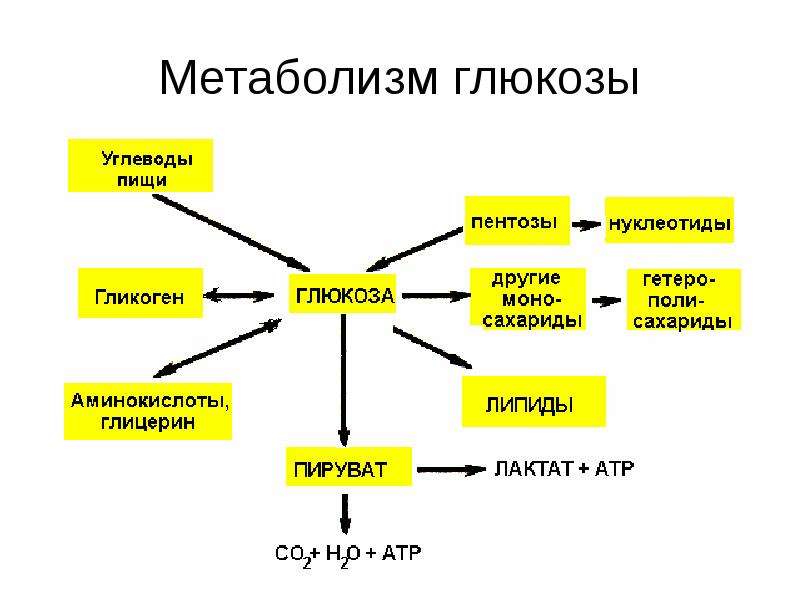 78,81,82 Длительные физические упражнения у людей 82–84 и крыс, 78 , а также AICAR также известны как вызывающие фосфорилирование AS160 PAS. Таким образом, в дополнение к Akt, AMPK фосфорилирует AS160. 81 Мутация четырех сайтов PAS значительно ингибирует поглощение глюкозы, индуцированное как инсулином, так и физической нагрузкой. 85 AS160 также содержит кальмодулин-связывающий домен, и мутация этого домена ингибирует потребление глюкозы, стимулируемое физической нагрузкой, но не инсулином. 86 Эти данные показывают, что как фосфорилирование, так и связывание кальмодулина на AS160 участвуют в регуляции стимулируемого физической нагрузкой поглощения глюкозы. Эти данные также предполагают, что, хотя AS160 может служить точкой конвергенции как инсулиновой, так и зависимой от физических упражнений передачи сигналов в регуляции поглощения глюкозы, другие белки могут участвовать в этой регуляции поглощения глюкозы.
78,81,82 Длительные физические упражнения у людей 82–84 и крыс, 78 , а также AICAR также известны как вызывающие фосфорилирование AS160 PAS. Таким образом, в дополнение к Akt, AMPK фосфорилирует AS160. 81 Мутация четырех сайтов PAS значительно ингибирует поглощение глюкозы, индуцированное как инсулином, так и физической нагрузкой. 85 AS160 также содержит кальмодулин-связывающий домен, и мутация этого домена ингибирует потребление глюкозы, стимулируемое физической нагрузкой, но не инсулином. 86 Эти данные показывают, что как фосфорилирование, так и связывание кальмодулина на AS160 участвуют в регуляции стимулируемого физической нагрузкой поглощения глюкозы. Эти данные также предполагают, что, хотя AS160 может служить точкой конвергенции как инсулиновой, так и зависимой от физических упражнений передачи сигналов в регуляции поглощения глюкозы, другие белки могут участвовать в этой регуляции поглощения глюкозы.
TBC1D1 является еще одним потенциальным молекулярным звеном между сигнальными путями, сходящимися с транслокацией GLUT4 в скелетных мышцах. 78,81,87–91 TBC1D1 и AS160 разделяют 47% общей идентичности и имеют несколько сопоставимых структурных особенностей. TBC1D1 был впервые идентифицирован в адипоцитах в культуре, но имеет очень ограниченную экспрессию в этой ткани. Напротив, TBC1D1 высоко экспрессируется в скелетных мышцах. 89 Инсулин увеличивает фосфорилирование TBC1D1 PAS в скелетных мышцах 90,92,93 , но, в отличие от AS160, TBC1D1 может регулировать стимулируемый инсулином транспорт глюкозы через PAS-независимый механизм. 92 Мутации TBC1D1 по-разному регулируют транспорт глюкозы в скелетных мышцах, стимулируемый инсулином и физической нагрузкой. 92,93 Таким образом, TBC1D1 регулирует транспорт глюкозы в мышцах как инсулином, так и стимулированным физической нагрузкой, но через различные сайты фосфорилирования. Взятые вместе, эти данные демонстрируют, что AS160 и TBC1D1 являются точкой конвергенции для регуляции транслокации GLUT4 для транспорта глюкозы, стимулированного инсулином и физической нагрузкой, в скелетных мышцах.
6.ПОВЫШЕНИЕ ЧУВСТВИТЕЛЬНОСТИ ИНСУЛИНА К ТРАНСПОРТУ ГЛЮКОЗЫ ПОСЛЕ УПРАЖНЕНИЯ
Влияние резких упражнений на транспорт глюкозы относительно недолговечно, возвращаясь к исходному уровню обычно через ~ 30-40 минут. Однако, как только исчезнут острые эффекты упражнений per se , наступит период, характеризующийся повышенной эффективностью инсулина для стимуляции транспорта глюкозы. 94,95 Это повышение послетренировочной чувствительности к инсулину наблюдалось у людей в течение 48 часов после тренировки. 96 Механизмы повышенной чувствительности к инсулину не известны. Хотя снижение концентрации гликогена в мышцах может играть роль в повышении чувствительности к инсулину, вызванном физической нагрузкой, усиление действия инсулина может происходить даже после полного восполнения запасов гликогена. 94 Сигнальные механизмы, опосредующие повышение чувствительности к инсулину после тренировки, также неизвестны, но, как и острые эффекты физических упражнений на транспорт глюкозы, не считаются следствием повышенной активности рецептора инсулина или IRS-1. 94,95,97 Однако у нас и других есть данные, предполагающие усиленное фосфорилирование тирозина IRS-2, 98,99 Akt фосфорилирование 44,100,101 и активность, 44 Субстрат Atk с фосфорилированием 160 кДа (AS160) , 100 и экспрессия цитоплазматического SHP2 101 в состоянии после тренировки.
7. ТРЕНИРОВКИ: ВЛИЯНИЕ НА ЗДОРОВЫХ ЛЮДЕЙ И ЛЮДЕЙ С ДИАБЕТОМ 2 ТИПА
Регулярная физическая активность приводит к многочисленным адаптациям в скелетных мышцах, которые позволяют мышцам более эффективно вырабатывать АТФ и становиться более устойчивыми к усталости. 102 Что касается метаболизма углеводов, некоторые из ключевых адаптаций, которые происходят в скелетных мышцах при тренировках, включают повышенное потребление глюкозы и повышенную экспрессию GLUT4. 103,104 Тренированные мышцы также характеризуются повышенной концентрацией гликогена, который является важным фактором снижения уровня утомляемости при длительных упражнениях. Тренировка с физической нагрузкой вызывает преобразование типа мышечных волокон в более окислительный и, возможно, медленный фенотип, 105–107 и повышение активности и содержания митохондрий. 108–110 Кроме того, физические упражнения могут повысить чувствительность к инсулину и улучшить общий гомеостаз глюкозы, 111–113 , что особенно важно для людей с метаболическими заболеваниями, такими как диабет 2 типа.
Диабет 2 типа возникает в результате сочетания генетической предрасположенности и факторов окружающей среды, включая отсутствие физической активности и плохое питание. 114 Таким образом, диабет 2 типа обычно развивается по мере того, как люди становятся более тучными и менее активными, что приводит к инсулинорезистентности, нарушению толерантности к глюкозе и, в конечном итоге, к началу полномасштабного диабета 2 типа.Хотя диабет 2 типа является многофакторным заболеванием, это заболевание измененного углеводного обмена на многих уровнях. У людей с диабетом 2 типа уровень инсулина нормальный или высокий, но такие ткани, как печень, скелетные мышцы и жировая ткань, становятся устойчивыми к инсулину. Поджелудочная железа компенсирует это путем производства большого количества инсулина, но этот стресс может в конечном итоге привести к недостаточности поджелудочной железы и необходимости лечения экзогенным инсулином. Гиперинсулинемическое состояние может привести к нарушению транспорта глюкозы в печень, скелетные мышцы и жировую ткань. 115 Хотя диабет 2 типа обычно возникает у взрослых, количество детей и подростков, страдающих этим заболеванием, резко увеличивается. Фактически, в настоящее время в Соединенных Штатах насчитывается 23,6 миллиона человек, что составляет примерно 8% населения, страдающего диабетом, и это число увеличилось вдвое за последние 15 лет и продолжает расти с темпами эпидемии. 116
Хотя эти статистические данные обескураживают, хорошая новость заключается в том, что регулярные физические упражнения могут отсрочить или предотвратить возникновение диабета 2 типа. 117–120 Исследования с использованием рандомизированных исследований показали, что меры по изменению образа жизни, которые включали ~ 150 минут физической активности в неделю в сочетании с потерей веса, вызванной диетой, снижали риск диабета 2 типа на 58% в группе риска. . 91,117 Физические упражнения, независимо от диеты, также показали свою эффективность для профилактики и прогрессирования диабета 2 типа. 118 Физические упражнения у людей с диабетом 2 типа могут улучшить концентрацию глюкозы в крови, массу тела, липиды, артериальное давление, сердечно-сосудистые заболевания, смертность и общее качество жизни. 121–127 Исследование Look AHEAD продемонстрировало, что сочетание потери веса и физической активности у людей с диабетом 2 типа вызывает умеренную потерю веса примерно на 6%, улучшение гликолизированного гемоглобина, улучшение подвижности и улучшение функции почек, но не улучшение сердечно-сосудистых заболеваний. за 10-летний период. 121,123,124,126 Однако, поскольку уровень физической подготовки оценивался только в течение 4-го года исследования, нельзя сделать выводы о влиянии уровня физической подготовки на сердечно-сосудистые заболевания. 121,123,124,126 Было показано, что увеличение физической активности у взрослых с диабетом 2 типа приводит к частичной или полной ремиссии диабета 2 типа у 11,5% субъектов в течение первого года вмешательства, а еще у 7% наблюдалась частичная или полная ремиссия этого типа. 2 сахарный диабет после 4 лет тренировок. 122 Взятые вместе, все эти данные показывают, что влияние физических упражнений на метаболизм углеводов оказывает глубокое влияние на метаболическое здоровье, и эти знания важны, поскольку мы работаем над борьбой с эпидемией диабета 2 типа.
Благодарности
Работа в лаборатории автора была поддержана грантами Национального института здравоохранения R01-AR42238, R01-DK101043, R01-DK099511 (L.J.G.) и 5P30 DK36836 (Центр диабета Джослина, ДРК). J.D.M. поддерживается стипендиатом Американской диабетической ассоциации (L.J.G.) на основе наставников. К.И.С. был поддержан грантом Американского колледжа спортивной медицины и стипендией Мэри К. Якокка в Диабетическом центре Джослин, а в настоящее время поддерживается Национальным институтом здоровья K01-DK105109.
СПИСОК СОКРАЩЕНИЙ
90sp405 фосфат Pi 90sp405 ras гомологичен из мозга| АДФ | аденозиндифосфат | ||
| AICAR | аминоимидазол-4-карбоксамид рибонуклеозид | ||
| кетофосфат | AMPhosphospdenoside | ||
| AMPhosphosphosphora | AS160 | Субстрат Akt 160 кДа | |
| АТФ | аденозинтрифосфат | ||
| CaMKII | Ca 2+ / кальмодулин-зависимый протеинкиназный трансортер II | GLP | |
| глюкоза типа GL | |||
| LKB1 | киназа печени B1 | ||
| MIRKO | Мыши с нокаутом по мышечно-специфическим рецепторам инсулина | ||
| PAS | фосфо-Akt Rab-субстрат | ||
| SNARK | сахароза неферментирующая AMPK-родственная киназа |
Ссылки
1.Брамбл Д.М., Либерман Д.Е. Бег на выносливость и эволюция Homo. Природа. 2004. 432: 345–352. [PubMed] [Google Scholar] 2. Чакраварти М.В., Бут FW. Еда, упражнения и «бережливые» генотипы: соединяющие точки на пути к эволюционному пониманию современных хронических заболеваний. J Appl Physiol. 2004; 96: 3–10. [PubMed] [Google Scholar] 3. Харгривз М. Метаболические системы; углеводный обмен. В: Фаррелл П.А., Джойнер MJ, Caizozzo VJ, редакторы. Продвинутая физиология упражнений. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2012 г.С. 3–391. [Google Scholar] 4. Spriet LL. Метаболические системы; липидный обмен. В: Фаррелл П.А., Джойнер MJ, Caizozzo VJ, редакторы. Продвинутая физиология упражнений. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2012. С. 392–407. [Google Scholar] 5. Сидозис Л.С., Стюарт К.А., Шульман Г.И., Лопасчук Г.Д., Вольф Р.Р. Глюкоза и инсулин регулируют окисление жиров, контролируя скорость поступления жирных кислот в митохондрии. J Clin Invest. 1996; 98: 2244–2250. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6.Wolfe RR. Метаболические взаимодействия между глюкозой и жирными кислотами у человека. Am J Clin Nutr. 1998; 67: 519S – 526S. [PubMed] [Google Scholar] 7. Acheson KJ, Schutz Y, Bessard T, Anantharaman K, Flatt JP, Jequier E. Емкость хранения гликогена и липогенез de novo во время массового перекармливания углеводов у человека. Am J Clin Nutr. 1988. 48: 240–247. [PubMed] [Google Scholar] 8. Maughan RJ. Спортивное питание. Справочник по спортивной медицине и науке. Лондон: Blackwell Science; 2002. [Google Scholar] 9. МакАрдл В, Катч ФКВ.Основы физиологии упражнений. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2000. [Google Scholar] 10. ван Баак М.А. Физическая активность и энергетический баланс. Public Health Nutr. 1999; 2: 335–339. [PubMed] [Google Scholar] 11. Romijn JA, Coyle EF, Sidossis LS и др. Регулирование эндогенного жирового и углеводного обмена в зависимости от интенсивности и продолжительности упражнений. Am J Physiol. 1993; 265: E380 – E391. [PubMed] [Google Scholar] 12. Graham TE. Гликоген: обзор возможных регуляторных ролей белков, связанных с гранулами.Appl Physiol Nutr Metab. 2009; 34: 488–492. [PubMed] [Google Scholar] 13. ван Лун Л.Дж., Гринхафф П.Л., Константин-Теодосиу Д., Сарис В.Х., Вагенмакерс А.Дж. Влияние увеличения интенсивности упражнений на использование мышечного топлива у людей. J Physiol. 2001; 536: 295–304. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Голлник П.Д., Пил К., Салтин Б. Характер избирательного истощения гликогена в мышечных волокнах человека после упражнений различной интенсивности и с разной скоростью вращения педалей. J Physiol. 1974. 241: 45–57. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15.Халтман Э., Харрис Р.С. Углеводный обмен. В: Poortmans JR, редактор. Принципы биохимии упражнений. Базель: Каргер; 1988. С. 78–119. [Google Scholar] 16. Рихтер Э.А., Рудерман Н.Б., Гаврас Х., Белур Э.Р., Гальбо Х. Гликогенолиз мышц во время упражнений: двойной контроль адреналином и сокращениями. Am J Physiol. 1982; 242: E25 – E32. [PubMed] [Google Scholar] 17. Watt MJ, Howlett KF, Febbraio MA, Spriet LL, Hargreaves M. Адреналин увеличивает гликогенолиз скелетных мышц, активацию пируватдегидрогеназы и окисление углеводов во время умеренных физических нагрузок у людей.J Physiol. 2001; 534: 269–278. [Бесплатная статья PMC] [PubMed] [Google Scholar] 18. Хоулетт Р.А., Паролин М.Л., Дайк Д.Д. и др. Регулирование гликогенфосфорилазы и ПДГ в скелетных мышцах при различной выходной мощности. Am J Physiol. 1998; 275: R418 – R425. [PubMed] [Google Scholar] 19. Берк Л. М., Ангус Д. Д., Кокс Г. Р. и др. Влияние жировой адаптации и восстановления углеводов на метаболизм и производительность при длительной езде на велосипеде. J Appl Physiol. 2000. 89: 2413–2421. [PubMed] [Google Scholar] 20. Бергстром Дж., Хермансен Л., Халтман Э., Салтин Б.Диета, мышечный гликоген и физическая работоспособность. Acta Physiol Scand. 1967; 71: 140–150. [PubMed] [Google Scholar] 21. Бергстром Дж., Халтман Э. Синтез мышечного гликогена после упражнений: усиливающий фактор, локализованный в мышечных клетках человека. Природа. 1966; 210: 309–310. [PubMed] [Google Scholar] 22. Чесли A, Heigenhauser GJ, Spriet LL. Регулирование активности гликогенфосфорилазы в мышцах после краткосрочных тренировок на выносливость. Am J Physiol. 1996; 270: E328 – E335. [PubMed] [Google Scholar] 23. Кубо К., Фоли Дж. Э.Ограничивающие скорость шаги для инсулино-опосредованного поглощения глюкозы перфузируемой задней конечностью крысы. Am J Physiol. 1986; 250: E100 – E102. [PubMed] [Google Scholar] 24. Нешер Р., Карл И.Е., Кипнис Д.М. Диссоциация эффектов инсулина и сокращения на транспорт глюкозы в эпитрохлеарной мышце крысы. Am J Physiol. 1985; 249: C226 – C232. [PubMed] [Google Scholar] 25. Белл Г.И., Бурант К.Ф., Такеда Дж., Гулд Г.В. Структура и функция облегчающих переносчиков сахара у млекопитающих. J Biol Chem. 1993; 268: 19161–19164. [PubMed] [Google Scholar] 26.Каяно Т., Бурант С.Ф., Фукумото Х. и др. Человеческие переносчики глюкозы. Выделение, функциональная характеристика и локализация генов кДНК, кодирующих изоформу (GLUT5), экспрессируемую в тонкой кишке, почках, мышцах и жировой ткани, а также необычную псевдогеноподобную последовательность переносчика глюкозы (GLUT6) J Biol Chem. 1990; 265: 13276–13282. [PubMed] [Google Scholar] 27. Клип А., Паке МР. Транспорт глюкозы и переносчики глюкозы в мышцах и их метаболическая регуляция. Уход за диабетом. 1990; 13: 228–243.[PubMed] [Google Scholar] 28. Роджерс С., Македа М.Л., Дочерти С.Е. и др. Идентификация нового белка, подобного переносчику глюкозы, — GLUT-12. Am J Physiol Endocrinol Metab. 2002; 282: E733 – E738. [PubMed] [Google Scholar] 29. Кац Е.Б., Стенбит А.Е., Хаттон К., ДеПиньо Р., Чаррон М.Дж. Нарушения сердечной и жировой ткани, но не диабет у мышей с дефицитом GLUT4. Природа. 1995; 377: 151–155. [PubMed] [Google Scholar] 30. Зисман А., Перони О.Д., Абель Э.Д. и др. Целенаправленное нарушение транспортера глюкозы 4 избирательно в мышцах вызывает инсулинорезистентность и непереносимость глюкозы.Nat Med. 2000; 6: 924–928. [PubMed] [Google Scholar] 31. Хиршман М.Ф., Валлберг-Хенрикссон Х., Вардзала Л.Дж., Хортон Э.Д., Хортон Э.С. Острая физическая нагрузка увеличивает количество переносчиков глюкозы плазматической мембраны в скелетных мышцах крысы. FEBS Lett. 1988. 238: 235–239. [PubMed] [Google Scholar] 32. Хиршман MF, Goodyear LJ, Wardzala LJ, Horton ED, Horton ES. Идентификация внутриклеточного пула переносчиков глюкозы из базальных и инсулино-стимулированных скелетных мышц крыс. J Biol Chem. 1990; 265: 987–991. [PubMed] [Google Scholar] 33.Lauritzen HP, Galbo H, Brandauer J, Goodyear LJ, Ploug T. Большие везикулы GLUT4 неподвижны, в то время как локально и обратимо истощаются во время временной инсулиновой стимуляции скелетных мышц живых мышей: визуальный анализ динамики везикул зеленого флуоресцентного белка, усиленного GLUT4. Сахарный диабет. 2008. 57: 315–324. [PubMed] [Google Scholar] 34. Лауритцен Х.П., Гальбо Х, Тойода Т, Гудиер Л.Дж. Кинетика транслокации GLUT4, вызванной сокращением, в волокнах скелетных мышц живых мышей. Сахарный диабет. 2010; 59: 2134–2144.[Бесплатная статья PMC] [PubMed] [Google Scholar] 35. Лето Д., Сальтиель А.Р. Регулирование транспорта глюкозы инсулином: контроль движения GLUT4. Nat Rev Mol Cell Biol. 2012; 13: 383–396. [PubMed] [Google Scholar] 36. Ян С., Кокер К.Дж., Ким Дж.К. и др. У мышей с гетерозиготным нокаутом по синтаксину 4 развивается мышечная инсулинорезистентность. J Clin Invest. 2001; 107: 1311–1318. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Кристиансен С, Харгривз М, Рихтер Э.А. Вызванное упражнениями увеличение транспорта глюкозы, GLUT-4 и VAMP-2 в плазматической мембране из мышц человека.Am J Physiol. 1996; 270: E197 – E201. [PubMed] [Google Scholar] 38. Валлберг-Хенрикссон H, констебль SH, молодой Д.А., Holloszy JO. Транспорт глюкозы в скелетные мышцы крысы: взаимодействие между упражнениями и инсулином. J Appl Physiol. 1988; 65: 909–913. [PubMed] [Google Scholar] 39. Хаяши Т., Войташевский Дж. Ф., Goodyear LJ. Регулирование транспорта глюкозы в скелетных мышцах с помощью физических упражнений. Am J Physiol. 1997; 273: E1039 – E1051. [PubMed] [Google Scholar] 40. Фолли Ф., Саад М.Дж., Бэкер Дж. М., Кан Ч.Р. Стимуляция инсулином активности фосфатидилинозитол-3-киназы и ассоциация с субстратом 1 рецептора инсулина в печени и мышцах интактной крысы.J Biol Chem. 1992; 267: 22171–22177. [PubMed] [Google Scholar] 41. Goodyear LJ, Giorgino F, Balon TW, Condorelli G, Smith RJ. Влияние сократительной активности на тирозинфосфопротеины и активность PI 3-киназы в скелетных мышцах крыс. Am J Physiol. 1995; 268: E987 – E995. [PubMed] [Google Scholar] 42. Greengard P, Valtorta F, Czernik AJ, Benfenati F. Фосфопротеины синаптических пузырьков и регуляция синаптической функции. Наука. 1993; 259: 780–785. [PubMed] [Google Scholar] 43. Тредвей Дж. Л., Джеймс Д. Э., Бурсель Е, Рудерман Н. Б..Влияние упражнений на связывание инсулиновых рецепторов и активность киназы в скелетных мышцах. Am J Physiol. 1989; 256: E138 – E144. [PubMed] [Google Scholar] 44. Войташевский Дж. Ф., Хигаки Ю., Хиршман М. Ф. и др. Физические упражнения модулируют пострецепторную передачу сигналов инсулина и транспорт глюкозы у мышей с нокаутом мышечно-специфических рецепторов инсулина. J Clin Invest. 1999; 104: 1257–1264. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45. Брунинг Дж. К., Майкл М. Д., Винней Дж. Н. и др. Нокаут мышечного рецептора инсулина проявляет признаки метаболического синдрома NIDDM без изменения толерантности к глюкозе.Mol Cell. 1998. 2: 559–569. [PubMed] [Google Scholar] 46. Джессен Н., Goodyear LJ. Сигналы сокращения для транспорта глюкозы в скелетных мышцах. J Appl Physiol. 2005. 99: 330–337. [PubMed] [Google Scholar] 47. Kramer HF, Goodyear LJ. Упражнение, передача сигналов MAPK и NF-kappaB в скелетных мышцах. J Appl Physiol. 2007. 103: 388–395. [PubMed] [Google Scholar] 48. Lessard SJ, Rivas DA, Alves-Wagner AB и др. Сопротивление аэробным упражнениям вызывает метаболическую дисфункцию и открывает новые сигнальные сети, регулируемые упражнениями.Сахарный диабет. 2013; 62: 2717–2727. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Richter EA, Hargreaves M. Упражнения, GLUT4 и поглощение глюкозы в скелетных мышцах. Physiol Rev.2013; 93: 933–1017. [PubMed] [Google Scholar] 50. Rockl KS, Witczak CA, Goodyear LJ. Сигнальные механизмы в скелетных мышцах: острые реакции и хроническая адаптация к упражнениям. IUBMB Life. 2008. 60: 145–153. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Koh HJ, Arnolds DE, Fujii N, et al. Избирательный нокаут LKB1 в скелетных мышцах увеличивает чувствительность к инсулину, улучшает гомеостаз глюкозы и снижает TRB3.Mol Cell Biol. 2006; 26: 8217–8227. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Харди Д.Г. Чувствительность к энергии активированной АМФ протеинкиназой и ее влияние на метаболизм мышц. Proc Nutr Soc. 2011; 70: 92–99. [PubMed] [Google Scholar] 53. Харди Д.Г., Карлинг Д., Карлсон М. Подсемейство AMP-активированных / SNF1 протеинкиназ: метаболические сенсоры эукариотической клетки? Анну Рев Биохим. 1998. 67: 821–855. [PubMed] [Google Scholar] 54. Кемп Б.Е., Митчелхилл К.И., Стэплтон Д., Мичелл Б.Дж., Чен З.П., Виттерс Л.А. Работа с потребностями в энергии: протеинкиназа, активируемая АМФ.Trends Biochem Sci. 1999; 24: 22–25. [PubMed] [Google Scholar] 55. Харди Д.Г. AMPK: положительная и отрицательная регуляция и ее роль в энергетическом гомеостазе всего тела. Curr Opin Cell Biol. 2014; 33С: 1–7. [PubMed] [Google Scholar] 56. Хаяши Т., Хиршман М.Ф., Курт Э.Дж., Виндер В.В., Goodyear LJ. Доказательства опосредования 5′-АМФ-активируемой протеинкиназой эффекта сокращения мышц на транспорт глюкозы. Сахарный диабет. 1998. 47: 1369–1373. [PubMed] [Google Scholar] 57. Winder WW, Holmes BF, Rubink DS, Jensen EB, Chen M, Holloszy JO.Активация АМФ-активированной протеинкиназы увеличивает количество митохондриальных ферментов в скелетных мышцах. J Appl Physiol. 2000; 88: 2219–2226. [PubMed] [Google Scholar] 58. Merrill GF, Kurth EJ, Hardie DG, Winder WW. Рибозид AICA увеличивает АМФ-активированную протеинкиназу, окисление жирных кислот и поглощение глюкозы мышцами крысы. Am J Physiol. 1997; 273: E1107 – E1112. [PubMed] [Google Scholar] 59. Эбботт М.Дж., Богачус Л.Д., Тюркотт Л.П. Дефицит AMPKalpha2 обнаруживает зависимость от времени в регуляции индуцированного сокращением захвата пальмитата и глюкозы мышцами мышей.J Appl Physiol. 2011; 111: 125–134. [PubMed] [Google Scholar] 60. Дженсен Т.Э., Роуз А.Дж., Йоргенсен С.Б. и др. Возможная CaMKK-зависимая регуляция фосфорилирования AMPK и поглощения глюкозы в начале умеренного тетанического сокращения скелетных мышц. Am J Physiol Endocrinol Metab. 2007; 292: E1308 – E1317. [PubMed] [Google Scholar] 61. Jensen TE, Schjerling P, Viollet B, Wojtaszewski JF, Richter EA. Активация AMPK alpha1 необходима для стимуляции захвата глюкозы в скелетных мышцах мышей за счет сокращения сокращений, но не за счет h3O2.PLoS One. 2008; 3: e2102. [Бесплатная статья PMC] [PubMed] [Google Scholar] 62. Йоргенсен С.Б., Виоллет Б., Андреелли Ф. и др. Нокаут изоформы протеинкиназы, активируемой альфа2, но не альфа1, 5′-АМФ, устраняет 5-аминоимидазол-4-карбоксамид-1-бета-4-рибофуранозид, но не вызывает захвата глюкозы в скелетных мышцах, вызванного сокращением. J Biol Chem. 2004. 279: 1070–1079. [PubMed] [Google Scholar] 63. Лефорт Н., Сент-Аманд Е., Морасс С., Кот СН, Маретт А. Альфа-субъединица AMPK важна для транспорта глюкозы, опосредованного субмаксимальным сокращением, в скелетных мышцах in vitro.Am J Physiol Endocrinol Metab. 2008; 295: E1447 – E1454. [PubMed] [Google Scholar] 64. Fujii N, Hirshman MF, Kane EM, et al. Активность АМФ-активированной протеинкиназы альфа2 не является существенной для транспорта глюкозы в скелетных мышцах, вызванного сокращением и гиперосмолярностью. J Biol Chem. 2005; 280: 39033–39041. [PubMed] [Google Scholar] 65. Му Дж, Брозиник Дж. Т., младший, Валладарес О., Букан М., Бирнбаум М. Дж.. Роль АМФ-активированной протеинкиназы в регулируемом сокращением и гипоксией транспорте глюкозы в скелетных мышцах.Mol Cell. 2001; 7: 1085–1094. [PubMed] [Google Scholar] 66. Маарбьерг С.Дж., Йоргенсен С.Б., Роуз А.Дж. и др. Генетическое нарушение передачи сигналов AMPKalpha2 не снижает усвоение глюкозы мышцами во время упражнений на беговой дорожке у мышей. Am J Physiol Endocrinol Metab. 2009; 297: E924 – E934. [PubMed] [Google Scholar] 67. Сакамото К., Маккарти А., Смит Д. и др. Дефицит LKB1 в скелетных мышцах предотвращает активацию AMPK и поглощение глюкозы во время сокращения. EMBO J. 2005; 24: 1810–1820. [Бесплатная статья PMC] [PubMed] [Google Scholar] 68.Ко Х. Дж., Тойода Т., Фуджи Н. и др. Неферментирующая сахарозу AMPK-родственная киназа (SNARK) опосредует стимулируемый сокращением транспорт глюкозы в скелетных мышцах мышей. Proc Natl Acad Sci U S. A. 2010; 107: 15541–15546. [Бесплатная статья PMC] [PubMed] [Google Scholar] 69. Джеппесен Дж., Маарбьерг С.Дж., Джорди А.Б. и др. LKB1 регулирует окисление липидов во время упражнений независимо от AMPK. Сахарный диабет. 2013; 62: 1490–1499. [Бесплатная статья PMC] [PubMed] [Google Scholar] 70. Райт, округ Колумбия, Хакер К.А., Холлоши Д.О., Хан Д.Х. И Ca2 +, и AMPK опосредуют стимуляцию транспорта глюкозы за счет мышечных сокращений.Сахарный диабет. 2004. 53: 330–335. [PubMed] [Google Scholar] 71. Витчак CA, Fujii N, Hirshman MF, Goodyear LJ. Са2 + / кальмодулин-зависимая протеинкиназа-киназа-альфа регулирует поглощение глюкозы скелетными мышцами независимо от AMP-активируемой протеинкиназы и активации Akt. Сахарный диабет. 2007; 56: 1403–1409. [PubMed] [Google Scholar] 72. Witczak CA, Jessen N, Warro DM, et al. CaMKII регулирует поглощение глюкозы, вызванное сокращением, но не инсулином, скелетными мышцами мышей. Am J Physiol Endocrinol Metab. 2010; 298: E1150 – E1160.[Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Дженсен Т.Э., Силов Л., Роуз А.Дж. и др. Стимулируемый сокращением транспорт глюкозы в мышцах контролируется AMPK и механическим стрессом, но не высвобождением Ca (2 +) саркоплазматического ретикулума. Mol Metab. 2014; 3: 742–753. [Бесплатная статья PMC] [PubMed] [Google Scholar] 74. Веннерберг К., Россман К.Л., Der CJ. Краткое описание суперсемейства Ras. J Cell Sci. 2005; 118: 843–846. [PubMed] [Google Scholar] 75. Kaddai V, Marchand-Brustel Y, Cormont M. Rab белки в эндоцитозе и трафике Glut4.Acta Physiol (Oxf) 2008; 192: 75–88. [PubMed] [Google Scholar] 76. Силов Л., Йенсен Т.Э., Кляйнерт М. и др. Передача сигналов Rac1 необходима для стимулированного инсулином захвата глюкозы и нарушена в скелетных мышцах инсулинорезистентных мышей и человека. Сахарный диабет. 2013; 62: 1865–1875. [Бесплатная статья PMC] [PubMed] [Google Scholar] 77. Силов Л., Йенсен Т.Э., Кляйнерт М. и др. Rac1 — новый регулятор захвата глюкозы скелетными мышцами, стимулированного сокращением. Сахарный диабет. 2013; 62: 1139–1151. [Бесплатная статья PMC] [PubMed] [Google Scholar] 78.Bruss MD, Arias EB, Lienhard GE, Cartee GD. Повышенное фосфорилирование Akt-субстрата 160 кДа (AS160) в скелетных мышцах крысы в ответ на инсулин или сократительную активность. Сахарный диабет. 2005; 54: 41–50. [PubMed] [Google Scholar] 79. Сано Х., Кейн С., Сано Э. и др. Стимулируемое инсулином фосфорилирование белка, активирующего ГТФазу Rab, регулирует транслокацию GLUT4. J Biol Chem. 2003. 278: 14599–14602. [PubMed] [Google Scholar] 80. Thong FS, Dugani CB, Klip A. Включение и выключение сигналов: трафик GLUT4 по инсулино-сигнальной магистрали.Физиология. 2005. 20: 271–284. [PubMed] [Google Scholar] 81. Kramer HF, Witczak CA, Fujii N, et al. Отчетливые сигналы регулируют фосфорилирование AS160 в ответ на инсулин, AICAR и сокращение скелетных мышц мышей. Сахарный диабет. 2006; 55: 2067–2076. [PubMed] [Google Scholar] 82. Treebak JT, Birk JB, Rose AJ, Kiens B, Richter EA, Wojtaszewski JF. Фосфорилирование AS160 связано с активацией тримерного комплекса альфа2бета2gamma1-, но не альфа2бета2gamma3-AMPK в скелетных мышцах во время физических упражнений у людей.Am J Physiol Endocrinol Metab. 2007; 292: E715 – E722. [PubMed] [Google Scholar] 83. Дешмук А., Коффи В.Г., Чжун З., Чибалин А.В., Хоули Дж. А., Зиерат-младший. Вызванное физической нагрузкой фосфорилирование новых субстратов Akt AS160 и филамина А в скелетных мышцах человека. Сахарный диабет. 2006; 55: 1776–1782. [PubMed] [Google Scholar] 84. Sriwijitkamol A, Coletta DK, Wajcberg E, et al. Влияние острых упражнений на передачу сигналов AMPK в скелетных мышцах субъектов с диабетом 2 типа: исследование зависимости от времени и дозы. Сахарный диабет.2007; 56: 836–848. [Бесплатная статья PMC] [PubMed] [Google Scholar] 85. Крамер Х. Ф., Витчак К. А., Тейлор Э. Б., Фуджи Н., Хиршман М. Ф., Goodyear LJ. AS160 регулирует поглощение глюкозы, вызванное инсулином и сокращением, скелетными мышцами мышей. J Biol Chem. 2006; 281: 31478–31485. [PubMed] [Google Scholar] 86. Kramer HF, Taylor EB, Witczak CA, Fujii N, Hirshman MF, Goodyear LJ. Кальмодулин-связывающий домен AS160 регулирует поглощение глюкозы скелетными мышцами, но не стимулируемое инсулином. Сахарный диабет. 2007. 56: 2854–2862.[PubMed] [Google Scholar] 87. Кейн С., Сано Х., Лю С.К. и др. Метод идентификации субстратов серинкиназы. Akt фосфорилирует новый белок адипоцитов с доменом белка, активирующего ГТФазу Rab (GAP). J Biol Chem. 2002; 277: 22115–22118. [PubMed] [Google Scholar] 88. Karlsson HK, Zierath JR, Kane S, Krook A, Lienhard GE, Wallberg-Henriksson H. Инсулино-стимулированное фосфорилирование субстрата Akt AS160 нарушается в скелетных мышцах у пациентов с диабетом 2 типа. Сахарный диабет. 2005; 54: 1692–1697. [PubMed] [Google Scholar] 89.Роуч РГ, Чавес Дж. А., Миинеа С. П., Линхард Дж. Э.. Субстратная специфичность и влияние GLUT4 на транслокацию Rab GTPase-активирующего белка Tbc1d1. Биохим Дж. 2007; 403: 353–358. [Бесплатная статья PMC] [PubMed] [Google Scholar] 90. Тейлор Э.Б., Ан Д., Крамер Х.Ф. и др. Открытие TBC1D1 как инсулино-, AICAR- и стимулируемого сокращением сигнального звена в скелетных мышцах мышей. J Biol Chem. 2008; 283: 9787–9796. [Бесплатная статья PMC] [PubMed] [Google Scholar] 91. Treebak JT, Glund S, Deshmukh A, et al. AMPK-опосредованное фосфорилирование AS160 в скелетных мышцах зависит от каталитических и регуляторных субъединиц AMPK.Сахарный диабет. 2006; 55: 2051–2058. [PubMed] [Google Scholar] 92. А. Д., Тойода Т., Тейлор Э. Б. и др. TBC1D1 регулирует транспорт глюкозы, индуцированный инсулином и сокращением, в скелетных мышцах мышей. Сахарный диабет. 2010. 59: 1358–1365. [Бесплатная статья PMC] [PubMed] [Google Scholar] 93. Вичайвонг К., Пурохит С., Ан Д. и др. Сокращение регулирует сайт-специфическое фосфорилирование TBC1D1 в скелетных мышцах. Биохим Дж. 2010; 431: 311–320. [Бесплатная статья PMC] [PubMed] [Google Scholar] 94. Cartee GD, Young DA, Sleeper MD, Zierath J, Wallberg-Henriksson H, Holloszy JO.Длительное увеличение инсулино-стимулированного транспорта глюкозы в мышцах после тренировки. Am J Physiol. 1989; 256: E494 – E499. [PubMed] [Google Scholar] 95. Войташевский Дж. Ф., Хансен Б. Ф., Кинс Б., Рихтер Э. А.. Передача сигналов инсулина в скелетных мышцах человека: динамика и эффект упражнений. Сахарный диабет. 1997. 46 (11): 1775–1781. [PubMed] [Google Scholar] 96. Mikines KJ, Sonne B, Farrell PA, Tronier B, Galbo H. Влияние физических упражнений на чувствительность и реакцию на инсулин у людей. Am J Physiol. 1988; 254: E248 – E259.[PubMed] [Google Scholar] 97. Войташевский Дж. Ф., Хансен Б. Ф., Гаде Дж. И др. Передача сигналов инсулина и чувствительность к инсулину после тренировки в скелетных мышцах человека. Сахарный диабет. 2000. 49: 325–331. [PubMed] [Google Scholar] 98. Хоулетт К.Ф., Сакамото К., Хиршман М.Ф. и др. Передача сигналов инсулина после тренировки у мышей с дефицитом субстрата-2 инсулинового рецептора. Сахарный диабет. 2002. 51: 479–483. [PubMed] [Google Scholar] 99. Хоулетт К.Ф., Сакамото К., Ю Х., Гудиер Л.Дж., Харгривз М. Инсулино-стимулированный инсулиновый рецептор, связанный с субстратом-2, фосфатидилинозитол-3-киназной активностью в скелетных мышцах человека после тренировки.Обмен веществ. 2006. 55 (8): 1046–1052. [PubMed] [Google Scholar] 100. Ариас Е.Б., Ким Дж., Фунаи К., Карти Г.Д. Предшествующие упражнения увеличивают фосфорилирование субстрата Akt на 160 кДа (AS160) в скелетных мышцах крыс. Am J Physiol Endocrinol Metab. 2007; 292 (4): E1191 – E1200. [PubMed] [Google Scholar] 101. Wadley GD, Konstantopoulos N, Macaulay L, et al. Повышенное содержание стимулированного инсулином Akt pSer473 и цитозольного белка SHP2 в скелетных мышцах человека после интенсивных физических нагрузок и краткосрочных тренировок. J Appl Physiol.2007. 102 (4): 1624–1631. [PubMed] [Google Scholar] 102. Тонконоги М., Сахлин К. Физические упражнения и функция митохондрий в скелетных мышцах человека. Exerc Sport Sci Rev. 2002; 30 (3): 129–137. [PubMed] [Google Scholar] 103. Джеймс Д.Э., Креген Э.В., Чизхолм DJ. Влияние физических упражнений на действие инсулина in vivo в отдельных тканях крысы. J Clin Invest. 1985. 76: 657–666. [Бесплатная статья PMC] [PubMed] [Google Scholar] 104. Goodyear LJ, Hirshman MF, Valyou PM, Horton ES. Число переносчиков глюкозы, функция и субклеточное распределение в скелетных мышцах крыс после тренировки.Сахарный диабет. 1992; 41: 1091–1099. [PubMed] [Google Scholar] 105. Андерсен П., Хенрикссон Дж. Тренировки вызвали изменения в подгруппах волокон скелетных мышц человека II типа. Acta Physiol Scand. 1977; 99 (1): 123–125. [PubMed] [Google Scholar] 106. Фитинги RH. Влияние регулярных тренировок на сократительную функцию скелетных мышц. Am J Phys Med Rehabil. 2003. 82 (4): 320–331. [PubMed] [Google Scholar] 107. Röckl KS, Hirshman MF, Brandauer J, Fujii N, Witters LA, Goodyear LJ. Адаптация скелетных мышц к тренировкам: активированная АМФ протеинкиназа опосредует сдвиг типа мышечных волокон.Сахарный диабет. 2007. 56 (8): 2062–2069. [PubMed] [Google Scholar] 108. Holloszy JO. Биохимические адаптации в мышцах: влияние упражнений на поглощение кислорода митохондриями и дыхательную активность в скелетных мышцах. J Biol Chem. 1967; 242: 2278–2282. [PubMed] [Google Scholar] 109. Голлник П.Д., Армстронг Р.Б., Салтин Б., Сауберт С.В., Сембрович В.Л., Шеперд Р.Э. Влияние тренировки на активность ферментов и состав волокон скелетных мышц человека. J Appl Physiol. 1973; 34 (1): 107–111. [PubMed] [Google Scholar] 110. Холлоши Дж.О., Бут FW.Биохимическая адаптация к упражнениям на выносливость в мышцах. Annu Rev Plant Physiol Plant Mol Biol. 1976; 38: 273–291. [PubMed] [Google Scholar] 111. Бьорнторп П., Фален М., Гримби Г. и др. Углеводный и липидный обмен у физически хорошо тренированных мужчин среднего возраста. Обмен веществ. 1972; 21: 1037–1044. [PubMed] [Google Scholar] 112. Рудерман Н.Б., Ганда О.П., Йохансен К. Влияние физических тренировок на толерантность к глюкозе и липиды плазмы при диабете в зрелом возрасте. Сахарный диабет. 1979; 28: 89–92. [PubMed] [Google Scholar] 113.Ostergard T, Andersen JL, Nyholm B и др. Влияние физических упражнений на чувствительность к инсулину, физическую форму и окислительную способность мышц у родственников первой степени родства пациентов с диабетом 2 типа. Am J Physiol Endocrinol Metab. 2006; 290 (5): E998 – E1005. [PubMed] [Google Scholar] 114. Ху Ф. Б., Мэнсон Дж. Э., Штампфер М. Дж. И др. Диета, образ жизни и риск сахарного диабета 2 типа у женщин. N Engl J Med. 2001; 345: 790–797. [PubMed] [Google Scholar] 115. ДеФронцо Р.А., Трипати Д. Инсулинорезистентность скелетных мышц является основным дефектом при диабете 2 типа.Уход за диабетом. 2009; 32 (Приложение 2): S157 – S163. [Бесплатная статья PMC] [PubMed] [Google Scholar] 116. Национальная целевая группа по профилактике и лечению ожирения. Избыточный вес, ожирение и риск для здоровья. Arch Intern Med. 2000; 160: 898–904. [PubMed] [Google Scholar] 117. Pan XR, Li GW, Hu YH и др. Влияние диеты и упражнений на профилактику NIDDM у людей с нарушенной толерантностью к глюкозе. Да Цин IGT и исследование диабета. Уход за диабетом. 1997. 20 (4): 537–544. [PubMed] [Google Scholar] 118. Кольберг С.Р., Сигал Р.Дж., Фернхолл Б. и др.Упражнения и диабет 2 типа: Американский колледж спортивной медицины и Американская диабетическая ассоциация: краткое изложение совместной позиции. Уход за диабетом. 2010. 33: 2692–2696. [Бесплатная статья PMC] [PubMed] [Google Scholar] 119. Койл Э. Ф., Когган А. Р., Хеммерт М. К., Айви Дж. Л. Использование гликогена в мышцах во время длительных физических упражнений с углеводной пищей. J Appl Physiol. 1986; 61: 165–172. [PubMed] [Google Scholar] 120. Кинни Дж. М., Такер Х. Н.. Энергетический обмен. Тканевые детерминанты и клеточные следствия.Нью-Йорк, Нью-Йорк: Raven Press; 1992. [Google Scholar] 121. Эспеланд М.А., Глик Н.А., Бертони А. и др. Влияние интенсивного вмешательства в образ жизни на использование и стоимость медицинских услуг среди взрослых с избыточным весом и ожирением, страдающих диабетом 2 типа: действие для здоровья при диабете. Уход за диабетом. 2014. 37 (9): 2548–2556. [Бесплатная статья PMC] [PubMed] [Google Scholar] 122. Грегг Э.В., Чен Х., Вагенкнехт Л.Е. и др. Связь интенсивного вмешательства в образ жизни с ремиссией диабета 2 типа. ДЖАМА. 2012. 308 (23): 2489–2496.[Бесплатная статья PMC] [PubMed] [Google Scholar] 123. Посмотрите AHEAD Research Group. Влияние долгосрочного поведенческого вмешательства по снижению веса на нефропатию у взрослых с избыточным весом или ожирением и диабетом 2 типа: вторичный анализ рандомизированного клинического исследования Look AHEAD. Ланцет Диабет Эндокринол. 2014; 2 (10): 801–809. [Бесплатная статья PMC] [PubMed] [Google Scholar] 124. Крыло Р.Р., Болин П., Бранкати Флорида и др. Сердечно-сосудистые эффекты интенсивного изменения образа жизни при диабете 2 типа. N Engl J Med. 2013. 369 (2): 145–154.[Бесплатная статья PMC] [PubMed] [Google Scholar] 125. Келли Д.Е., Хе Дж., Меньшикова Е.В., Ритов В.Б. Дисфункция митохондрий скелетных мышц человека при диабете 2 типа. Сахарный диабет. 2002. 51 (10): 2944–2950. [PubMed] [Google Scholar] 126. Rejeski WJ, Bray GA, Chen SH и др. Старение и физическая активность при диабете 2 типа: 8 лет интенсивного изменения образа жизни. J Gerontol A Biol Sci Med Sci. 2015; 70 (3): 343–351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 127. Крыло Р.Р., Ланг В., Вадден Т.А. и др. Преимущества умеренной потери веса в снижении факторов риска сердечно-сосудистых заболеваний у людей с избыточным весом и ожирением с диабетом 2 типа.Уход за диабетом. 2011. 34 (7): 1481–1486. [Бесплатная статья PMC] [PubMed] [Google Scholar] Метаболизмуглеводов во время упражнений | Как мышцы используют гликоген.
Узнайте, как мышцы используют гликоген, как они забирают глюкозу из кровотока, как она расщепляется посредством гликолиза до пирувата, сжигается в цикле Кребса или превращается в лактат.
Физиология упражнений | Сокращение мышц | Мышечные волокна | Мышечная адаптация | Топливо для упражнений | СНО Метаболизм | Жировой обмен | Поглощение кислорода | Сердечно-сосудистые упражнения | Респираторные реакции | VO2 Max | Регулирование температуры | Тепло | Баланс жидкости | Усталость | Спринт | Выносливость | Гены | Практический пример
Метаболизм СНО во время упражнений
Узнайте об углеводном обмене во время упражнений.Лекция начинается с изучения процесса, с помощью которого гликоген и глюкоза поступают из мышц и кровотока, как гликоген и глюкоза расщепляются посредством гликолиза до пирувата, как пируват затем окисляется в цикле Кребса или превращается в лактат. Узнайте, как мышечный гликоген используется во время тренировки, в зависимости от интенсивности тренировок. Лекция будет охватывать поглощение, регулирование, выработку глюкозы, окисление и метаболизм лактата.
Следующая тема — метаболизм углеводов во время упражнений, в основном более продолжительные субмаксимальные упражнения, и мы собираемся сосредоточиться на том, как мышца использует мышечный гликоген и как он поглощает и использует глюкозу из кровотока.Если вы помните из этого обзора энергетического метаболизма в скелетных мышцах, мы собираемся сосредоточиться на гликогене и глюкозе как внутри мышцы, так и за ее пределами, как он расщепляется в результате гликолиза до пирувата, и этот пируват затем окисляется в цикле Кребса или превращается в лактат.
Разделы
- Использование мышечного гликогена во время упражнений
- Регуляция мышечного гликогенолиза во время упражнений
- Тренировка и использование мышечного гликогена во время упражнений
- Поглощение глюкозы во время упражнений
- Поглощение глюкозы во время упражнений
- Регулирование мышечной активности во время упражнений
- Регулирование мышечной активности Поглощение глюкозы во время упражнений
- Сигналы сокращения для транспорта глюкозы во время упражнений
- Тренировка, захват и окисление глюкозы
- Выход глюкозы в печени во время упражнений
- Регулирование выхода глюкозы из печени во время упражнений
- Регуляция выхода глюкозы в печени во время упражнений
- Регуляция выхода глюкозы в печени во время упражнений Регуляция уровня глюкозы в печени Окисление углеводов — PDH
- Метаболизм лактата во время упражнений
- Регулирование метаболизма лактата во время упражнений
- Тренировка и метаболизм лактата во время упражнений
Использование гликогена в мышцах во время упражнений
900 02 Если мы посмотрим, как мышечный гликоген используется во время упражнений.Основными определяющими факторами права на использование гликогена являются интенсивность и продолжительность упражнений. На этом графике вы можете увидеть, как с увеличением интенсивности упражнений происходит усиление распада мышечного гликогена справа. Это сверхурочное время при заданной интенсивности упражнений снижает скорость истощения гликогена. Как мы увидим в лекциях об утомлении, истощение гликогена во время длительных физических упражнений часто связано с утомлением.
Регуляция мышечного гликогенолиза во время упражнений
Если мы задумаемся о факторах, которые регулируют распад гликогена во время упражнений, это может объяснить в первую очередь эффекты интенсивности упражнений.Мы видим, что существует местный контроль со стороны факторов, которые увеличивают в мышцах, особенно кальция, который, как вы помните, из мышечного сокращения, увеличивается в мышце при сокращении мышцы. Также увеличение неорганического фосфата, которое происходит при расщеплении мышц АТФ, является еще одним активатором ферментов, расщепляющих гликоген во время упражнений. С точки зрения гормонального контроля распада мышечного гликогена, основным регулятором является увеличение циркулирующего адреналина. По мере того, как интенсивность упражнений увеличивается и уровень адреналина в плазме увеличивается, он связывается с рецепторами в мышцах и посредством ряда шагов активирует распад гликогена в мышцах.Чем выше интенсивность упражнений, чем выше уровень адреналина, тем сильнее распад мышечного гликогена. Мы также знаем, что наличие гликогена в мышцах увеличивает их собственное разрушение. Итак, если есть повышенные запасы гликогена, вы склонны расщеплять их с большей скоростью.
Было некоторое обсуждение и споры о том, влияет ли увеличение доступности глюкозы в кровоток на распад гликогена во время упражнений. На сегодняшний день большинство исследований предполагают, что он имеет довольно скромный эффект.Напротив, если уровни жирных кислот в кровотоке увеличиваются, это, как было показано, снижает скорость распада мышечного гликогена. И были некоторые интересы в стратегиях питания, которые служат для увеличения доступности жирных кислот с целью изменения скорости распада гликогена. Наконец, повышение температуры мышц, которое вы видите, когда тренируетесь в жару, связано с более высокой скоростью распада гликогена. Таким образом, когда спортсмены занимаются спортом в жарких условиях, они часто больше полагаются на запасы гликогена в мышцах.Это имеет значение для стратегий питания, которые им необходимо адаптировать к этим обстоятельствам.
Тренировка и использование гликогена в мышцах во время тренировки
Еще одним важным фактором, влияющим на распад гликогена во время тренировки, является статус тренировки. Важной адаптацией к тренировкам является увеличение митохондриальной окислительной способности мышц, что связано с меньшим использованием гликогена. Вы можете видеть, что как аэробное, так и так называемое анаэробное использование гликогена снижается после тренировок.Это серьезная адаптация, которая, как считается, способствует повышенной сопротивляемости утомляемости, которую вы наблюдаете у хорошо тренированных субъектов во время длительных напряженных упражнений.
Поглощение глюкозы во время упражнений
Если мы обратим внимание на глюкозу из кровотока как на источник энергии для сокращения мышц, мы снова увидим, что как интенсивность, так и продолжительность упражнений влияют на скорость поглощения глюкозы. На этом графике показано поглощение глюкозы сокращающимися мышцами ног при трех уровнях интенсивности упражнений.Таким образом, увеличивается интенсивность, увеличивается потребление глюкозы, и вы также видите, что при любой заданной интенсивности упражнений прогрессивное увеличение поглощения глюкозы. Если упражнение длится несколько часов, то со временем вы увидите медленное снижение потребления глюкозы по мере снижения уровня глюкозы в крови. Это одна из причин, по которой употребление углеводосодержащих напитков часто используется спортсменами, занимающимися выносливостью, в качестве стратегии для поддержания уровня глюкозы в крови и поддержания ее усвоения во время длительных тренировок.
Поглощение глюкозы во время упражнений — Места регулирования
С точки зрения регуляции поглощения глюкозы мышцами, мы должны помнить, что этот процесс происходит за счет облегченной диффузии, и это означает, что нам нужен градиент для глюкозы, чтобы двигаться от снаружи мышцы внутрь мышцы. Нам нужна специальная транспортная молекула-носитель, чтобы помочь доставить глюкозу через мембрану. Существует три основных участка регуляции усвоения глюкозы мышцами: поступление глюкозы, транспорт глюкозы через плазматическую мембрану с помощью белка, который мы знаем как GLUT4, и внутриклеточный метаболизм глюкозы во время упражнений с большим увеличением мышечной массы. кровоток мы видим увеличение доставки глюкозы к мышцам.Происходит активация процесса транспорта глюкозы, и я расскажу об этом чуть позже. Во время упражнений усиление метаболизма через те гликолитические и окислительные пути, о которых мы говорили, означает, что глюкоза быстро метаболизируется и поддерживает градиент, по которому глюкоза перемещается в мышцы. В послетренировочный период очень важным процессом является восстановление мышечного гликогена. Повторный синтез гликогена — это основная метаболическая судьба глюкозы, которая усваивается в период восстановления.Употребление углеводов во время восстановления — важный способ максимального повторного синтеза гликогена во время восстановления.
Регуляция усвоения мышечной глюкозы во время упражнений
Если мы посмотрим на регуляцию мышечного поглощения глюкозы во время упражнений, мы увидим, что те три процесса, которые я только что упомянул, усиливаются. Увеличивается доставка глюкозы из-за увеличения мышечного кровотока. Транспортный белок GLUT4, который обычно находится внутри мышечной клетки, быстро перемещается к плазматической мембране, где становится функционирующим переносчиком глюкозы.Были некоторые споры о том, можно ли повысить активность этого транспортного белка во время упражнений. По крайней мере, на данный момент нет никаких доказательств того, что это происходит. Наконец, как я уже сказал, если вы увеличите утилизацию глюкозы через гликолитические окислительные пути, это будет поддерживать градиент диффузии в сокращающиеся скелетные мышцы. Мы знаем, что наличие других субстратов будет влиять на усвоение глюкозы. Если в мышцах высокий уровень гликогена, мы, как правило, наблюдаем более низкое поглощение глюкозы.Доступность глюкозы в кровотоке очень важна, потому что она устанавливает концентрацию глюкозы в артериальной крови для этого диффузионного градиента. Таким образом, если уровень глюкозы низкий во время длительных упражнений, при отсутствии приема глюкозы вы будете склонны видеть снижение поглощения глюкозы, а если вы увеличите уровень глюкозы в крови, проглотив углеводный напиток и всасывая глюкозу из кишечника, вы увидите увеличение поглощения глюкозы.
Влияние свободных жирных кислот на усвоение глюкозы немного менее очевидно по сравнению с воздействием на гликоген в мышцах.Некоторые исследования предполагают, что повышенная доступность жирных кислот замедляет усвоение глюкозы, в то время как другие исследования не выявили никакого эффекта. В отношении усвоения глюкозы во время упражнений важно отметить, что оно происходит независимо от инсулина. Процессы, которые участвуют в поглощении глюкозы во время мышечных сокращений, немного отличаются от процессов, связанных со стимуляцией инсулина. И именно по этой причине существует большой интерес к упражнениям как к способу улучшения усвоения глюкозы при таких заболеваниях, как диабет, при которых инсулин тоже не работает.Еще одно важное соображение заключается в том, что если вы страдаете диабетом I типа и вам необходимо вводить себе инъекцию инсулина. Если это происходит в непосредственной близости от упражнений, потому что эти два стимула дополняют друг друга, что часто может увеличить риск преждевременной гипогликемии. Вот почему диабетики I типа часто берут с собой конфеты, чтобы быстро повысить уровень глюкозы в крови, если они чувствуют, что уровень глюкозы в крови падает, или если они чувствуют то, что называется гипогликемией. Наконец, адреналин, циркулирующий адреналин, который увеличивается с увеличением интенсивности упражнений, это хорошо описанное влияние на гликоген в мышцах, а влияние на усвоение глюкозы менее очевидно.
Сигнал сокращения для транспорта глюкозы во время упражнений
Учитывая, что перемещение GLUT4 из мышечной клетки в сарколемму очень важно для удаления плазматической мембраны как барьера для поглощения глюкозы. Большой интерес вызывает молекулярная регуляция этого процесса транспорта GLUT4. На этом слайде вы можете увидеть ряд молекул и ферментов, которые участвуют в этом процессе транслокации GLUT4. Наибольшее внимание было уделено двум довольно фундаментальным изменениям в мышцах.Мы говорили об этом в лекции по адаптации, а именно об увеличении кальция и изменении энергетического статуса, которое влияет на киназу, протеинкиназу, активированную ANP. Итак, опять же, локальные события в мышцах, изменения кальция и изменения уровней энергии в мышцах служат для стимуляции транслокации GLUT4 для облегчения захвата глюкозы сокращающимися мышцами во время упражнений.
Тренировка, усвоение и окисление глюкозы
Так же, как мы видели с нейтрализацией мышечного гликогена после тренировки, мы также видим снижение зависимости от глюкозы.Это исследование было проведено с использованием меченых изотопов глюкозы, которые позволяют измерить поглощение глюкозы, а также внешний вид углеродной метки в выдыхаемом воздухе, чтобы вы могли измерить окисление. Вы можете видеть, что как поглощение глюкозы, так и ее окисление снижаются после тренировки на выносливость.
Выход глюкозы в печень во время упражнений
Теперь очень важно, чтобы концентрация глюкозы в крови поддерживалась в относительно нормальном диапазоне во время упражнений. Это роль печени во время упражнений.Таким образом, точно так же, как вы видите увеличение поглощения глюкозы мышцами, происходит параллельное увеличение выработки глюкозы в печени. Здесь вы можете видеть, что кривые выхода глюкозы в печень очень похожи на кривые поглощения глюкозы мышцами. При увеличении интенсивности упражнений и увеличении их продолжительности увеличивается выработка глюкозы в печени. Вы заметите, что при более низкой интенсивности здесь, когда продолжительность упражнения увеличивалась, в конечном итоге печень не может поддерживать тот же уровень выработки глюкозы, и он начинает снижаться.В отсутствие углеводных добавок именно в этот момент, если мышцы продолжают поглощать глюкозу, уровень глюкозы в плазме начинает снижаться.
Регуляция выработки глюкозы в печени во время упражнений
С точки зрения регуляции выработки глюкозы в печени, это довольно сложно, и существуют избыточные механизмы. Мы видим механизмы как прямой связи, так и обратной связи. Под прямой связью мы подразумеваем активацию печени параллельно с началом физических упражнений, и считается, что различные гормональные изменения и, возможно, даже некоторые симпатические нервы могут играть роль.Я расскажу об этом чуть позже. Во время упражнений меняются гормоны поджелудочной железы, уровни инсулина имеют тенденцию снижаться, а уровни глюкагона имеют тенденцию повышаться, и эти два сигнала, играющие важную роль, позволяют печени увеличивать выработку глюкозы во время упражнений. Циркулирующий адреналин также может воздействовать на запасы гликогена в печени, которые затем расщепляются с высвобождением глюкозы. Считается, что симпатические нервы играют определенную роль, хотя было проведено несколько интересных экспериментов с пациентами, которым была проведена трансплантация печени, и поэтому нервы, ведущие к печени, были перерезаны.Когда они тренируются, они все еще могут увеличить выработку глюкозы в печени. Итак, я думаю, это демонстрирует, нравится ли вам избыточность, и обычно, когда есть несколько механизмов, управляющих процессом, это означает, что этот процесс очень важен. И мы часто видим это в физиологии с рядом систем регулятивного контроля. Как и в случае с мышцами, если запасы гликогена в печени увеличиваются. Вы склонны расщеплять гликоген в печени во время упражнений и иметь более высокий выход глюкозы в печень. Первичная обратная связь, регулирующая выработку глюкозы в печени, — это концентрация глюкозы в крови.Таким образом, если он увеличивается, вы, как правило, снижаете выработку глюкозы в печени. Одним из последствий приема углеводов во время продолжительных упражнений является то, что вы фактически притупляете выход глюкозы в печень, потому что глюкоза, которая всасывается из кишечника, может компенсировать любое снижение выхода глюкозы из печени.
Тренировка и выработка глюкозы в печени во время упражнений
Есть два процесса, которые печень использует для производства глюкозы: она может расщеплять гликоген, и это называется гликогенолизом, или она также может принимать различные метаболиты, вырабатываемые во время упражнений, такие как лактат, глицерин и некоторые аминокислоты и превращают его в глюкозу в процессе, известном как глюконеогенез.Перед тренировкой вы можете увидеть на левой панели относительный вклад гликогенолиза и глюконеогенеза в общий выход глюкозы в печени. Кроме того, вы заметите, что после периода тренировок, так же, как мы наблюдали снижение усвоения и окисления глюкозы мышцами, вы можете увидеть параллельное снижение выработки глюкозы в печени. Интересно, что снижение происходит как в гликогенолизе, так и в глюконеогенезе.
Регулирование окисления углеводов — PDH
Глюкоза из кровотока и единицы глюкозы, полученные из мышечного гликогена, расщепляются в ходе ряда реакций, которые мы называем гликолизом, с образованием пирувата.У этого пирувата есть две основные судьбы: он может быть преобразован в ацетилхолин и вступить в цикл Кребса и окисляться, или он может быть преобразован в лактат. С точки зрения окисления пирувата, важного фермента, который регулирует окисление пирувата и, следовательно, скорость окисления углеводов, называют пируватдегидрогеназой. На этом слайде снова видно, что интенсивность и продолжительность являются основными детерминантами активности пируватдегидрогеназы (ПДГ). Таким образом, по мере увеличения интенсивности упражнений вы увеличиваете скорость окисления углеводов, что связано с большей активацией этого важного фермента.
Метаболизм лактата во время упражнений
Другая сторона пирувата преобразуется в лактат, и довольно хорошо известная кривая — это увеличение лактата при увеличивающейся интенсивности упражнений, и вы можете видеть на левой панели экспоненциальный рост. лактата по мере увеличения интенсивности упражнений, и это частично связано с увеличением скорости распада гликогена. Большой интерес вызвал вопрос о том, что мы называем порогом лактата, или о том, наблюдается ли это довольно значительное повышение уровня лактата.Я вернусь к этому позже, когда мы поговорим об ограничениях производительности. Но это связано с показателями выносливости, и поэтому в прикладных спортивных науках определенно проявился большой интерес к измерению реакции лактата на упражнения. Вы можете видеть, что, когда вы тренируетесь ниже порога лактата, наблюдается относительно умеренное увеличение лактата в крови. В то же время, когда вы тренируетесь выше порога лактата, вы можете увидеть устойчивый рост уровня лактата в крови.
Регуляция метаболизма лактата во время упражнений
С точки зрения регуляции метаболизма лактата во время упражнений, производство лактата действительно определяется балансом между скоростью производства пирувата и скоростью окисления.Уровни лактата, которые вы видите в крови, в свою очередь, определяются тем, сколько лактата вырабатывается сокращающимися мышцами и сколько удаляется из кровообращения либо печенью в процессе глюконеогенеза, либо мышцами, потому что это известно что сокращающиеся мышцы могут окислять лактат. Окислительная способность мышц будет влиять на способность этих мышц использовать кислород, а ферменты, которые превращают пируват в лактат, а лактат обратно в пируват, различаются по своей химической активности.Состав этих ферментов будет влиять на то, где пируват превращается в лактат, или наоборот. Показано, что подача кислорода к сокращающимся мышцам влияет на выработку лактата. Многое было о том, является ли это прямым следствием гипоксии в мышцах. Или есть ли другие изменения, сопровождающие низкий уровень кислорода, такие как увеличение адреналина, что увеличивает распад гликогена и лактата. Как я уже сказал, адреналин будет стимулировать распад гликогена, увеличивая скорость производства пирувата и, следовательно, увеличивая производство лактата.Точно так же, если у вас высокий уровень мышечного гликогена, потому что это приводит к большему расщеплению мышечного гликогена, вы также видите увеличение лактата.
Тренировки и метаболизм лактата во время упражнений
Наконец, одной из отличительных особенностей метаболических адаптаций тренировок на выносливость является снижение уровня лактата. Здесь вы можете увидеть уровни лактата в мышцах до и после тренировки с характерным снижением уровня лактата в мышцах после тренировки. Это отражается на изменении уровня лактата в крови, который также снижается после тренировки.Лактатный порог смещается вправо после тренировки. Как я сказал ранее, это используется в прикладных спортивных науках как биомаркер тренировочных адаптаций в мышцах. В последние годы наблюдается большой интерес к белкам, которые переносят лактат. Так называемые переносчики монокарбоксилатов или МСТ. Важной изоформой, которая увеличивается после тренировки, является MCT1, и она способствует поглощению лактата мышцами и митохондриями, а также способствует окислению лактата.Какова важная метаболическая судьба лактата, вырабатываемого во время упражнений? Итак, можно сказать, что на метаболизм углеводов во время упражнений влияет ряд факторов. В первую очередь интенсивность и продолжительность упражнений и тренировочный статус имеют большое влияние на метаболизм гликогена, глюкозы и лактата [6].
Цитата 6. Харгривз, Марк. «Углеводный метаболизм во время упражнений». YouTube. Coursera Inc., 20 февраля 2013 г. Интернет. 25 сен. 2014.
Вы тренер по спортивным результатам?
Если вы квалифицированный силовой тренер или тренер по спортивным показателям, мы хотим услышать ваше мнение! Если вы хотите помочь людям, посещающим наш веб-сайт, свяжитесь с нами сегодня.Мы приветствуем вас в TribeLocus — , где люди находят или рассказывают о решениях для здоровья, фитнеса и физических упражнений для повышения качества жизни и жизненного опыта .℠
Контакты
Метаболизм и энергетика | Блог HealthEngine
Что такое метаболизм?
Метаболизм в основном относится ко всем химическим реакциям в организме , используемым для производства энергии .Это включает в себя сложный набор процессов, которые превращают топливо в специализированные соединения, заряженные энергией. В организме главный конечный агент для производства энергии называется аденозинтрифосфатом (АТФ). Когда АТФ расщепляется или используется клетками, высвобождается огромное количество энергии. Эта энергия необходима для клеток, чтобы они могли расти и делиться, синтезировать важные соединения, сокращать мышцы и выполнять множество других важных функций.
Метаболизм , таким образом, производит энергию для выполнения всех функций различных тканей в организме.Метаболизм работает путем расщепления пищевых продуктов или соединений в организме на более мелкие компоненты. Затем они могут вступать в особые реакции с образованием АТФ. Оставшиеся компоненты перерабатываются организмом и используются для восстановления исходных соединений.
Источники энергии
В организме есть три основных типа молекул, которые оно использует для получения энергии:
- Углеводы: Это соединения сахарного типа в организме. Углеводы поступают из таких продуктов, как хлеб, крупы, картофель, фрукты и сахаросодержащие продукты или напитки.Когда углеводы перевариваются в желудочно-кишечной системе, они распадаются на более мелкие молекулы, такие как глюкоза (простой сахар). Основными местами хранения углеводов в организме являются печень и мышцы.
- Липиды: Это в основном относится к жирам (таким как холестерин) из рациона или хранящимся в жировой ткани (другими словами, в жировой ткани). Для получения энергии липиды расщепляются на более мелкие компоненты, называемые жирными кислотами. Следовательно, липиды на самом деле представляют собой просто цепочки жирных кислот, соединенных вместе.
- Белки: Они составляют почти три четверти всех твердых веществ в организме. Таким образом, белки являются основными структурными компонентами организма. Они состоят из более мелких агентов, называемых аминокислотами, которые считаются строительными блоками белков. Белок присутствует в диете в таких продуктах, как мясо, яйца, орехи и молочные продукты.
В целом углеводов образуют основной источник энергии для организма. Они наиболее эффективны при производстве АТФ или энергии (что означает, что они производят намного больше АТФ на количество разложенного топлива).Организм сначала расщепляет углеводы, а затем жиры и, наконец, белки, только если два других топлива истощены. Это важно, поскольку белки, как правило, менее эффективны при выработке энергии. Кроме того, белки выполняют несколько важных функций, поэтому в случае их разрушения несколько систем могут выйти из строя.
Чтобы проиллюстрировать пример, в случае голодания в организме будет меньше доступных углеводов, поэтому начнется расщепление жировых запасов в организме. Как только все доступные запасы углеводов и жира будут исчерпаны, организм начнет расщеплять белки, чтобы обеспечить энергию.
На схеме ниже представлены основные источники энергии организма. Они расщепляются ферментами на более мелкие частицы. Эти небольшие углеродные цепочки могут затем попасть по особым путям для выработки энергии (обсуждается ниже).
Аэробный обмен
Аэробный метаболизм относится к метаболическим процессам, которые происходят в присутствии кислорода. Кислород действует как окислитель при сгорании различных видов топлива. Происходят особые реакции, которые в конечном итоге приводят к тому, что кислород принимает электроны (маленькие отрицательно заряженные частицы).Это вызывает высвобождение энергии и производство АТФ. Продукты жизнедеятельности — это вода и углекислый газ, которые легко выводятся из организма. Углеводы — основное топливо, используемое для аэробного метаболизма.
В отсутствие кислорода некоторые реакции невозможны. Другой процесс происходит с участием пировиноградной кислоты, которая также приводит к выработке АТФ. Эти механизмы позволяют клеткам выжить еще несколько минут, когда они лишены кислорода. Анаэробный метаболизм вызывает накопление молочной кислоты.Кроме того, это менее эффективный способ производства энергии. На одну молекулу исходного топлива образуется меньше АТФ.
Углеводный обмен
Когда углеводов расщепляются в кишечнике, они превращаются в более мелкие простые сахара, которые могут всасываться. Глюкоза является основным производимым агентом. Глюкоза попадает в клетки и либо сразу же расщепляется для производства энергии, либо превращается в гликоген (форма хранения глюкозы). Основные запасы гликогена в организме находятся в печени и мышцах.При необходимости эти источники можно использовать для получения энергии.
Гликоген расщепляется, чтобы воспроизвести глюкозу . Глюкоза претерпевает ряд реакций, чтобы в конечном итоге произвести АТФ. Эти реакции зависят от адекватного поступления кислорода и глюкозы. Если кислорода не хватает, глюкоза может расщепляться другим набором реакций, как описано выше. Однако, если глюкозы не хватает, организм обратится к другим источникам топлива для получения энергии.
Метаболизм глюкозы включает следующие этапы:
- Гликолиз: В основном это относится к расщеплению глюкозы на вещество, называемое пировиноградной кислотой.В результате этой реакции образуется пара молекул АТФ.
- Цикл Кребса: Пировиноградная кислота входит в цикл Кребса, превращаясь в ацетил-КоА. Это снова серия реакций, которая приводит к расщеплению топлива на диоксид углерода и воду. Это дает больше полезной энергии. Исходное соединение регенерируется, поэтому цикл может продолжаться. Цикл Кребса происходит в митохондриях клеток. Это маленькие органы овальной формы с двойной мембраной, маленькие органы клеток, которые действуют как электростанции клеток.
- Окислительное фосфорилирование: Во время цикла Кребса большая часть потенциальной энергии передается в виде электронов другому соединению, называемому НАД. Это нарушается в цепи переноса электронов. Происходит цепочка реакций, когда электроны передаются следующему соединению в очереди. Последним агентом, принимающим электроны, является кислород. Этот процесс генерирует много энергии, которая превращается в АТФ.
Липидный обмен
Липиды — это в основном жиры в организме, которые включают холестерин, триглицериды и фосфолипиды.Основными их компонентами являются жирные кислоты, которые выделяются при расщеплении липидов. Жирные кислоты всасываются через кишечник и попадают через лимфатическую систему. Жиры можно использовать для получения энергии или накапливать в жировой ткани. Метаболизм липидов включает следующие процессы:
- Липолиз: Это относится к расщеплению жиров на их жирные кислоты и другие компоненты. Некоторые из этих агентов могут непосредственно вступать в цикл Кребса для окисления.Триглицериды расщепляются на жирные кислоты и глицерин. Последний превращается в пировиноградную кислоту, которая может войти в цикл Кребса.
- Бета-окисление: Это относится к расщеплению жирных кислот в митохондриях. В результате этого процесса образуется АТФ, а также ацетил-КоА, который может вступать в цикл Кребса и производить больше энергии.
Обмен липидов эффективен с точки зрения производства АТФ. Однако липиды не растворяются в крови, поэтому доступ к их запасам может быть затруднен.Поэтому на них не полагаются для производства большого количества АТФ за короткое время, а скорее используются, когда запасы углеводов ограничены.
Кетоз
Кетоз означает повышенную концентрацию кетонов тел в крови. Наиболее распространенным производимым кетоном является уксусная кислота . Это вызвано метаболизмом преимущественно жиров при отсутствии достаточного углеводного обмена. Таким образом, это признак голодания, сахарного диабета (поскольку инсулин не может транспортировать глюкозу к клеткам) и иногда возникает, когда диета почти полностью состоит из жиров.
Когда углеводы недоступны для получения энергии, организм переключается на метаболизм жирных кислот . Организм берет их из жировой ткани (жировые запасы тела). Образующиеся жирные кислоты могут быть расщеплены для получения энергии или могут быть преобразованы в кетоновые тела в печени. Некоторые кетоны могут выделяться с дыханием и придавать ему сладкий запах (ацетоновое дыхание).
Обмен белков
Тело состоит из большого количества белков, различных структур и функций.Основной компонент белков — аминокислоты. Примерно 20 различных аминокислот составляют строительные блоки всех белков. Аминокислоты подразделяются на незаменимые (это означает, что они необходимы в диете, поскольку организм не может их синтезировать) и несущественные (что означает, что организм может вырабатывать их при необходимости).
Правильный баланс аминокислот необходим для того, чтобы можно было синтезировать все важные белки. Когда белки перевариваются, связи между аминокислотами разрываются, и они высвобождаются.Обычно аминокислоты перерабатываются и используются для производства новых белков. Однако, если источники энергии ограничены, аминокислоты можно использовать для выработки энергии. Это должно происходить только тогда, когда запасы углеводов и жиров истощаются, поскольку белки составляют несколько важных структур в организме. Если они подвергаются интенсивному метаболизму, это может нарушить функцию тканей.
В метаболизме белков происходят следующие процессы:
- Дезаминирование: Первым шагом в расщеплении аминокислот является удаление аминогруппы (части аминокислотной структуры, содержащей азот и водород).В результате этого процесса образуется аммиак, который печенью превращается в мочевину. Затем мочевина может выводиться с мочой. Аминокислота превращается в соединение, называемое кетокислотой, которое может вступать в цикл Кребса.
- Окисление аминокислот: Это относится к распаду кетокислот и образованию АТФ, подобно ацетил-КоА в углеводном и липидном обмене. Количество АТФ, производимого в результате метаболизма белков, немного меньше, чем метаболизм глюкозы для эквивалентных весов.
Последствия потери веса
Некоторые диеты используют вышеуказанные принципы метаболизма для снижения веса . Чтобы похудеть, ваше тело должно сжигать больше калорий (посредством упражнений), чем требуется из рациона. Некоторые диеты ограничивают общее количество калорий, что, очевидно, приведет к потере веса, поскольку будут использованы запасы энергии тела. Другие диеты работают, пытаясь изменить нормальный баланс между метаболизмом углеводов, липидов и белков. Помните, что организм сначала сжигает углеводы, а затем жиры и белки, только когда два других истощены.Поэтому, если углеводы в рационе ограничены, организм начнет сжигать жировые отложения. Низкокалорийные диеты (ЖКД) и программы замены еды, такие как диета Тони Фергюсона, работают именно по этому механизму.
Статья любезно просмотрена:
Группа по интересам DAA WA по онкологии
и
Food4Health (Helen Baker Dietitian-APD)
Дополнительная информация
| Для получения дополнительной информации о фитнесе и физических упражнениях, включая растяжки, типы упражнений, восстановление после упражнений и упражнения с нарушениями здоровья, а также некоторые полезные видеоролики, см. Фитнес и упражнения. |
| Для получения дополнительной информации о питании, включая информацию о типах и составе продуктов, питании и людях, условиях, связанных с питанием, а также диетах и рецептах, а также некоторых полезных видео и инструментах, см. Питание. |
| Для получения дополнительной информации об ожирении, медицинских и социальных проблемах, методах снижения веса, а также о некоторых полезных инструментах см. Ожирение и потеря веса . |
Список литературы
- Fine EJ, Feinman RD. Термодинамика диет для похудения. Нутр Метаб (Лондон) . 2004; 1 (1): 15. [Аннотация | Полный текст]
- Guyton AC, зал JE. Учебник медицинской физиологии (10-е издание). Эдинбург: WB Saunders Company; 2000. [Книга]
- Джонсон Л. Основная медицинская физиология (2-е издание). Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 1998. [Книга]
- Martini F, Обер WC.Основы анатомии и физиологии (5-е издание). Нью-Джерси, Нью-Джерси: Прентис-Холл; 2001. [Книга]
Метаболизм и регуляция глюкозы: помимо инсулина и глюкагона
Abstract
Инсулин и глюкагон являются мощными регуляторами метаболизма глюкозы. Для десятилетиями мы рассматривали диабет с бигормональной точки зрения на глюкозу. регулирование. Эта точка зрения неполна и неадекватна для объяснения некоторых трудностей, с которыми сталкиваются пациенты и практикующие врачи при попытке строго контролировать концентрацию глюкозы в крови.Интенсивное лечение диабета с инсулином чревато расстройствами и риском. Несмотря на все наши усилия, колебания уровня глюкозы непредсказуемы, а гипогликемия и увеличение веса общий. Эти проблемы могут быть результатом недостатков или отклонений в другие глюкорегуляторные гормоны. Новое понимание ролей других гормоны поджелудочной железы и инкретин привели к мультигормональному взгляду на глюкозу гомеостаз.
ИСТОРИЧЕСКАЯ ПЕРСПЕКТИВА
Наше понимание диабета как метаболического заболевания изменилось. значительно с момента открытия инсулина в 1920-х годах.Инсулин был идентифицирован как мощный гормональный регулятор как появления глюкозы, так и исчезновение в кровообращении. Впоследствии диабет рассматривался как моногормональное расстройство, характеризующееся абсолютным или относительным инсулином дефицит. С момента своего открытия инсулин был единственным доступным фармакологическое лечение пациентов с сахарным диабетом 1 типа и основной терапия для пациентов с инсулино-дефицитным типом 2 сахарный диабет. 1–7
Недавнее открытие дополнительных гормонов с глюкорегуляторным действием. расширило наше понимание того, как различные гормоны способствуют гомеостазу глюкозы.В 1950-х годах глюкагон был охарактеризован как главный стимул производства глюкозы в печени. Это открытие привело к лучшему понимание взаимодействия между инсулином и глюкагоном, что приводит к бигормональное определение диабета. Впоследствии открытие второго О β-клеточном гормоне амилине впервые сообщили в 1987 году. Был определен амилин. иметь роль, дополняющую роль инсулина, и, как и инсулин, было обнаружено быть дефицитным у людей с диабетом. Эта более поздняя разработка привела к взгляд на гомеостаз глюкозы с участием нескольких панкреатических гормоны. 8
В середине 1970-х годов было идентифицировано несколько гормонов кишечника. Один из них, инкретиновый гормон, глюкагоноподобный пептид-1 (GLP-1), был признан еще одним важный вклад в поддержание уровня глюкозы гомеостаз. 9,10 Согласно современным представлениям, гомеостаз глюкозы регулируется взаимодействие гормонов инсулина, глюкагона, амилина и инкретина.
Это расширенное понимание гомеостаза глюкозы будет центральным в разработка новых фармакологических агентов для улучшения клинических результатов и качество жизни людей с диабетом.В этом обзоре основное внимание будет уделено более недавно обнаруженные гормоны, участвующие в гомеостазе глюкозы и не предназначен для всестороннего обзора методов лечения диабета.
НОРМАЛЬНАЯ ФИЗИОЛОГИЯ
Концентрация глюкозы в плазме является функцией скорости поступления глюкозы. кровообращение (появление глюкозы) уравновешивается скоростью удаления глюкозы из кровообращения (исчезновение глюкозы). Циркулирующая глюкоза получается из трех источников: кишечное всасывание во время сытости, гликогенолиз и глюконеогенез.Главный фактор, определяющий, насколько быстро глюкоза появляется в кровообращении во время сытого состояния — это скорость желудочного опорожнение. Другие источники циркулирующей глюкозы происходят в основном из печеночные процессы: гликогенолиз, расщепление гликогена, полимеризация форма хранения глюкозы; и глюконеогенез, образование глюкозы в основном из лактата и аминокислот во время голодания.
Гликогенолиз и глюконеогенез частично находятся под контролем глюкагон, гормон, вырабатываемый α-клетками поджелудочной железы.В течение в первые 8–12 часов голодания гликогенолиз является основным механизмом. какая глюкоза становится доступной (рис. 1А). Глюкагон облегчает этот процесс и, таким образом, способствует выработке глюкозы. появление в обращении. При более длительном голодании глюкоза, продуцируется глюконеогенезом, высвобождается из печени.
Рисунок 1.Гомеостаз глюкозы: роль инсулина и глюкагона. 1А. Для у людей, не страдающих диабетом, натощак, глюкоза плазмы получается из гликогенолиз под руководством глюкагона (1).Базальный уровень инсулина контролировать утилизацию глюкозы (2). Роль инсулина в подавлении глюконеогенеза и гликогенолиз минимален из-за низкой секреции инсулина натощак состояние (3). 1Б. Для людей, не страдающих диабетом и находящихся в состоянии питания, уровень глюкозы в плазме составляет происходит из-за приема внутрь питательных веществ (1). В бигормональной модели глюкагон секреция подавляется за счет действия секреции эндогенного инсулина (2). Это действие осуществляется паракринным путем (коммуникация внутри островковых клеток) (3).Дополнительно в сытом состоянии инсулин подавляет глюконеогенез и гликогенолиз в печени (4) и способствует удаление глюкозы на периферии (5). 1С. Для людей с диабетом в в состоянии натощак глюкоза плазмы образуется в результате гликогенолиза и глюконеогенез (1) под руководством глюкагона (2). Экзогенный инсулин (3) влияет на скорость исчезновения периферической глюкозы (4) и из-за его недостаток в портальном кровообращении, не регулирует должным образом степень, в которой происходит печеночный глюконеогенез и гликогенолиз (5).1D. Для лицам с диабетом в сытом состоянии экзогенный инсулин (1) неэффективен в подавлении секреции глюкагона через физиологические паракринный путь (2), что приводит к увеличению продукции глюкозы в печени (3). В виде в результате появление глюкозы в кровообращении превышает скорость исчезновение глюкозы (4). Чистый эффект — постпрандиальная гипергликемия. (5).
Глюкорегуляторные гормоны включают инсулин, глюкагон, амилин, GLP-1, глюкозозависимый инсулинотропный пептид (GIP), адреналин, кортизол и гормон роста.Из них инсулин и амилин являются производными β-клетки, глюкагон из α-клеток поджелудочной железы, а также GLP-1 и GIP из L-клеток кишечника.
Глюкорегуляторные гормоны организма предназначены для поддержания концентрации циркулирующей глюкозы в относительно узком диапазоне. в в состоянии натощак глюкоза покидает кровообращение с постоянной скоростью. Чтобы идти в ногу при исчезновении глюкозы необходима эндогенная продукция глюкозы. Для для всех практических целей единственным источником выработки эндогенной глюкозы является печень.Почечный глюконеогенез вносит существенный вклад в системный пул глюкозы только в периоды крайнего голодания. Хотя большинство тканей обладают способностью гидролизовать гликоген, только печень и почки содержат глюкозо-6-фосфатаза, фермент, необходимый для высвобождения глюкозы в тираж. В бигормональной модели гомеостаза глюкозы инсулин является ключевой регулирующий гормон исчезновения глюкозы, а глюкагон является основным регулятор появления глюкозы. После достижения пика после еды кровь глюкоза медленно снижается в течение следующих нескольких часов, в конечном итоге возвращаясь до уровня голодания.Сразу после кормления удаление глюкозы в скелетные мышцы и жировая ткань управляются в основном инсулином. В то же время, эндогенное производство глюкозы подавляется 1) прямым действием инсулин, доставляемый через воротную вену в печень и 2) паракринный эффект или прямая связь внутри поджелудочной железы между α- и β-клетки, что приводит к подавлению глюкагона (Фигура 1Б). 11–14
β-КЛЕТОЧНЫЕ ГОРМОНЫ
Инсулин
До недавнего времени инсулин был единственным известным гормоном β-клеток поджелудочной железы. для снижения концентрации глюкозы в крови.Инсулин, небольшой белок, состоящий из две полипептидные цепи, содержащие 51 аминокислоту, являются ключевым анаболическим гормоном который секретируется в ответ на повышение уровня глюкозы в крови и аминокислот после приема пищи. Как и многие гормоны, инсулин оказывает свое действие через связывание со специфическими рецепторами, присутствующими на многих клетках тела, включая жировые, печеночные и мышечные клетки. Основное действие инсулина — стимулируют исчезновение глюкозы.
Инсулин помогает контролировать уровень глюкозы после приема пищи тремя способами.Первоначально, инсулин сигнализирует клеткам чувствительных к инсулину периферических тканей, в первую очередь скелетные мышцы, чтобы увеличить их поглощение глюкоза. 15 Во-вторых, инсулин действует на печень, способствуя гликогенезу. Наконец, инсулин одновременно подавляет секрецию глюкагона α-клетками поджелудочной железы, таким образом сигнал печени о прекращении производства глюкозы посредством гликогенолиза и глюконеогенез (таблица 1).
Таблица 1.Эффекты первичных глюкорегуляторных гормонов
Все эти действия снижают кровообращение глюкоза. 13 Другое действия инсулина включают стимуляцию синтеза жира, стимулирование хранение триглицеридов в жировых клетках, стимулирование синтеза белка в печени и мышцы, и разрастание клеток рост. 13
Действие инсулина тщательно регулируется в ответ на циркулирующую глюкозу концентрации. Инсулин не секретируется, если концентрация глюкозы в крови ≤ 3,3 ммоль / л, но секретируется в возрастающих количествах в виде глюкозы концентрация увеличивается сверх этого порог. 14 После приема пищи секреция инсулина происходит в две фазы: начальная быстрое высвобождение предварительно сформированного инсулина с последующим усилением синтеза инсулина и высвобождение в ответ на глюкозу в крови. Происходит длительное высвобождение инсулина если концентрация глюкозы остается высокая. 13,14
В то время как глюкоза является наиболее мощным стимулом для инсулина, другие факторы стимулируют секрецию инсулина. Эти дополнительные стимулы включают повышенное содержание плазмы. концентрации некоторых аминокислот, особенно аргинина, лейцина и лизина; GLP-1 и GIP высвобождаются из кишечника после еды; и парасимпатический стимуляция через блуждающий нерв нерв. 16,17
Амилин
Изолирован из амилоидных отложений поджелудочной железы на островках Лангерганса, Впервые амилин был описан в литературе в 1987 году. Амилин, 37-амино кислотный пептид, нейроэндокринный гормон, коэкспрессируемый и секретируемый с инсулин β-клетками поджелудочной железы в ответ на питательные вещества стимулы. 8,10,18,19 Когда секретируется поджелудочной железой, молярное соотношение инсулина и амилина в воротной вене тираж примерно 50: 1. Из-за извлечения инсулина из печени, это соотношение падает до ~ 20: 1 на периферии тираж. 20,21
Исследования на людях показали, что секреторная и плазменная профили концентрации инсулина и амилина аналогичны при низком голодании. концентрации и увеличивается в ответ на питательные вещества потребление. 22,23 У здоровых взрослых концентрация амилина в плазме натощак колеблется от 4 до 8. пмоль / л после приема пищи повышается до 25 пмоль / л. У пациентов с диабетом амилин недостаточен при типе 1 и нарушен при типе 2 сахарный диабет. 24,25
Доклинические данные показывают, что амилин работает с инсулином, помогая координировать скорость появления и исчезновения глюкозы в кровообращение, тем самым предотвращая аномальное повышение концентрации глюкозы (Фигура 2). 26
Рис. 2.Постпрандиальный поток глюкозы в контрольной группе без диабета. Постпрандиальный поток глюкозы — это баланс между появлением глюкозы в кровообращении и исчезновение или поглощение глюкозы. Внешний вид глюкозы — это функция печени. (эндогенное) производство глюкозы и источники пищи, и регулируется гормоны поджелудочной железы и кишечника. Исчезновение глюкозы опосредовано инсулином. Рассчитано на основе данных исследования Pehling et al. al. 26
Амилин дополняет эффекты инсулина на циркулирующую глюкозу концентрации через два основных механизма (Рисунок 3).Амилин подавляет постпрандиальный глюкагон секреция, 27 тем самым снижая выработку глюкозы в печени, стимулированную глюкагоном, после прием питательных веществ. Это подавление постпрандиальной секреции глюкагона постулируется, что центрально опосредуется эфферентными блуждающими сигналами. Важно отметить, что амилин не подавляет секрецию глюкагона во время индуцированного инсулином гипогликемия. 21,28 Амилин также замедляет скорость опорожнения желудка и, следовательно, скорость, с которой питательные вещества доставляются из желудка в тонкий кишечник для абсорбция. 29 дюйм в дополнение к его влиянию на секрецию глюкагона и скорость желудочного опорожняя, амилин дозозависимо снижает потребление пищи и массу тела в животные модели (таблица 1). 30–32
Рис. 3.Гомеостаз глюкозы: роль инсулина, глюкагона, амилина и GLP-1. Мультигормональная модель гомеостаза глюкозы (недиабетики): в в состоянии сытости амилин общается через нервные пути (1), подавляя постпрандиальная секреция глюкагона (2), помогая замедлить скорость желудочного опорожнение (3).Эти действия регулируют скорость появления глюкозы в тираж (4). * На животных моделях было показано, что амилин дозозависимо снижение потребления пищи и массы тела (5). Кроме того, инкретиновые гормоны, такие как как и GLP-1, глюкозозависимо усиливает секрецию инсулина (6) и подавляет секреция глюкагона (2) и, через нервные пути, помогает замедлить опорожнение желудка и снизить потребление пищи и массу тела (5).
Амилин действует главным образом через центральную нервную систему.Исследования на животных выявили специфические участки рецепторов, подобных кальцитонину, для амилин в областях мозга, преимущественно в области постремы. Площадь postrema является частью дорсального блуждающего комплекса ствола головного мозга. Заметный Особенностью области постремы является то, что в ней отсутствует гематоэнцефалический барьер, что позволяет подверженность быстрым изменениям концентрации глюкозы в плазме, а также циркулирующие пептиды, в том числе амилин. 33–36
Таким образом, амилин регулирует скорость появления глюкозы из как эндогенные (печеночные), так и экзогенные (полученные из пищи) источники, и инсулин регулирует уровень глюкозы исчезновение. 37
α-КЛЕТОЧНЫЙ ГОРМОН: ГЛЮКАГОН
Глюкагон — ключевой катаболический гормон, состоящий из 29 аминокислот. это секретируются α-клетками поджелудочной железы. Описанный Роджером Унгером в 1950-х годах, глюкагон был охарактеризован как противодействующий эффекту инсулин. 38 глюкагон играет важную роль в поддержании уровня глюкозы в плазме натощак за счет стимуляция выработки глюкозы в печени.
Унгер первым описал диабетическое состояние как «Бигормональное» заболевание, характеризующееся дефицитом инсулина и избыток глюкагона.Он также предположил, что терапия, направленная на коррекцию избытка глюкагона станет важным шагом вперед в лечении сахарный диабет. 38
Производство глюкозы в печени, которое в первую очередь регулируется глюкагоном, поддерживает базальную концентрацию глюкозы в крови в пределах нормы во время состояние голодания. Когда уровень глюкозы в плазме падает ниже нормы, глюкагон секреция увеличивается, что приводит к выработке глюкозы в печени и возвращению уровень глюкозы в плазме до нормы диапазон. 39,40 Этот эндогенный источник глюкозы не нужен во время и сразу после еды, и секреция глюкагона подавляется. В сочетании с прямое воздействие инсулина на печень, подавление глюкагона приводит к почти полное подавление выработки глюкозы в печени (Рисунок 4).
Рис. 4.Секреция инсулина и глюкагона: пациенты, не страдающие диабетом и диабетом. У субъектов, не страдающих диабетом (левая панель), глюкозо-стимулированный инсулин и амилин высвобождение из β -клеток приводит к подавлению постпрандиального секреция глюкагона.У субъекта с диабетом 1 типа инфузионный инсулин не подавлять α -клеточную продукцию глюкагона. Адаптированы из Ref. 38 .
В диабетическом состоянии неадекватное подавление постпрандиального секреция глюкагона (гиперглюкагонемия) 41,42 приводит к повышению выработки глюкозы в печени (Рисунок 4). Важно отметить, что экзогенно вводимый инсулин не может восстановить нормальный постпрандиальный концентрация инсулина в воротной вене и подавление секреции глюкагона через паракринный эффект.Это приводит к аномально высокому соотношение глюкагона и инсулина, которое способствует высвобождению печеночного глюкоза. 43 Эти пределы экзогенно вводимой инсулиновой терапии хорошо задокументированы в люди с диабетом 1 или 2 типа и считаются важными способствуют постпрандиальному гипергликемическому состоянию, характерному для сахарный диабет.
ИНКРЕТИНОВЫЕ ГОРМОНЫ GLP-1 И GIP
Сложности гомеостаза глюкозы становятся более ясными при рассмотрении роль пептидов кишечника.К концу 1960-х годов Перли и Кипнис 44 и другие продемонстрировали, что проглоченная пища вызывает более сильное высвобождение инсулина, чем глюкоза вводится внутривенно. Этот эффект, получивший название «инкретин эффект », предположил, что сигналы от кишечника важны для гормональная регуляция исчезновения глюкозы. Кроме того, эти гормональные сигналы от проксимального отдела кишечника, по-видимому, помогают регулировать опорожнение желудка и кишечника. моторика.
Было охарактеризовано несколько гормонов инкретина, и доминирующие из них для гомеостаза глюкозы используются GIP и GLP-1.GIP стимулирует секрецию инсулина и регулирует метаболизм жиров, но не подавляет секрецию глюкагона или опорожнение желудка. 45 Уровни GIP в норме или немного повышены у людей с типом 2. сахарный диабет. 46 В то время как GIP — более мощный инкретиновый гормон, GLP-1 секретируется в большей концентрации и более физиологически актуален в люди. 47
GLP-1 также стимулирует глюкозозависимую секрецию инсулина, но является значительно снижается после приема пищи у людей с диабетом 2 типа или нарушение глюкозы толерантность. 46,48 GLP-1 стимулирует секрецию инсулина при высоких концентрациях глюкозы в плазме но не тогда, когда концентрация глюкозы в плазме приближается или падает ниже нормы диапазон. GLP-1 происходит из молекулы проглюкагона в кишечнике. синтезируется и секретируется L-клетками, обнаруженными в основном в подвздошной и толстой кишке. Концентрации циркулирующего GLP-1 низкие в состоянии натощак. Однако оба GIP и GLP-1 эффективно стимулируются при приеме смешанного или смешанного приема пищи. обогащен жирами и углеводы. 49,50 В отличие от GIP, GLP-1 подавляет секрецию глюкагона и замедляет работу желудочного сока. опорожнение. 51
GLP-1 обладает множеством глюкорегуляторных эффектов (Таблица 1 и Рисунок 3). В поджелудочной железе GLP-1 стимулирует секрецию инсулина глюкозозависимым образом, в то время как ингибирование глюкагона секреция. 52,53 Исследования на животных показали, что действие GLP-1 происходит напрямую. через активацию рецепторов GLP-1 на β-клетках поджелудочной железы и косвенно через сенсорное нервы. 54 GLP-1 имеет период полувыведения из плазмы составляет около 2 минут, и его исчезновение регулируется в первую очередь за счет фермента дипептидилпептидазы-IV (DPP-IV), который быстро расщепляет и инактивирует GLP-1.
Инфузия GLP-1 снижает уровень глюкозы после приема пищи, а также при голодании в течение ночи глюкоза в крови концентрации. 55 Постпрандиальный эффект GLP-1 частично обусловлен ингибированием глюкагона. секреция. Тем не менее, хотя GLP-1 ингибирует секрецию глюкагона в состоянии сытости, он не притупляет реакцию глюкагона на гипогликемия. 56 GLP-1 помогает регулировать опорожнение желудка и кислотность желудочного сока. секреция, 17 возможно, передавая сигналы рецепторам GLP-1 в головном мозге и тем самым стимулируя эфферентные тракты блуждающего нерва нерв. 56 Как желудочный опорожнение замедляется, постпрандиальный выброс глюкозы снижается. Администрация GLP-1 был связан с регуляцией пищевого поведения и тела масса. 57,58 Кроме того, сообщалось о наблюдениях улучшения уровня инсулина GLP-1. чувствительность и повышение уровня глюкозы утилизация. 58
Значительный и растущий интерес вызывает роль GLP-1 в сохранение функции β-клеток и β-клеток распространение. 59 дюйм исследования на животных, было показано, что GLP-1 усиливает функциональные β-клетки масса. 59
ДИАБЕТ ПАТОФИЗИОЛОГИЯ
Наше понимание патофизиологии диабета постоянно развивается. Тип 1 диабет был охарактеризован как аутоиммунно-опосредованное разрушение панкреатический β-клетки. 60 The возникающий дефицит инсулина также означает дефицит другого секретируемый и колокированный гормон β-клеток, амилин. 25 Как в результате концентрация глюкозы после приема пищи повышается из-за отсутствия инсулино-стимулированное исчезновение глюкозы, плохо регулируемая печеночная глюкоза продуктивность, а также повышенное или ненормальное опорожнение желудка после еда. 61
Раннее течение диабета 2 типа, постпрандиальное действие β-клеток становится ненормальным, о чем свидетельствует потеря немедленного инсулинового ответа на еда. 62 Периферийное устройство инсулинорезистентность сочетается с прогрессирующей недостаточностью β-клеток и снижается доступность инсулина, амилина и GLP-1 63 внести свой вклад к клинической картине гипергликемии при сахарном диабете.
Аномальное опорожнение желудка характерно для диабета как 1-го, так и 2-го типа. В скорость опорожнения желудка является ключевым фактором, определяющим уровень глюкозы после приема пищи концентрации (рис. 5). 64 Если опорожнение желудка ускоряется, то представление пищи, полученной поступление глюкозы в кровоток плохо синхронизируется с доставкой инсулина. В люди с диабетом, отсутствие или задержка секреции инсулина в дальнейшем обостряет постпрандиальную гипергликемию. И амилин, и GLP-1 регулируют желудочный опорожнение за счет замедления доставки питательных веществ из желудка к малому кишечник.
Рис. 5.Скорость опорожнения желудка является важным фактором, определяющим постпрандиальный период. гликемия. У субъектов, не страдающих диабетом ( n = 16), уровень глюкозы в плазме концентрация увеличивается по мере увеличения скорости опорожнения желудка ( р = 0,58, P <0,05). По материалам Ref. 64 .
ЗАМЕНА ИНСУЛИНА
В течение последних 80 лет инсулин был единственным фармакологическим препаратом. альтернатива, но она заменила только одно из необходимых гормональных соединений для гомеостаза глюкозы.Новые рецептуры инсулина и инсулина секретагоги, такие как сульфонилмочевины и меглитиниды, способствуют улучшение гликемического контроля. В то время как сульфонилмочевины и меглитиниды обладают используется для прямой стимуляции β-клеток поджелудочной железы к секреции инсулина, заместительная терапия инсулином до сих пор является краеугольным камнем лечения 1 и прогрессирующий диабет 2 типа на протяжении десятилетий. Достижения в инсулинотерапии имеют включает не только улучшение источника и чистоты гормона, но и разработка более физиологических средств доставки.
Очевидно, что существуют ограничения, которые препятствуют нормализации уровня глюкозы в крови с помощью только инсулин. Во-первых, экзогенно вводимый инсулин не имитирует секреция эндогенного инсулина. В нормальной физиологии печень подвергается воздействию от двух до четырехкратного увеличения концентрации инсулина по сравнению с периферическим тираж. 65 Инсулин, вводимый периферически, не приближается к этому соотношению, что приводит к недостаточный уровень глюкозы в печени подавление. 66–68 Во-вторых, паракринное подавление глюкагона инсулином ограничено при диабете и неадекватно компенсируется периферическим инсулином (Рисунки 1C, 1D).в постпрандиальное состояние, когда концентрация глюкагона должна быть низкой, а гликогена магазины надо перестраивать, происходит парадоксальный подъем глюкагона и истощение гликогена магазины. 69 А наконец, терапевтическое увеличение доз инсулина приводит к дальнейшему периферическая гиперинсулинемия, которая может предрасполагать человека к гипогликемия и увеличение веса. Как показано в разделе «Контроль диабета» и Исследование осложнений и проспективное исследование диабета в Соединенном Королевстве, усиленный уход сопряжен с риском.В обоих исследованиях участники в группах интенсивной терапии наблюдалось увеличение числа тяжелых случаев в 2-3 раза. гипогликемия. 4,6 Кроме того, усиление контроля над диабетом было связано с увеличение веса. 70
РЕГУЛИРОВАНИЕ ДЕЙСТВИЯ ГЛЮКАГОНА
Очевидно, что заместительная инсулиновая терапия стала важным шагом на пути к восстановление гомеостаза глюкозы. Но это только часть окончательного решение. Жизненно важная взаимосвязь между инсулином и глюкагоном предполагает: дополнительные участки для лечения.При недостаточной концентрации инсулина и повышенная концентрация глюкагона в воротной вене, действие глюкагона чрезмерно, способствуя эндогенному и ненужному поступлению глюкозы в сытое состояние. На сегодняшний день не существует фармакологических средств регулирования глюкагона. и необходимость снижения постпрандиальной секреции глюкагона остается клинической проблемой. цель для будущих терапий.
ДЕЙСТВИЯ АМИЛИНА
Теперь очевидно, что появление глюкозы в кровообращении имеет центральное значение для гомеостаз глюкозы, и этот аспект не рассматривается экзогенно вводили инсулин.Амилин работает с инсулином и подавляет глюкагон. секреция. Он также помогает регулировать опорожнение желудка, что, в свою очередь, влияет на скорость появления глюкозы в кровообращении. Синтетический аналог человека амилин, который связывается с рецептором амилина, амилиномиметическим агентом, находится в разработка.
GLP-1 ДЕЙСТВИЯ
Картина гомеостаза глюкозы стала более ясной и сложной по мере того, как выяснена роль инкретиновых гормонов. Инкретиновые гормоны играют важную роль. роль в регулировании появления глюкозы и повышении уровня инсулина секреция.Секреция GIP и GLP-1 стимулируется при приеме пищи, но GLP-1 является более физиологически значимым гормон. 71,72
Однако замена GLP-1 в его естественном состоянии создает биологические проблемы. В клинических испытаниях применялась непрерывная подкожная или внутривенная инфузия. превосходит однократные или повторные инъекции GLP-1 из-за быстрого деградация GLP-1 под действием DPP-IV.
Чтобы обойти этот интенсивный и дорогостоящий метод лечения, клинические разработка соединений, которые вызывают глюкорегуляторные эффекты, аналогичные тем GLP-1 исследуются.Эти соединения, называемые миметиками инкретина, имеют более длительную продолжительность действия, чем нативный GLP-1. Помимо инкретина миметики, исследования показывают, что ингибиторы DPP-IV могут улучшить глюкозу контроль за счет увеличения действия нативного GLP-1. Эти новые классы исследуемые соединения могут усиливать секрецию инсулина и подавлять прандиальную секрецию глюкагона глюкозозависимым образом, регулировать опорожнение желудка и уменьшение количества еды потребление. 73 Наконец, миметики инкретина также могут играть роль в сохранении функции β-клеток и пролиферация β-клеток.
РЕЗЮМЕ
Несмотря на современные достижения в области фармакологической терапии диабета, достижение и поддержание оптимального гликемического контроля оставалось труднодостижимым и устрашающе. Очевидно, что усиленное ведение связано с уменьшением риск осложнения. 6,74 Тем не менее, несмотря на это научное понимание, средний гемоглобин 1c у пациентов с диабетом в США> 9%. 75
Регулирование уровня глюкозы — это изысканная комбинация многих гормонов, как поджелудочной железы и кишечника, которые оказывают влияние на несколько тканей-мишеней, таких как мышца, мозг, печень и адипоцит.В то время как практикующие врачи и пациенты имели несколько вариантов лечения в течение последних 10 лет, оба продолжать бороться за достижение и поддержание хорошего гликемического контроля. В настоящее время доступные методы лечения не полностью устраняют многие аномалии и / или недостаточность диабета 1 или 2 типа.
Остается потребность в новых мероприятиях, дополняющих наши текущие терапевтический арсенал без некоторых клинических недостатков, таких как риск гипогликемии и увеличения веса.Эти развивающиеся методы лечения предлагают потенциал для более эффективного управления диабетом за счет мультигормонального перспективу (рис. 3) и являются сейчас находится в стадии клинической разработки.
Сноски
Стивен Л. Аронофф, MD, FACP, FACE, является партнером и клиническим эндокринолог в Endocrine Associates of Dallas и директор Исследовательского Институт Далласа в Далласе, Техас. Кэти Берковиц, APRN, Британская Колумбия, FNP, CDE и Барб Шрейнер, RN, MN, CDE, BC-ADM, являются клиническими посредниками диабета с Департамент по медицинским вопросам Amylin Pharmaceuticals, Inc.в Сан-Диего, Калифорния Лаура Вант, RN, MS, CDE, CCRC, BC-ADM, это клиническое исследование координатор исследовательского института MedStar в Вашингтоне, округ Колумбия
Примечание: Доктор Аронофф получил гонорары за выступления представителей Amylin Pharmaceuticals, Inc., Eli Lilly и Компания и исследовательская поддержка со стороны Amylin, Lilly и Novo Nordisk. РС. Берковиц и г-жа Шрайнер работают в Amylin. Мисс Хант служит на консультативная группа для, является акционером и получает гонорары за выступал с выступлениями Амилин и работал координатором исследований для исследования финансируются компанией.Она также получила исследовательскую поддержку от Lilly, Novo Nordisk и MannKind Corporation. Amylin Pharmaceuticals, Inc., разрабатывает синтетические гормоны амилин и инкретин, а Mannkind Корпорация разрабатывает систему ингаляции инсулина для лечения сахарный диабет.
- Американская диабетическая ассоциация
Ссылки
- ↵
Американская диабетическая ассоциация: Клинические исследования Практические рекомендации 2004 г. Уход за диабетом 27 (Дополнение 1): S1 – S150,2004
Hirsch IB: Тип 1 сахарный диабет и использование гибких схем инсулина.Am Fam Врач 60: 2343 –2352, 2355–2356,1999
Bolli GB, Di Марчи Р.Д., Парк Г.Д., Прамминг С., Койвисто В.А.: Аналоги инсулина и их потенциал в управлении сахарным диабетом. Диабетология 42: 1151 –1167, 1999
- ↵
Исследовательская группа DCCT: Гипогликемия в Контроль над диабетом и его осложнения. Диабет46 : 271–286,1997
Исследовательская группа DCCT: прибавка в весе связаны с интенсивной терапией в борьбе с диабетом и его осложнениями Пробный.Уход за диабетом 11: 567 –573, 1988
- ↵
Учебная группа UKPDS: интенсив контроль уровня глюкозы в крови с помощью сульфонилмочевины или инсулина по сравнению с традиционное лечение и риск осложнений у пациентов с типом 2 сахарный диабет. Ланцет 352: 837 –853, 1998
- ↵
Buse JB, Weyer C, Мэггс Д.Г .: Замена амилина прамлинтидом при диабете 1 и 2 типа: a физиологический подход к преодолению барьеров с помощью инсулинотерапии. Клинический диабет 20: 137 –144, 2002
- ↵
Moore CX, Cooper GJS: Совместная секреция амилина и инсулина из культивируемых островковых бета-клеток: модуляция стимуляторами секреции питательных веществ, островковыми гормонами и гипогликемическими агентами.Biochem Biophys Res Commun 179: 1 –9, 1991
- ↵
Naslund E, Богефорс Дж., Скогар С., Грибак П., Якобссон Х., Холст Дж. Дж., Хеллстрем PM: GLP-1 замедляет опорожнение твердого желудка и подавляет высвобождение инсулина, глюкагона и PYY в людях. Am J Physiol 277: R910 –R916, 1999
- ↵
Cooper GJS, Willis AC, Кларк A, Тернер RD, Sim RB, Reid KB: Очистка и характеристика пептид из богатой амилоидом поджелудочной железы пациентов с диабетом 2 типа. Proc Natl Acad Sci U S A 84: 8628 –8632, 1987
- ↵
Wallum BJ, Kahn SE, McCulloch DK, Porte D: секреция инсулина у нормального и диабетического человека.В Международном учебнике сахарного диабета. Альберти КГММ, ДеФронцо Р.А., Кин Х., Зиммет П., ред. Чичестер, Великобритания, Джон Вили и сыновья, 1992, с.285. –301
Lefebvre PJ: Возвращение к глюкагону и его семейству. Уход за диабетом18 : 715–730,1995
- ↵
Cryer PE: Глюкоза гомеостаз и гипогликемия. В учебнике Уильяма Эндокринология. Уилсон Дж. Д., Фостер Д. В., ред. Филадельфия, Пенсильвания, W.B. Saunders Company, 1992, стр.1223. –1253
- ↵
Gerich JE: Control гликемии.Baillieres Best Pract Res Clin Endocrinol Метаб 7: 551 –586, 1993
- ↵
Gerich JE, Шнайдер В., Диппе С.Е., Ланглуа М., Ноакко К., Карам Дж., Форшем П.: Характеристика реакции глюкагона на гипогликемию у человека. J Clin Endocrinol Metab 38:77 –82, 1974
- ↵
Holst JJ: Глюкагоноподобный пептид 1: недавно открытый желудочно-кишечный гормон. Гастроэнтерология 107: 1848 –1855, 1994
- ↵
Drucker DJ: Миниобзор: глюкагоноподобные пептиды.Эндокринология142 : 521–527,2001
- ↵
Огава А., Харрис В., Маккоркл С.К., Унгер Р.Х., Ласки К.Л.: секреция амилина из поджелудочной железы крысы и его избирательная потеря после лечения стрептозотоцином. J Clin Инвестируйте 85: 973 –976, 1990
- ↵
Koda JE, Fineman M, Rink TJ, Dailey GE, Muchmore DB, Linarelli LG: концентрации амилина и контроль глюкозы. Ланцет 339: 1179 –1180, 1992
- ↵
Данные в файле, Amylin Pharmaceuticals, Inc., Сан Диего, Калифорния
- ↵
Weyer C, Maggs DG, Янг А.А., Колтерман О.Г.: Замена амилина прамлинтидом в качестве дополнения к инсулинотерапия при сахарном диабете 1 и 2 типа: физиологический подход к улучшенному метаболическому контролю. Curr Pharm Des 7: 1353 –1373, 2001
- ↵
Koda JE, Fineman МС, Колтерман О.Г., Каро Дж.Ф .: 24-часовой профиль амилина в плазме повышен в IGT субъекты против обычного контроля (Аннотация). Диабет44 (Приложение 1): 238A, 1995
- ↵
Fineman MS, Giotta Член парламента, Томпсон Р.Г., Колтерман О.Г., Кода Дж.Э .: Ответ амилина после приема Сустакала у пациентов с сахарным диабетом II типа, получавших инсулин, снижается проглатывание (Абстрактный).Диабетология 39 (Приложение 1): A149, 1996
- ↵
Янг A: Amylin’s физиология и ее роль при диабете. Курр Опин Эндокринол Диаб 4: 282 –290, 1997
- ↵
Kruger DF, Gatcomb ПМ, Оуэн СК: Клинические последствия амилина и дефицита амилина. Диабетическое образование 25: 389 –397, 1999
- ↵
Pehling G, Tessari П., Герих Дж. Э., Хеймонд М. В., Сервис Ф. Дж., Рицца Р. А.: Аномальные углеводы в пище предрасположенность к инсулинозависимому диабету: относительный вклад эндогенное производство глюкозы и начальное внутреннее поглощение и влияние интенсивная инсулинотерапия.J Clin Invest74 : 985–991,1984
- ↵
Гедулин Б.Р., Каток Т.Дж., Янг А.А.: Дозозависимый эффект глюкагоностатического действия амилина у крыс. Обмен веществ 46:67 –70, 1997
- ↵
Heise T, Heinemann L, Heller S, Weyer C, Wang Y, Strobel S, Kolterman O, Maggs D: Эффект прамлинтид на симптомы, катехоламин и глюкагон реакции на гипогликемию у здоровых людей. Обмен веществ. В прессе
- ↵
Samson M, Szarka Л.А., Камиллери М., Велла А., Зинсмайстер А.Р., Рицца Р.А.: прамлинтид, амилин. аналог, выборочно задерживает опорожнение желудка: потенциальная роль блуждающего нерва торможение.Am J Physiol 278: G946 –G951, 2000
- ↵
Bhavsar S, Watkins J, Янг A: синергия между амилином и холецистокинином для подавления приема пищи потребление у мышей. Физиологическое поведение64 : 557–561,1998
Рашинг, штат Пенсильвания, Хэган ММ, Сили Р.Дж., Латц Т.А., Вудс СК: Амилин: новое действие в мозге, снизить массу тела. Эндокринология141 : 850–853,2000
- ↵
Рашинг, штат Пенсильвания, Хэган ММ, Сили Р.Дж., Лутц Т.А., Д’Алессио Д.А., Эйр Э.Л., Вудс СК: ингибирование центрального Передача сигналов амилина увеличивает потребление пищи и ожирение у крыс.Эндокринология 142: 5035 –5038, 2001
- ↵
Wimalawansa SJ: Амилин, пептид, связанный с геном кальцитонина, кальцитонин и адреномедуллин: а пептидное суперсемейство. Критические обороты Neurobiol11 : 167–239,1997
Beeley NRA, Прикетт К.С.: Семейство пептидов амилина, CGRP и кальцитонина. Экспертное мнение о терапевтических патентах6 : 555–567,1996
Ван Россум Д., Menard DP, Fournier A, St Pierre S, Quirion R: Авторадиографическое распределение и рецепторный профиль связывания (I-125) участков связывания амилина Болтона-Хантера-крысы в мозгу крысы.J Pharmacol Exp Ther270 : 779–787, 1994
- ↵
Beaumont K, Kenney MA, Young AA, Rink TJ: Сайты связывания амилина с высоким сродством в головном мозге крысы. Мол Фармакол 44: 493 –497, 1993
- ↵
Buse JB, Weyer C, Maggs D: Замена амилина прамлинтидом при диабете 1 и 2 типа: a физиологический подход к преодолению барьеров с помощью инсулинотерапии. Клинический диабет 20: 137 –144, 2002
- ↵
Унгер RH: Глюкагон физиология и патофизиология.N Engl J Med285 : 443–449,1971
- ↵
Orci L, Malaisse-Lagae F, Amherdt M, Ravazzola M, Weisswange A, Dobbs RD, Perrelet A, Унгер Р: Клеточные контакты на островках Лангерганса человека. J Clin Эндокринол Метаб 41: 841 –844, 1975
- ↵
Герих Дж., Дэвис Дж., Лоренци М., Рицца Р., Боханнон Н., Карам Дж., Льюис С., Каплан Р., Шульц Т., Крайер П: Гормональные механизмы восстановления после гипогликемии у человека. Am J Physiol 236: E380 –E385, 1979
- ↵
Cryer PE: Глюкоза противодействие в человеке.Сахарный диабет 30 : 261–264,1981
- ↵
Dinneen S, Alzaid A, Turk D, Rizza R: Отсутствие подавления глюкагона способствует постпрандиальная гипергликемия при ИЗСД. Диабетология38 : 337–343,1995
- ↵
Baron AD, Schaeffer L, Schragg P, Kolterman OG: Роль гиперглюкагонемии в поддержании повышенных показателей выработки глюкозы в печени при диабете II типа. Диабет 36: 274 –283, 1987
- ↵
Перли М.Дж., Кипнис DM: реакция инсулина плазмы на пероральную и внутривенную глюкозу: исследования в нормальные и диабетические субъекты.J Clin Invest46 : 1954–1962, 1967
- ↵
Ип Р.Г., Вульф ММ: Биология GIP и жировой обмен. Life Sci66 : 91–103,2000
- ↵
Vilsboll T, Krarup Т., Дикон К.Ф., Мадсбад С., Холст Дж. Дж.: Снижение концентрации постпрандиальных интактный биологически активный глюкагоноподобный пептид 1 при диабете 2 типа пациенты. Диабет 50: 609 –613, 2001
- ↵
Nauck MA, Heimesaat MM, Orskov C, Holst JJ, Ebert R, Creutzfeldt W: Консервированный инкретин активность глюкагоноподобного пептида 1 [7-36 амид], но не синтетического человеческого желудочный ингибирующий полипептид у пациентов с сахарным диабетом 2 типа.Дж. Клин Инвест 91: 301 –307, 1993
- ↵
Lugari R, Dei Cas А, Уголотти Д., Финарди Л., Барилли А.Л., Огнибене С., Лучани А., Зандоменеги Р., Gnudi A: Доказательства раннего нарушения индуцированного глюкагоноподобным пептидом 1 секреция инсулина при диабете 2 типа (инсулинозависимый) человека. Horm Metab Res 34: 150 –154, 2002
- ↵
Herrmann C, Goke R, Richter G, Fehmann HC, Arnold R, Goke B: глюкагоноподобный пептид-1 и уровни глюкозозависимого инсулин-высвобождающего полипептида в плазме в ответ на питательные вещества.Пищеварение 56: 117 –126, 1995
- ↵
Elliott RM, Morgan LM, Trefger JA, Deacon S, Wright J, Marks V: глюкагоноподобный пептид-1 (7-36) секреция амида и глюкозозависимого инсулинотропного полипептида в ответ к попаданию в организм человека питательных веществ: паттерны острой постпрандиальной и 24-часовой секреции. Дж. Эндокринол 138: 159 –166, 1993
- ↵
Matsuyama T, Komatsu R, Namba M, Watanabe N, Itoh H, Tarui S: глюкагоноподобный пептид-1 (7-36 амид): мощный глюкагоностатический и инсулинотропный гормон.Диабет Res Clin Pract 5: 281 –284, 1988
- ↵
Nauck MA, Holst JJ, Willms B, Schmiegel W: глюкагоноподобный пептид 1 (GLP-1) как новый терапевтический подход к диабету 2 типа. Exp Clin Endocrinol Диабет 105: 187 –195, 1997
- ↵
Perfetti R, Merkel P: глюкагоноподобный пептид-1: главный регулятор бета-клеток поджелудочной железы. функция. Eur J Endocrinol 143: 717 –725, 2000
- ↵
Burcelin R, Da Коста А, Друкер Д., Торенс Б: Глюкозная компетентность гепатопортальной вены сенсор требует наличия активированного рецептора глюкагоноподобного пептида-1.Диабет 50: 1720 –1728, 2001
- ↵
Рахман Дж., Гриббл FM, Барроу Б.А., Леви Дж. К., Бьюкенен К. Д., Тернер Р. К.: Нормализация инсулина. ответы на глюкозу при инфузии глюкагоноподобного пептида 1 в течение ночи (7-36) амид у пациентов с NIDDM. Диабет45 : 1524–1530,1996
- ↵
Nauck MA, Heimesaat MM, Behle K, Holst JJ, Nauck MS, Ritzel R, Hufner M, Schmiegel WH: Влияние глюкагоноподобного пептида 1 на противорегулирующие гормональные реакции, когнитивные функции и секреция инсулина при гиперинсулинемии ступенчатая эксперименты с зажимом гипогликемии на здоровых добровольцах.J Clin Эндокринол Метаб 87: 1239 –1246, 2002
- ↵
Turton MD, O’Shea Д., Ганн И., Бик С.А., Эдвардс К.М., Миран К., Чой С.Дж., Тейлор Г.М., Хит М.М., Ламберт PD, Wilding JP, Smith DM, Ghatei MA, Herbert J, Bloom SR: роль для глюкагоноподобный пептид-1 в центральной регуляции питания. Природа 379: 69 –72, 1996
- ↵
Zander M, Мадсбад S, Madsen JL, Holst JJ: Влияние 6-недельного курса глюкагоноподобного пептида 1 на гликемический контроль, чувствительность к инсулину и функция бета-клеток при типе 2 диабет: исследование в параллельных группах.Ланцет359 : 824–830,2002
- ↵
Drucker DJ: Глюкагоноподобные пептиды: регуляция пролиферации, дифференцировки и дифференцировки клеток. апоптоз. Мол эндокринола 17: 161 –171, 2003
- ↵
Аткинсон, Массачусетс, Макларен Н.К .: Патогенез инсулинозависимого сахарного диабета. N Engl J Med 331: 1428 –1436, 1994
- ↵
Kruger DF, Gatcomb ПМ, Оуэн СК: Клинические последствия амилина и дефицита амилина. Диабетическое образование 25: 389 –397, 1999
- ↵
Kahn SE: The важность бета-клеток в патогенезе сахарного диабета 2 типа.Am J Med 108: 2S –8S, 2000
- ↵
Toft-Nielsen MB, Дамхольт М.Б., Мадсбад С., Хильстед Л.М., Хьюз Т.Э., Михельсен Б.К., Холст Дж.Дж.: Детерминанты нарушения секреции глюкагоноподобного пептида-1 при типе 2 пациенты с диабетом. J Clin Endocrinol Metab86 : 3717–3723,2001
- ↵
Horowitz M, Edelbroek MA, Wishart JM, Straathof JW: Взаимосвязь между пероральной глюкозой толерантность и опорожнение желудка у нормальных здоровых людей. Диабетология 36: 857 –862, 1993
- ↵
Зинман Б., Цуй EYL: Альтернативные пути доставки инсулина.В международном Учебник по сахарному диабету. 2-е изд. Альберти КГММ, Zimmet P, Defronzo RA, Eds. Нью-Йорк, Джон Вили и сыновья, 1997, стр.929. –936
- ↵
Jacobs MA, Keulen ET, Kanc K, Casteleijn S, Scheffer P, Deville W, Heine RJ: Метаболическая эффективность препрандиального введения аналога человеческого инсулина Lys (B28), Pro (B29) в Пациенты с ИЗСД: сравнение с обычным человеческим инсулином во время трехразового приема пищи тестовый период. Уход за диабетом 20: 1279 –1286, 1997
Heinemann L, Heise T, Wahl LC, Trautmann ME, Ampudia J, Starke AA, Berger M: Прандиальная гликемия после приема пищи, богатой углеводами, у пациентов с диабетом I типа: использование быстрого действующий аналог инсулина.Диабет Мед13 : 625–629,1996
- ↵
Bruttomesso D, Пианта А., Мари А., Валерио А., Марескотти М.С., Авогаро А., Тиенго А., Дель Прато С. Восстановление раннего повышения уровня инсулина в плазме улучшает глюкозу толерантность больных сахарным диабетом 2 типа. Диабет48 : 99–105,1999
- ↵
Jiang G, Zhang BB: Глюкагон и регуляция метаболизма глюкозы. Am J Physiol Эндокринол Метаб 284: E671 –E678, 2003
- ↵
Purnell JQ, Hokanson JE, Marcovina SM, Steffes MW, Cleary PA, Brunzell JD: Эффект чрезмерное увеличение веса при интенсивной терапии сахарного диабета 1 типа по липидам уровни и артериальное давление: результаты DCCT.JAMA280 : 140–146,1998
- ↵
Kreymann B, Williams G, Ghatei MA, Bloom SR: глюкагоноподобный пептид-17-36: физиологический инкретин в человеке. Ланцет 2: 1300 –1303, 1987
- ↵
Holst JJ: Глюкагоноподобный пептид 1: недавно открытый желудочно-кишечный гормон. Гастроэнтерология 107: 1848 –1855, 1994
- ↵
Друкер Д: Усиление действия инкретина для лечения диабета 2 типа. Уход за диабетом 26: 2929 –2940, 2003
- ↵
Исследовательская группа DCCT: Влияние интенсивная терапия сахарного диабета на развитие и длительное прогрессирование осложнения при инсулинозависимом сахарном диабете.N Engl J Средний 329: 977 –986, 1993
- ↵
Klein R, Klein BE, Мосс С.Е., Круикшенкс К.Дж.: Медицинское лечение гипергликемии в течение 10-летний период у людей с сахарным диабетом. Уход за диабетом19 : 744–750,1996
Почему жиры, а не углеводы, являются предпочтительным топливом для человеческого тела
Есть веская причина, по которой так много людей (в основном сжигателей сахара, разрозненная группа которых включает фрукторианцев, веганов, HEDers, бодибилдеров, большинство MD, Министерство сельского хозяйства США и практически все программы RD в стране), похоже, не могут понять, почему низкоуглеводный подход к еде — лучший выбор для здоровья и фитнеса: их фундаментальная парадигма — основная теория, лежащая в основе всего остального в этой системе убеждений — ошибочна.Они остаются рабами устаревшего представления о глюкозе как о короле топлива, поэтому живут в страхе, что у них кончится. По правде говоря, жир является предпочтительным топливом для метаболизма человека и был на протяжении большей части эволюции человека. В нормальных человеческих условиях нам на самом деле требуется лишь минимальное количество глюкозы, большая часть или вся она может поступать через печень по мере необходимости на ежедневной основе. Тот простой факт, что углеводы / глюкоза настолько легкодоступны и дешевы сегодня, не означает, что мы должны полагаться на них как на основной источник топлива или уважать их так высоко.Фактически, именно эта слепая приверженность «парадигме углеводов» заставила многих из нас испытать огромное количество метаболических проблем, которые угрожают сокрушить нашу систему здравоохранения.
Мне непонятно, что такой большой сегмент так называемого сообщества здоровья и фитнеса будет продолжать защищать высокоуглеводные диеты с таким упорством. К настоящему времени все должно быть очень очевидно. Исследования продолжают накапливаться, указывая на то, что потребление углеводов является основной переменной, определяющей состав тела, и что избыток глюкозы в результате потребления углеводов (особенно из обработанного зерна и сахара) является основной причиной ожирения и многих заболеваний.Из этого логически следует, что, если вы можете ограничить потребление углеводов до диапазона, который абсолютно необходим (и даже до 50 граммов в день больше), и восполнить разницу вкусными жирами и белками, вы можете буквально перепрограммировать свои гены обратно на эволюционный уровень. — заводские настройки, которые были у вас при рождении — настройки, которые давали вам возможность начать жизнь как действительно эффективный организм, сжигающий жир, и продолжать делать это до конца своей жизни, пока вы посылаете правильные сигналы своим генам .Стать эффективным сжигателем жира — основная предпосылка стратегии питания и упражнений Primal Blueprint.
Но логика не управляет, когда вы застряли в углеводной парадигме, поэтому я все еще вижу некоторых заблуждающихся блоггеров, осуждающих стратегию питания Primal Blueprint как потенциально вредную из-за ее относительно низкого потребления углеводов или заявляющих, что мой совет «обычно держите углеводы ниже 150 граммов в день, если вы не спортсмен »- это смешно. Сколько еще раз мне придется подслушивать тренера, который советует здоровому клиенту «есть 5 или 6 небольших приемов пищи в течение дня, всегда с небольшим количеством углеводов, чтобы поддерживать уровень сахара в крови и не переходить в режим голодания».»? Пора прекратить эту чушь и переосмыслить нынешние взгляды на метаболизм человека, чтобы точно отразить два с половиной миллиона лет эволюции, которые сформировали нынешний геном человека — идеальный рецепт ДНК, который полностью предполагает, что мы с рождения будем функционировать в основном за счет жиров.
Пришло время изменить метаболическую парадигму в мире здоровья и фитнеса.«Логика» ошибочной углеводной парадигмы выглядит примерно так
Основное предположение состоит в том, что глюкоза является предпочтительным топливом для большинства клеток; НО, поскольку мы не можем хранить очень много глюкозы (в виде гликогена в печени и мышцах), нам необходимо обеспечить постоянный источник глюкозы в виде экзогенных углеводов (еда с высоким содержанием углеводов), чтобы поддерживать мозг, кровь и определенные органы. жужжание и мышцы готовы к активности.И, если мы не будем кормить себя достаточным количеством углеводов каждые несколько часов, уровень сахара в крови упадет, и мы перейдем в «режим голодания» и поглотим нашу драгоценную мышечную ткань. И любое отсутствие регулярного пополнения глюкозы (например, пропуск еды или голодания) вызовет повышение уровня кортизола, что будет иметь дополнительные пагубные последствия. БОЛЬШЕ, известно, что избыток глюкозы в кровотоке повышает уровень инсулина и предрасполагает к накоплению лишних калорий (из всех источников) в виде жира. ПОЭТОМУ, мы также должны делать много умеренных и тяжелых кардио-нагрузок или силовых упражнений большую часть дней, чтобы сжечь этот лишний накопленный жир.ОДНАКО, если мы хотим быть готовы и иметь возможность часто и усиленно тренироваться, чтобы сжигать накопленный жир, нам нужно есть много сложных углеводов между тренировками, чтобы пополнить запасы гликогена. И ИСКЛЮЧИТЕЛЬНО, единственный способ похудеть — это ограничить количество калорий (количество калорий меньше калорий), НО если вы тренируетесь регулярно, почти невозможно поддерживать режим с ограничением калорий и при этом иметь возможность тренироваться достаточно усердно, чтобы сжигать заметные калории. Блин.
Конечно, есть исключения, такие как целеустремленные и генетически одаренные типы, которые могут тренироваться много часов, заправляться углеводами и не прибавлять много жира (эй, я был одним из них).Но если вы не любите постоянно заниматься спортом и у вас действительно счастливые семейные гены, Carb Paradigm — это неустойчивая и нелепая беговая дорожка в прямом и переносном смысле , самореализующееся пророчество для большинства людей, которые с годами склонны постепенно и коварно набирать вес. Интересно, почему. Если вы относитесь к 60% населения США с избыточным весом, описанный выше сценарий проигрывает, потому что вы всю жизнь программировали свои гены в направлении эффективного сжигания сахара и, как следствие, стали зависимыми. на свежий сахар (углеводы) каждые несколько часов.Естественно, в присутствии всей этой глюкозы и при условии, что вы действительно занимаетесь спортом, ваши гены в конечном итоге получат сигналы для активации ферментных систем, путей и рецепторов, участвующих в сжигании сахара и хранении жира , и они будут подавляют всех, кто участвует в доступе и сжигании жира для получения энергии. Конечно, не дает правильного ответа, но создает впечатление, будто глюкоза — король . Что еще хуже, если вы не занимаетесь спортом, вы идете по пути к инсулинорезистентности и / или ожирению.
Проблема: основное предположение парадигмы углеводов неверно
Глюкоза не является предпочтительным топливом для мышечных клеток при нормальных метаболических условиях покоя человека или даже при большинстве нормальных моделей движений человека (физических упражнений). Жир есть. Конечно, учитывая неограниченный запас глюкозы и регулярное пополнение запасов гликогена, скелетные мышцы будут прожигать его во время упражнений так же, как огонь горит от растопки, когда это все, что вы можете предложить. Организм может сдвинуть процесс окисления углеводов, чтобы не отставать от потребления.Но скелетные мышцы могут сжигать жир с большой эффективностью (и с гораздо меньшими окислительными выбросами) при относительно высокой производительности в течение очень длительных тренировок. Сердечная мышца на самом деле предпочитает кетоны, и мозг может нормально работать (возможно, даже оптимально) на смеси кетонов и минимальном количестве глюкозы. Наше выживание как вида зависело от этих эволюционных адаптаций вдали от зависимости от глюкозы. Целые цивилизации веками существовали на практически безуглеводной диете. Подумайте об этом: на самом деле нет потребности в каких-либо «основных диетических углеводах» в питании человека . Можно прожить очень долгую и здоровую жизнь, никогда не потребляя много углеводов, если они вообще есть, при условии, что вы получаете достаточное количество белков и жиров с пищей. Чего нельзя сказать о долгом отсутствии белка или жира. Слишком сократите потребление любого из этих макроэлементов, и в конечном итоге вы заболеете и умрете.
Эволюционная модель
Жиры и белки были доминирующими макроэлементами (когда пища была даже доступна) на протяжении большей части наших двух с половиной миллионов лет развития человека.Отсутствие регулярного доступа к пище и дефицит углеводов в течение большей части этого времени потребовали, чтобы мы адаптировали эффективные пути для быстрого хранения и доступа к телу для получения энергии, если мы хотим выжить изо дня в день и из поколения в поколение. Наши двигательные паттерны были таковы, что нам никогда не требовалось большое количество глюкозы или нам нужно было хранить очень много гликогена. Это были преимущественно жиры, кетоны и минимальное вливание глюкозы посредством глюконеогенеза. Углеводы в рационе были незначительными. На самом деле, когда вы рассматриваете, насколько до смешного малы резервуары гликогена в организме, вы понимаете, что для нас было бы невозможно выжить как биологический вид, если бы глюкоза была действительно «предпочтительным» топливом. Печень, основное резервное хранилище гликогена / глюкозы для мозга и других органов, сжигающих глюкозу, может хранить только около 100 граммов гликогена. Стоит меньше суток. Ваши мышцы могут удерживать только 350-500 граммов, чего едва хватает, чтобы работать в течение 90 минут с разумной нагрузкой, а этот гликоген даже не доступен для питания мозга.Между тем, у нас есть практически неограниченные возможности для хранения жира (например, 100 000 граммов или около миллиона калорий для некоторых людей). Причина, по которой в хранении гликогена не было необходимости, заключается в том, что между нашей способностью к обильному хранению жира, легким доступом к жирам в качестве топлива, глюконеогенезом и кетонами нам просто не нужно было много. Эволюция, как правило, не вознаграждает структуры или функции, которые занимают ненужное пространство или тратят энергию.
Итак, сколько глюкозы вам действительно нужно?
Намного меньше, чем думает большинство людей.В любой момент общее количество глюкозы, растворенной в кровотоке здорового человека, не страдающего диабетом, эквивалентно одной чайной ложке (может быть, 5 граммов). Гораздо более токсично; гораздо меньше, и вы теряете сознание. Это не так много для так называемого «предпочтительного» топлива, не так ли? Несколько исследований показали, что при нормальных условиях низкого МЕТ (в состоянии покоя или от низкого до среднего уровня активности, такой как ходьба и легкая работа) организму требуется всего около 5 граммов глюкозы в час. И это для людей, которые еще не адаптированы к жирам или кето.Мозг является основным потребителем глюкозы, и людям, которые еще не соблюдают низкоуглеводную диету, требуется около 120 граммов в день. Низкоуглеводное питание значительно снижает потребности мозга в глюкозе, и тем, кто имеет очень низкий уровень углеводов (VLC) и кето-адаптирован, может потребоваться всего около 30 граммов глюкозы в день для подпитки мозга (и совсем немного для подпитки мышц. <75% максимальных усилий). Двадцать из этих граммов могут быть получены из глицерина (побочный продукт метаболизма жиров), а баланс - за счет глюконеогенеза в печени (который на самом деле может составлять до колоссальных 150 граммов в день, если вы не повредили его метаболически НАЖБП из-за передозировки фруктозы) .В итоге, если вы не занимаетесь физическим трудом или не тренируетесь (тренируетесь) усердно на ежедневной основе, после того, как вы станете адаптироваться к жирам, вам, вероятно, никогда не понадобится потреблять более 150 граммов диетических углеводов - и вы, вероятно, сможете процветать. на гораздо меньше. Многие спортсмены-спортсмены очень хорошо справляются (включая тренировки) с 30-70 граммами в день.
Толстая парадигма
Жирная парадигма, согласно которой человеческий вид достаточно эффективно процветал в течение двух с половиной миллионов лет, признает, что человеческий метаболизм запрограммирован эволюцией в основном на жировую основу (реальное предпочтительное топливо) .Другими словами, наши гены ожидают, что мы будем оптимально функционировать, когда мы потребляем жиры, и можем легко получить доступ к нашим накопленным жирам. Жирная парадигма признает, что организм способен производить адекватную глюкозу по мере необходимости. Он признает, что большинство типичных моделей движений человека могут почти полностью подпитываться жирами и / или кетонами (PDF), если это необходимо, но могут потреблять гликоген, когда требуются всплески энергии (и которые затем могут быть заменены со временем). Он признает, что жир (и холестерин) не являются непосредственной причиной сердечных заболеваний.Он признает, что жировые клетки предназначены для высвобождения накопленных жирных кислот по мере необходимости, особенно в периоды дефицита или голодания. Это позволяет использовать периодическое голодание как средство ускорения потери жира без ущерба для мышечной ткани. Он повышает чувствительность к инсулину, регулирует перепады энергии и настроения, а также способствует нормальному и здоровому снижению голода и тяги. Существует обратная сторона, однако, вы не можете тренироваться долго и упорно изо дня в день и из-парадигмы жира.
Итак, объяснив все это, поймите, пожалуйста, что я не карбобоязнь. Я на самом деле разрешаю больше углеводов в Primal Blueprint, чем многие другие стратегии низкоуглеводного питания. Я предпочитаю рассматривать углеводы как «выборные» макроэлементы, как инструмент, который можно использовать для управления уровнем гликогена по мере необходимости. Низкое содержание углеводов даже не является главной целью употребления пищи в ПБ: исключение зерен, сахара и масел из семян семян является главной целью. Конечно, когда вы избавляетесь от этого дерьма и естественным образом ограничиваете потребление углеводов овощами, корневыми клубнями и некоторыми фруктами, вы почти всегда уменьшаете количество углеводов до менее 150 граммов в день.И это имитирует диетическое питание наших предков.
Несколько лет назад я придумал простую кривую углеводов, которая дает довольно краткую картину того, куда должно падать большинство людей, если они ищут оптимальное здоровье и энергию, в зависимости от их размера, веса, пола, возраста, целей и т. Д. Теперь, спустя многие сотни тысяч пользовательских опытов, я обнаружил, что Curve в значительной степени подходит для значительной части населения.
Когда я обычно говорю, что постоянное потребление более 150 граммов углеводов может привести к коварному увеличению веса в течение всей жизни, я учитываю концепцию, что многие люди находятся под влиянием наследственной генетической предрасположенности к легкому накоплению жира под углеводами парадигма (60 +% лишнего веса).Я также принимаю во внимание снижение метаболизма, которое происходит естественным образом с возрастом, а также тот факт, что ПБ не НУЖНО очищать и пополнять запасы гликогена каждый день с помощью упражнений. Да, есть люди (небольшой процент отклоняющихся от нормы), которые могут поддерживать довольно приличный состав тела — до 300 граммов в день при небольших физических нагрузках. Могу поспорить, что они также избирательно подходят к источникам углеводов и лучше справляются с контролем общего количества калорий, так что излишков немного. Для большей части населения эти 150 баллов остаются хорошим средним уровнем для поддержания идеального телосложения.
Что ж, сегодня было много чего переварить. Вы видите, к чему я клоню. Мне нужна ваша помощь, чтобы показать медицинскому сообществу, что их основные предположения ошибочны и что им необходимо изменить метаболическую парадигму. Я уверен, что будет много конкретных вопросов, так что задайте их, и я напишу следующий пост через неделю или две.
Вам также может понравиться:
Полное руководство по маслам
Собираюсь кето: что есть
Убьет ли насыщенный жир ваши клетки?
Возьмите масло авокадо Primal Kitchen, чтобы добавить в свой рацион жир.
об авторе
Марк Сиссон — основатель Mark’s Daily Apple, крестный отец движения Primal Food and lifestyle и автор бестселлеров New York Times The Keto Reset Diet . Его последняя книга — Keto for Life , где он обсуждает, как он сочетает кето-диету с основным образом жизни для оптимального здоровья и долголетия. Марк также является автором множества других книг, в том числе The Primal Blueprint , которому приписывают ускорение роста движения Primal / Paleo еще в 2009 году.Проведя три десятилетия в изучении и обучении людей тому, почему еда является ключевым компонентом достижения и поддержания оптимального самочувствия, Марк основал Primal Kitchen, компанию по производству настоящих продуктов питания, которая создает основные продукты для кухни Primal / paleo, keto и Whole30.
сообщение навигации
Если вы хотите добавить аватар ко всем своим комментариям, нажмите здесь!
Влияние разного количества углеводов на метаболизм после похудания | Источник питания
Похудение — тяжелая работа, но многие люди, которые похудели, могут согласиться с тем, что снижение веса может быть еще более сложной задачей.Недостаток самоконтроля или слишком большое количество диетических поблажек часто называют причинами набора веса. Но новое исследование в ноябрьском выпуске BMJ ставит под сомнение эту традиционную точку зрения, обнаружив, что тип потребляемых вами калорий может влиять на вероятность того, что вы сохраните этот вес в долгосрочной перспективе. [1]
Человеческое тело спроектировано так, чтобы защищать себя, когда оно худеет, добровольно или непроизвольно, вызывая повышенное желание есть и замедляя метаболизм, в то же время более эффективно накапливая жир.Хотя может быть захватывающе видеть падение веса на весах, способность продолжать худеть или даже поддерживать любую потерю веса становится труднее, потому что тяга к еде возрастает, в то время как организм с большей готовностью откладывает эти калории в виде жира.
Целью исследования BMJ было выяснить, могут ли различные уровни углеводов в рационе предотвратить эти метаболические изменения, чтобы можно было избежать потери веса. Внимание к углеводам было основано на «углеводно-инсулиновой модели» ожирения, которая утверждает, что высокий уровень инсулина является результатом диеты с высокой гликемической нагрузкой (т.е.д., сильно переработанные углеводы, такие как рафинированный хлеб, крекеры, печенье и сахар) заставляют энергию из пищи легче накапливаться в виде жира и могут усиливать голод и тягу к еде, снижать расход энергии и способствовать увеличению веса.
Кабинет
Участники сначала были помещены на диету для снижения веса, чтобы сбросить около 12% от их начального веса (потеря веса составила в среднем 25 фунтов), чтобы дать толчок метаболическим изменениям. На следующем этапе 164 участника, достигших этой потери веса, были случайным образом распределены в одну из трех тестовых групп:
.- диета с высоким (60%) содержанием углеводов и низким (20%) содержанием жиров
- умеренная (40%) углеводная и (40%) жирная диета
- диета с низким (20%) содержанием углеводов и высоким (60%) содержанием жиров
Количество белка было одинаковым во всех группах и составляло 20%.Общее количество калорий было скорректировано в большую или меньшую сторону, чтобы предотвратить любые изменения веса у каждого участника. Все блюда были предоставлены участникам во время фазы похудания и в течение 20-недельной фазы тестирования. Типы продуктов в каждой диетической группе были разработаны так, чтобы быть максимально похожими, но различающимися по количеству: группа с высоким содержанием углеводов ела больше цельнозерновых, фруктов, бобовых и молочных продуктов с низким содержанием жира. Напротив, группа с низким содержанием углеводов ела больше жиров, но исключила все зерновые, а также некоторые фрукты и бобовые.
Участники соблюдали диету в течение 20 недель и измеряли общий расход энергии. В течение 20 недель участники во всех группах сохраняли свой вес, и была минимальная разница во вторичных показателях, включая физическую активность и расход энергии в покое (факторы, которые могли независимо увеличивать общий расход энергии).
Выводы
- Группа с низким содержанием углеводов показала повышенный расход энергии на 209–278 калорий в день по сравнению с группой с высоким содержанием углеводов.Группа с умеренным содержанием углеводов показала меньшее увеличение расхода примерно на 100 калорий по сравнению с группой с высоким содержанием углеводов. Эта тенденция сохранялась на протяжении 20-недельного периода.
- Повышенный метаболический эффект от низкоуглеводной диеты был наиболее значительным у людей с высокой секрецией инсулина в начале исследования, с повышенным расходом энергии в диапазоне 308-478 калорий / день. (Люди с высокой секрецией инсулина, как правило, имеют форму скорее «яблоки», чем «груши», поскольку избыток жира откладывается преимущественно в средней части тела.Этот вывод подтверждает недавнее исследование, которое предполагает, что различия в биологии могут повлиять на то, как люди реагируют на диеты для похудения в долгосрочной перспективе.
- Гормон, повышающий аппетит, грелин, значительно снизился на низкоуглеводной диете, что может помочь в поддержании потери веса. Другой гормон, регулирующий аппетит, лептин, также снизился. Лептин регулирует энергетический баланс и поддерживает стабильную массу тела. Обычно он противодействует грелину, посылая в мозг сигналы о подавлении аппетита, когда организм получает достаточно еды.Раньше считалось, что высокий уровень лептина снижает аппетит и заставляет организм использовать накопленный жир для получения энергии. Однако некоторые формы ожирения / избыточного веса могут привести к «резистентности к лептину», когда в организме высокий уровень лептина. В этом сценарии мозг не получает предупреждения о том, что уровень лептина уже высок, поэтому он продолжает посылать сильные сигналы голода, сохраняя при этом запасы жира. Другими словами, высокий уровень лептина может способствовать устойчивости к лептину. Его значение в исследовании BMJ заключалось в том, что диета с низким содержанием углеводов, по-видимому, улучшает чувствительность к лептину за счет снижения высоких уровней лептина.
«Это исследование повышает вероятность того, что сосредоточение внимания на ограничении углеводов, а не калорий, может лучше работать для долгосрочного контроля веса», — сказал д-р Дэвид Людвиг, профессор кафедры питания Гарвардского университета T.H. Chan School of Public Health, которая провела исследование с доктором Кара Эббелинг из Бостонской детской больницы.
Доктор Уолтер Уиллетт, профессор эпидемиологии и питания в Гарвардской школе Чана, который не участвовал в исследовании, также отметил, что «эти результаты тщательно проведенного исследования могут помочь объяснить, почему диеты с низким содержанием жиров и высоким содержанием углеводов неэффективны для большинство людей и не смогли поддерживать потерю веса в формальных рандомизированных испытаниях, которые длились один год или дольше.”
Связанные
В обзоре, опубликованном в журнале Science на той же неделе, что и исследование BMJ , доктор Людвиг обсудил разногласия по поводу конкретного соотношения жиров и углеводов для поддержания здорового веса и снижения риска заболеваний. [2] Он, д-р Уиллетт и другие эксперты в этой области согласились с тем, что, сосредоточив внимание в основном на качестве диеты — заменяя насыщенные или трансжиры ненасыщенными и заменяя рафинированные углеводы цельнозерновыми и некрахмалистыми овощами, — большинство людей может сохранить хорошее здоровье в пределах нормы. широкий диапазон соотношения жиров и углеводов.Подробнее читайте на странице Диетический жир — это хорошо? Диетический жир — это плохо? Приходим к консенсусу.
Ссылки- Ebbeling CB, Feldman HA, Klein GL, Wong JMW, Bielak L, Steltz SK, Luoto PK, Wolfe RR, Wong WW, Ludwig DS. Влияние низкоуглеводной диеты на расход энергии при сохранении веса: рандомизированное исследование. BMJ. 14 ноября 2018 г .; 363: k4583. * Раскрытие информации: эта работа была проведена на средства гранта Nutrition Science Initiative. Инициатива по науке о питании следила за ходом исследования и получила возможность прокомментировать рукопись.
- Людвиг, Д. С., Виллет, В. К., Волек, Дж. С., и Нойхаузер, М. Л. (2018). Диетический жир: от врага к другу ?. Наука , 362 (6416), 764-770.
Потребление энергии, метаболический гомеостаз и здоровье человека
Энергетические вещества (в основном углеводы и жиры) являются основой и гарантией жизнедеятельности, особенно окислительного фосфорилирования для обеспечения энергии. Однако чрезмерное всасывание и накопление этих веществ может привести к метаболическим заболеваниям, таким как ожирение, гиперлипидемия, диабет и рак.Большое количество исследований демонстрирует, что рецепторы, связанные с G-белками (GPCR), играют ключевую роль в идентификации и абсорбции энергетических веществ, а сигнальная сеть нервов, иммунной и эндокринной системы регулирует их хранение и использование. Слой слизи желудочно-кишечного тракта не только идентифицирует эти вещества посредством идентификации в компонентах диеты, но также передает иммунные, метаболические и эндокринные сигналы гормонов, цитокинов и хемокинов, способствуя взаимодействию между рецепторами и лигандами.Эти сигнальные молекулы передаются в соответствующие органы, ткани и клетки кровеносной системой, а активность клеток регулируется путем усиления клеточных сигналов, которые составляют сеть беспроводной связи между клетками в организме. Поглощение, накопление и использование энергетических веществ в организме подчиняются закону сохранения энергии. Энергия накапливается в виде жира и удовлетворяет потребности организма посредством двух связанных механизмов : катаболизма и окислительного фосфорилирования.В нормальных физиологических условиях потребление жиров включает метаболизм кетоновых тел через систему кровообращения, а потребление глюкозы требует цикла молочной кислоты в крови. Накопление избыточной энергии приводит к аномальной активации рапамицина (mTOR) у млекопитающих, что способствует выведению глюкозы или гликогена в виде глюкозы в крови и глюкозы в моче.


 в день)
в день)



 При распаде опухоли в кровь попадают чужеродные белки, вызывающие отравление организма. Это может приводить к снижению аппетита и к алиментарной углеводной недостаточности. Кроме того, некоторые опухоли способны производить вещества, воспринимаемые организмом как инсулин.
При распаде опухоли в кровь попадают чужеродные белки, вызывающие отравление организма. Это может приводить к снижению аппетита и к алиментарной углеводной недостаточности. Кроме того, некоторые опухоли способны производить вещества, воспринимаемые организмом как инсулин. Проинсулин – белок – предшественник инсулина и в значительном количестве может определяться в крови пациентов с инсулиномой, гипогликемией, почечной и печеночной недостаточностью.
Проинсулин – белок – предшественник инсулина и в значительном количестве может определяться в крови пациентов с инсулиномой, гипогликемией, почечной и печеночной недостаточностью. Выявление мутации C(-13910)T (регуляторная область гена). Исследование может быть назначено при подозрении на врождённый недостаток лактазы – пищеварительного фермента, обеспечивающего усвоение молочного сахара в желудочно-кишечном тракте. Представляет собой генетический анализ на измененные гены в соскобе щечной области. Положительный тест позволяет отличить врождённый дефицит фермента от приобретенных нарушений усвоения углеводов, как, например, при дисбактериозе.
Выявление мутации C(-13910)T (регуляторная область гена). Исследование может быть назначено при подозрении на врождённый недостаток лактазы – пищеварительного фермента, обеспечивающего усвоение молочного сахара в желудочно-кишечном тракте. Представляет собой генетический анализ на измененные гены в соскобе щечной области. Положительный тест позволяет отличить врождённый дефицит фермента от приобретенных нарушений усвоения углеводов, как, например, при дисбактериозе. Ультразвук проходит сквозь мягкие ткани до исследуемого органа и, отразившись, возвращается обратно. Полученное изображение передается на монитор. Исследование позволяет оценить размеры указанных органов, структуру тканей, выявить опухолевое поражение или кисту, исключить наличие жидкости в брюшной полости. При необходимости исследование может быть дополнено взятием биопсии под УЗИ-контролем.
Ультразвук проходит сквозь мягкие ткани до исследуемого органа и, отразившись, возвращается обратно. Полученное изображение передается на монитор. Исследование позволяет оценить размеры указанных органов, структуру тканей, выявить опухолевое поражение или кисту, исключить наличие жидкости в брюшной полости. При необходимости исследование может быть дополнено взятием биопсии под УЗИ-контролем.