Синтез гликогена (гликогенез). «БИОЛОГИЧЕСКАЯ ХИМИЯ», Березов Т.Т., Коровкин Б.Ф.
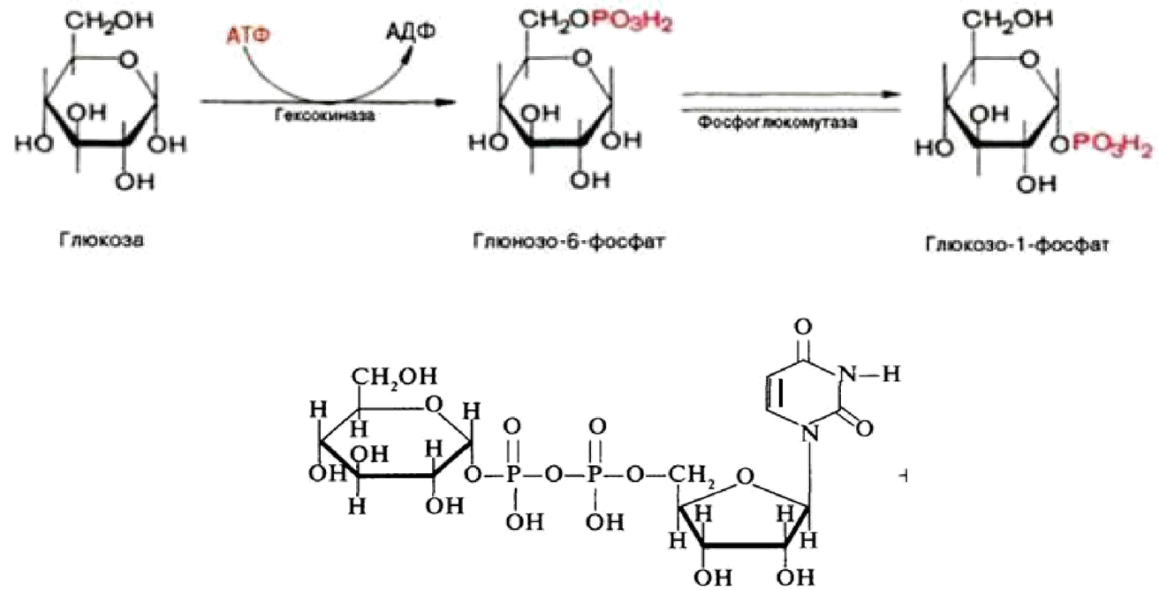
Прежде всего глюкоза подвергается фосфорилированию при участии фермента гексокиназы, а в печени – и глюкокиназы. Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фос-фат:
Образовавшийся глюкозо-1-фосфат уже непосредственно вовлекается в синтез гликогена. На первой стадии синтеза глюкозо-1-фосфат вступает во взаимодействие с УТФ (уридинтрифосфат), образуя уридиндифосфатглюкозу (УДФ-глюкоза) и пирофосфат. Данная реакция катализируется ферментом глюкозо-1-фосфат-уридилилтрансферазой (УДФГ-пирофосфорилаза):
Глюкозо-1-фосфат + УТФ < = > УДФ-глюкоза + Пирофосфат.
Приводим структурную формулу УДФ-глюкозы:
На второй
стадии – стадии образования гликогена – происходит перенос глюкозного остатка,
входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена («затравочное»
количество).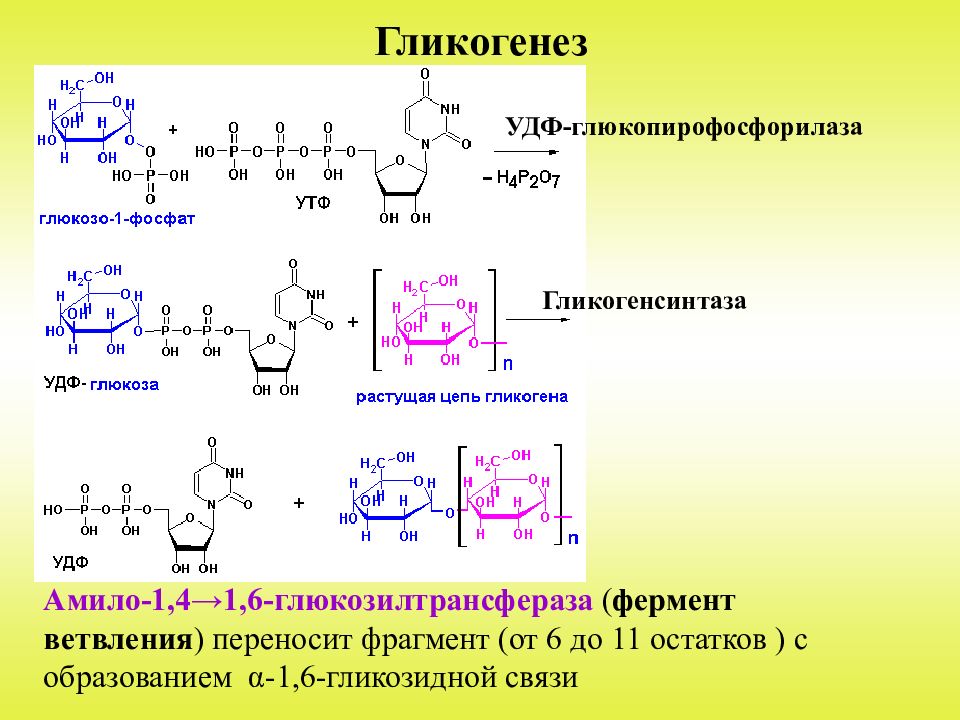
Образующийся УДФ затем вновь фосфорилируется в УТФ за счет АТФ, и таким образом весь цикл превращений глюкозо-1-фосфата начинается сначала.
В целом образование α-1,4-глюкозидной ветви («амилозной» ветви) гликогена можно представить в виде следующей схемы:
Установлено,
что гликогенсинтаза неспособна катализировать образование
α-(1–>6)-связи, имеющейся в точках ветвления гликогена. Этот процесс
катализирует специальный фермент, получивший название гли-когенветвящего
фермента, или амило-(1–>4)–>(1–>6)-трансглюкозидазы. Последний катализирует
перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков
глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее
11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи
гликогена. В результате образуется новая боковая цепь.
Последний катализирует
перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков
глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее
11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи
гликогена. В результате образуется новая боковая цепь.
Ветвление повышает растворимость гликогена. Кроме того, благодаря ветвлению создается большое количество невосстанавливающих концевых остатков, которые являются местами действия гликогенфосфорилазы и гликогенсинтазы.
Таким образом, ветвление увеличивает скорость синтеза и расщепления гликогена.
Благодаря
способности к отложению гликогена (главным образом в печени и мышцах и в
меньшей степени в других органах и тканях) создаются условия для накопления в
норме некоторого резерва углеводов. При повышении энерготрат в организме в
результате возбуждения ЦНС обычно происходят усиление распада гликогена и
образование глюкозы.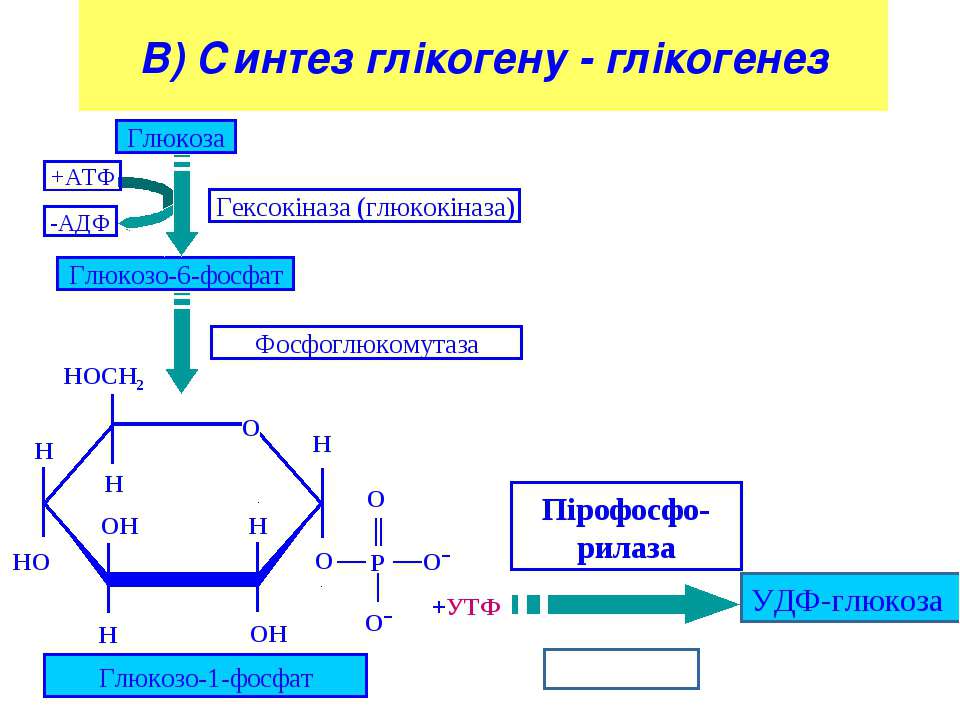
Помимо непосредственной передачи нервных импульсов к эффекторным органам и тканям, при возбуждении ЦНС повышаются функции ряда желез внутренней секреции (мозговое вещество надпочечников, щитовидная железа, гипофиз и др.), гормоны которых активируют распад гликогена, прежде всего в печени и мышцах (см. главу 8).
Как
отмечалось, эффект катехоламинов в значительной мере опосредован действием
цАМФ, который активирует протеинкиназы тканей. При участии последних происходит
фосфорилирование ряда белков, в том числе гликогенсинтазы и фосфорилазы b – ферментов, участвующих в обмене углеводов. Фосфорилированный
фермент гликогенсинтаза сам по себе малоактивен или полностью неактивен, но в
значительной мере активируется положительным модулятором глюкозо-6-фосфатом,
который увеличивает V Дефосфорилированная форма гликоген-синтазы, называемая также I-формой, или
независимой (independent) формой, активна и в отсутствие
глюкозо-6-фосфата.
Дефосфорилированная форма гликоген-синтазы, называемая также I-формой, или
независимой (independent) формой, активна и в отсутствие
глюкозо-6-фосфата.
Таким образом, адреналин оказывает двойное действие на обмен углеводов: ингибирует синтез гликогена из УДФ-глюкозы, поскольку для проявления максимальной активности D-формы гликогенсинтазы нужны очень высокие концентрации глюкозо-6-фосфата, и ускоряет распад гликогена, так как способствует образованию активной фосфорилазы а. В целом суммарный результат действия адреналина состоит в ускорении превращения гликогена в глюкозу.
Предыдущая страница | Следующая страница
СОДЕРЖАНИЕ
Гликогенез — словарь ветеринарных терминов — ВЦ Зоовет
Гликогенез — биохимическая реакция протекающая в основном в печени и мышцах в результате которой глюкоза превращается в гликоген.
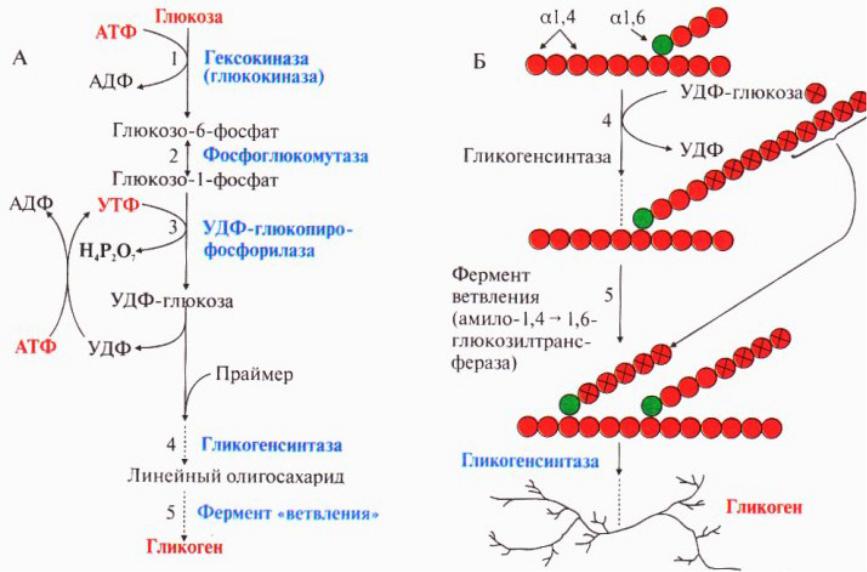
 Процесс гликогенеза, т.е. образование гликогена из глюкозы представляет собой процесс полимеризации, т.е происходит последовательное присоединение друг к другу мономеров глюкозы и образование полисахаридной цепи гликогена. Мышечный гликоген является источником глюкозы для самой мышечной клетки, а печеночный поддерживает физиологическую концентрацию глюкозы в крови.
Процесс гликогенеза, т.е. образование гликогена из глюкозы представляет собой процесс полимеризации, т.е происходит последовательное присоединение друг к другу мономеров глюкозы и образование полисахаридной цепи гликогена. Мышечный гликоген является источником глюкозы для самой мышечной клетки, а печеночный поддерживает физиологическую концентрацию глюкозы в крови.Возврат к списку
Гликогенез — Справочник химика 21
Гликогенез. Конечные продукты пищеварения углеводов — глюкоза, фруктоза и галактоза — диффундируют из пищеварительного тракта в воротную вену и попадают затем в печень. В результате различных превращений, протекающих с участием [c.382]
Опишите кратко гликогенез и гликогенолиз. Где происходят эти процессы [c.358]
Синтез гликогена (гликогенез) [c.322]
Гликогенез происходит в печени и в клетках мышц, как показано на схеме [c.
Снижение уровня сахара в крови, регуляция углеводного обмена, влияние на белковый и липидный обмен Повышение уровня сахара в крови стимуляцией гликогенеза в печени [c.239]
При отравлении стимулируется гликогенолиз и угнетается гликогенез, что обусловливает гипергликемию. Содержание Л. в печеночной ткани значительно снижается, угнетается активность альдолазы, активируется лактатдегидрогеназа, уменьшается концентрация пировиноградной кислоты, увеличивается уровень молочной кислоты. Содержание холестерина и р-липо-протеидов увеличивается изменяется баланс электролитов в крови, внутренних органах и структурах ЦНС в крови увеличивается концентрация пиридиннуклеотидов, содержание их в печени уменьшается, что связано с повреждающим действием иона Л. на никотинамидные ферменты в тканях нарушаются функции сердца и почек.
Избыток глюкозы накапливается в организме в виде гликогена, который образуется в результате процесса, называемого гликогенезом.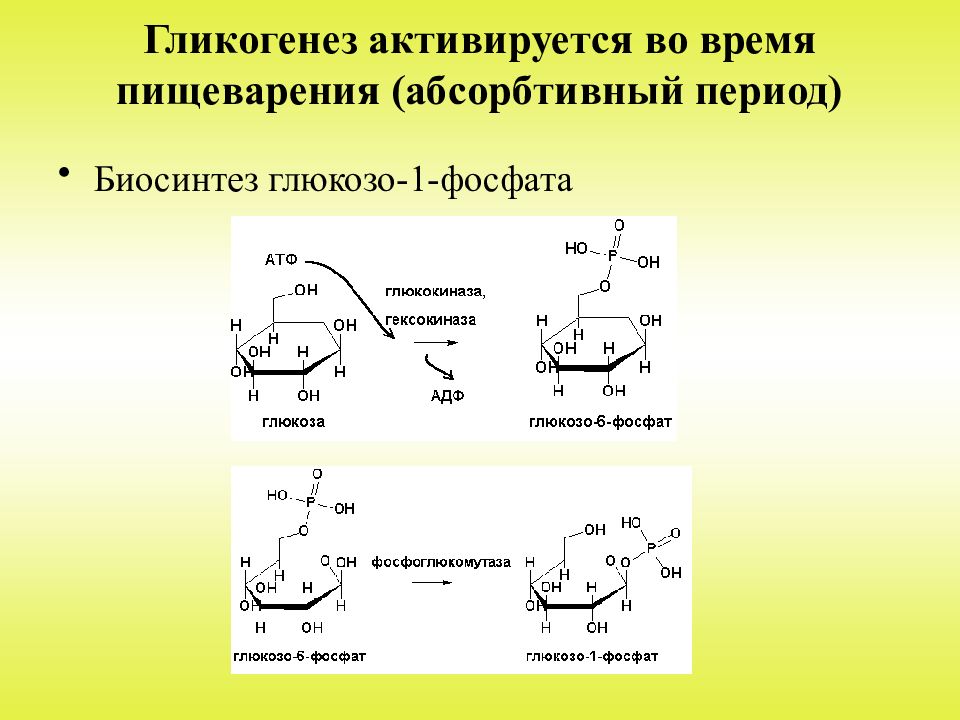 Остатки глюкозы (х= 12—18) конденсируются с выделением молекул воды, образуя гликоген по общей схеме [c.327]
Остатки глюкозы (х= 12—18) конденсируются с выделением молекул воды, образуя гликоген по общей схеме [c.327]
Цикл Кори. Гликогенез, гликогенолиз, гликолиз и лимоннокислый цикл связаны между собой (фиг. 105). Вся совокупность этих взаимоотношений называется циклом Кори. [c.383]
Поддерживание определенного уровня сахара крови — глюкозная толерантность — зависит от строгой регуляции интенсивности гликогенолиза, гликогенеза и окисления глюкозы. [c.388]
Две первые стадии гликогенолиза обратны двум последним стадиям гликогенеза. Глюкоза поступает в кровь из печени, так как в печени содержится основное количество фосфорилазы — фермента, катализирующего гидролиз гликогена. В мышечных клетках гликоген не гидролизуется, так как содержание в них фосфорилазы очень незначительно. [c.328]
Сахарный диабет — это болезнь, вызываемая недостаточностью инсулина в организме. Экспериментальные данные показывают, что инсулин регулирует скорость проникновения глюкозы внутрь клеток и защищает гексокиназу от ингибиторов (специфических ядов), благодаря чему глюкоза может быть фосфорилирована в глюкозо-6- сфат.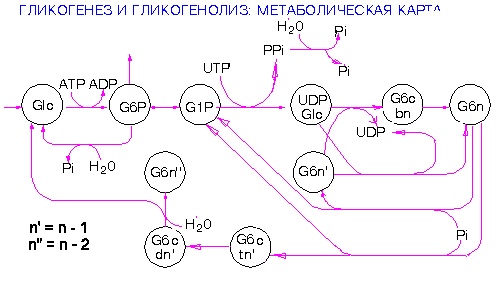 Это одна из важнейших реакций гликогенеза. [c.352]
Это одна из важнейших реакций гликогенеза. [c.352]
Низкое содержание сахара в крови может быть обусловлено чрезмерным гликогенезом, недостаточным глико-генолизом или какими-либо другими причинами, к которым относятся [c.353]
Избыточная глюкоза, поступившая при всасывании, откладывается в печени в виде запасного гликогена. В нормальных условиях этот орган содержит около 100 г гликогена, но его может накапливаться и до 400 г. Гликоген печени легко превращается в глюкозу, поэтому он является резервом, за счет которого организм получает глюкозу, если ее содержание в крови падает ниже нормального. Образование гликогена из глюкозы называется гликогенезом, а превращение гликогена в глюкозу — гликогенолизом. Мышцы также способны накапливать глюкозу в виде гликогена, но мышечный гликоген превращается в глюкозу не так легко, как гликоген печени. [c.365]
Гликогенез. Процесс гликогенеза — это не простое превращение глюкозы в гликоген. Как мы видели [c.365]
Как мы видели [c.365]
В норме примерно половина поглощенной глюкозы вступает на путь гликолиза и превращается в энергию, другая половина запасается в виде жиров или гликогена. В отсутствие инсулина ослабевает интенсивность гликолиза и замедляются анаболические процессы гликогенеза и липогенеза. Действительно, [c.256]
Эффекты глюкагона, как правило, противоположны эффектам инсулина. Если инсулин способствует запасанию энергии, стимулируя гликогенез, липогенез и синтез белка, то глюкагон, стимулируя гликогенолиз и липолиз, вызывает быструю мобилизацию источников потенциальной энергии с образованием глюкозы и жирных кислот соответственно. Глюкагон— наиболее активный стимулятор глюконеогенеза кроме того, он обладает и кетогенным действием. [c.264]
Глюкозо-6-фосфат занимает важное положение в области стыковки ряда метаболических путей (гликолиз, глюконеогенез, пентозофосфатный путь, гликогенез и гликогенолиз) (рис.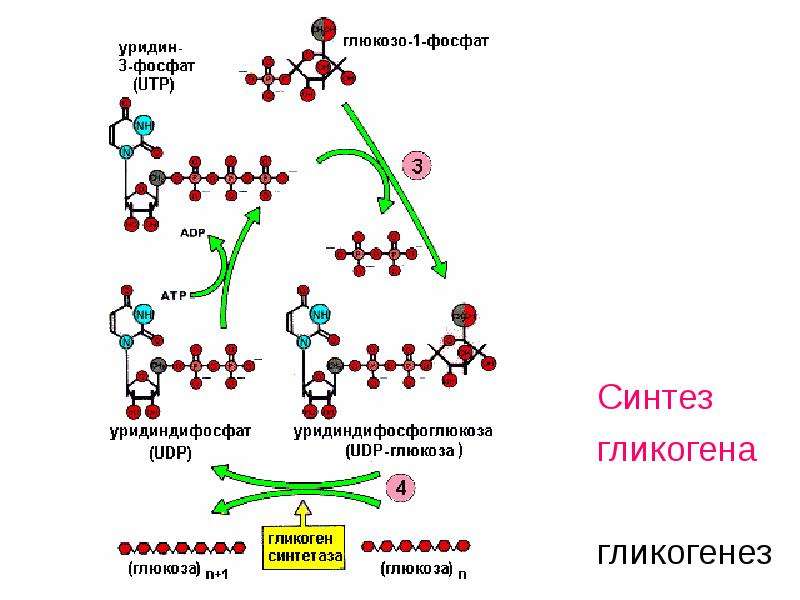 18.2). В ходе гликолиза он превращается во фруктозо-6-фосфат при участии фос гексозоизомеразы, при этом происходит альдо-кето-изомеризация. Фермент действует только на а-аномер глюкозо-6-фосфата [c.182]
18.2). В ходе гликолиза он превращается во фруктозо-6-фосфат при участии фос гексозоизомеразы, при этом происходит альдо-кето-изомеризация. Фермент действует только на а-аномер глюкозо-6-фосфата [c.182]
МЕХАНИЗМЫ КОНТРОЛЯ ГЛИКОГЕНОЛИЗА И ГЛИКОГЕНЕЗА [c.192]
Рнс. 22.5. Регуляция гликогенолиза и гликогенеза сАМР-зависимой протеинкиназой. При увеличении концентрации сАМР стимулируются реакции, ведущие к запуску гликогенолиза (они показаны жирными стрелками), и ингибируются реакции, ведущие к его торможению (показаны пунктирными стрелками). При уменьшении концентрации сАМ Р под действием фосфодиэстеразы возникает противоположная ситуация и в итоге стимулируется гликогенез [c.220]
Ранее предполагали, что процессы расщепления являются обращением процессов синтеза (например, гликогенолиз и гликогенез), а синтез жирных кислот рассматривали как процесс, обратный их окислению. [c.231]
Образование гликогена из углеводов называется гликогенезом, а из неуглеводного материала (аминокислот, глицерина и т.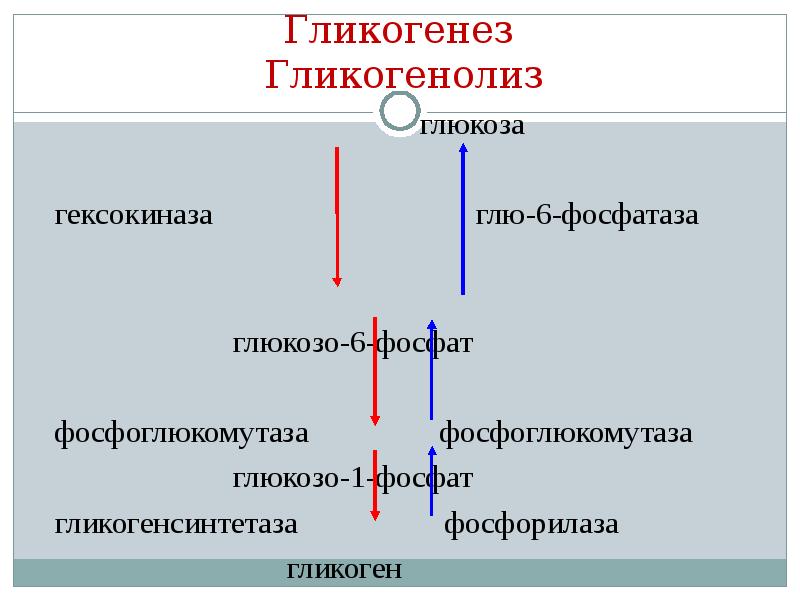 д.)—гликонеогенезом. В организме протекают и противоположные им процессы гликогенолиз — расщепление гликогена до глюкозы, а гликолиз — более глубокий распад до пировиноградной кислоты. [c.82]
д.)—гликонеогенезом. В организме протекают и противоположные им процессы гликогенолиз — расщепление гликогена до глюкозы, а гликолиз — более глубокий распад до пировиноградной кислоты. [c.82]
Процессы гликолиза и гликогенеза регулируются гормонами адреналином, инсулином, глюкагоном. Адреналин, выделяющийся в надпочечниках, стимулирует реакции гликолиза и снижает скорость гликогеногенеза, при этом улучшается снабжение мышц энергией. Инсулин, вьвделя-ющийся В-клетками островков Лангерганса в поджелудочной железе, усиливает транспорт глюкозы внутрь клеток, из-за чего снижается содержание глюкозы в крови и усиливается синтез гликогена. В ответ на низкое содержание глюкозы в крови адреналин стимулирует выделение в А-клетках островков Лангерганса гормона глюкагона, который стимулирует глюкогенез в печени, в результате образуется большое количество глюкозы, которая поступает в кровь и затем переносится в другие ткани. [c.82]
И 25°), она происходит только при распаде гликогена и не связана с гликогенезом, т.
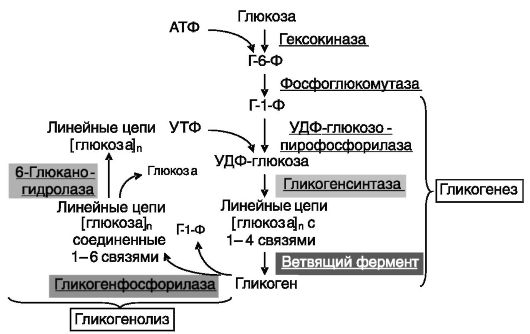 е. с процессом ресинтеза гликогена. Гликогенез происходит и тогда, когда отношение [Фн]/[Глюкозо-1-фосфат] достигает 300, а также при некоторых наследственных нарушениях обмена, нри которых фосфорилаза вообще отсутствует. Кроме того, в присутствии адреналина, который, как только что упоминалось, стимулирует активность фосфорилазы, происходит распад, а не синтез гликогена. В настоящее время благодаря работам Лелуара и других исследователей окончательно доказано, что синтез гликогена идет по пути полимеризации не самого глюкозо-1-фосфата, а смешанного ангидрида этого соединения и УМФ, так называемой УДФ-глюкозы, или УДФГ (См. гл. VIII). В этой реакции участвует специфичный фермент — гликогенсинтетаза. [c.285]
е. с процессом ресинтеза гликогена. Гликогенез происходит и тогда, когда отношение [Фн]/[Глюкозо-1-фосфат] достигает 300, а также при некоторых наследственных нарушениях обмена, нри которых фосфорилаза вообще отсутствует. Кроме того, в присутствии адреналина, который, как только что упоминалось, стимулирует активность фосфорилазы, происходит распад, а не синтез гликогена. В настоящее время благодаря работам Лелуара и других исследователей окончательно доказано, что синтез гликогена идет по пути полимеризации не самого глюкозо-1-фосфата, а смешанного ангидрида этого соединения и УМФ, так называемой УДФ-глюкозы, или УДФГ (См. гл. VIII). В этой реакции участвует специфичный фермент — гликогенсинтетаза. [c.285]Инсулин снижает уровень глюкозы в крови двумя путями ) способствуя ее проникновению в клетки и 2) активируя гликогенез в печени и мышцах. В отсутствие инсулина некоторый избыток глюкозы выводится почка.ми (гликозурня). [c.388]
Рнс. 19. 1. Схема гликогенеза и гликогенолиза в печени. На включение одной молекулы глюкозы в состав гликогена расходуются две высокоэнергетические фосфатные связи. 0 сгимуляция — ингибирование. Инсулин понижает уровень сАМР только в том случае, если повьииение уровня сАМР было вызвано глюкагоном или адреналином, т.е. по отношению к последним инсулин выступает как антагонист. [c.190]
1. Схема гликогенеза и гликогенолиза в печени. На включение одной молекулы глюкозы в состав гликогена расходуются две высокоэнергетические фосфатные связи. 0 сгимуляция — ингибирование. Инсулин понижает уровень сАМР только в том случае, если повьииение уровня сАМР было вызвано глюкагоном или адреналином, т.е. по отношению к последним инсулин выступает как антагонист. [c.190]
В процессе гликогенеза клетки забирают глюкозу из крови, а печень восполняет недостаток глюкозы посредством гликогеноли- [c.328]
В. Влияние на образование глюкозы (глюконеогенез). Влияние инсулина на транспорт глюкозы, гликолиз и гликогенез проявляется за считанные секун- [c.256]
Регуляция метаболизма гликогена осушествляется путем изменения активностей гликогенсинтазы и фосфорилазы (эти активности контролируются субстратами аллостерически, а также регулируются гормонами). Повышение концентрации сАМР приводит к активации фосфорилазы под действием киназы фосфорилазы и одновременно к переходу гликогенсинтазы в неактивную форму (см.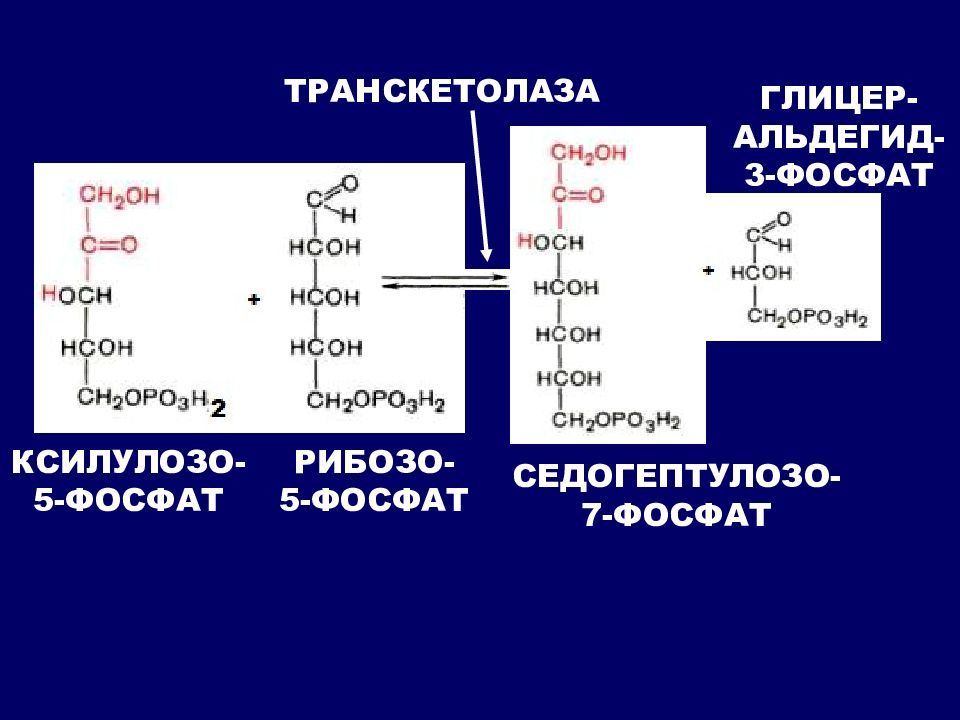 гл. 19) в обоих процессах участвует сАМР-зависимая про-теинкиназа. Таким образом, при ингибировании гликогенолиза усиливается гликогенез, а при ингибировании последнего усиливается гликогенолиз. Важное значение для регуляции метаболизма гликогена имеет то обстоятельство, что дефосфорилирование фосфорилазы а, киназы фосфорилазы и гликогенсин- [c.219]
гл. 19) в обоих процессах участвует сАМР-зависимая про-теинкиназа. Таким образом, при ингибировании гликогенолиза усиливается гликогенез, а при ингибировании последнего усиливается гликогенолиз. Важное значение для регуляции метаболизма гликогена имеет то обстоятельство, что дефосфорилирование фосфорилазы а, киназы фосфорилазы и гликогенсин- [c.219]
Описаны гликогенозы, связанные с недостаточностью фосфорилазы в печени (гликогеноз VI типа), недостаточностью фосфофруктокиназы в мышцах и эритроцитах (гликогенез VII типа болезнь Таруи), а также гликогеноз, обусловленный недостаточностью киназы фосфорилазы. Сообщалось также о случаях недостаточности аденилаткичазы и сАМР-зависимой протеинкиназы. [c.195]
Глюкуроновая кислота образуется из глюкозы по пути уроновых кислот в результате реакций, приведенных на рис. 21.1. Глюкозо-6-фосфат превращается в глюкозо-1-фосфат, который затем взаимодействует с уридинтрифосфатом (UTP) с образованием активного нуклеотида уридиндифосфатглюкозы (UDP-глюкозы). Последнюю реакцию катализирует фермент UDP-глюкозопирофосфорилаза. Реакции, предшествующие этой стадии, характерны для процесса гликогенеза в печени (см. рис. 19.1). UDP-глюкоза окисляется по С-6 с образованием глюкуро-ната, причем процесс протекает в две стадии. Продуктом стадии окисления, катализируемой NAD-зависимой UDP-глюкозодегидрогеназой, является UDP-глюкуронат. [c.205]
Последнюю реакцию катализирует фермент UDP-глюкозопирофосфорилаза. Реакции, предшествующие этой стадии, характерны для процесса гликогенеза в печени (см. рис. 19.1). UDP-глюкоза окисляется по С-6 с образованием глюкуро-ната, причем процесс протекает в две стадии. Продуктом стадии окисления, катализируемой NAD-зависимой UDP-глюкозодегидрогеназой, является UDP-глюкуронат. [c.205]
Гликогенез — gaz.wiki
Гликогенез реагирует на гормональный контроль.
Одной из основных форм контроля является разнообразное фосфорилирование гликогенсинтазы и гликогенфосфорилазы. Это регулируется ферментами под контролем гормональной активности, которая, в свою очередь, регулируется многими факторами. Таким образом, существует множество различных возможных эффекторов по сравнению с аллостерическими системами регуляции.
Адреналин (адреналин)
Гликогенфосфорилаза активируется фосфорилированием, тогда как гликогенсинтаза ингибируется.
Гликогенфосфорилаза превращается из своей менее активной формы «b» в активную форму «a» под действием фермента фосфорилазы киназы. Этот последний фермент сам активируется протеинкиназой А и дезактивируется фосфопротеинфосфатазой-1.
Этот последний фермент сам активируется протеинкиназой А и дезактивируется фосфопротеинфосфатазой-1.
Сама протеинкиназа А активируется гормоном адреналином. Адреналин связывается с рецепторным белком, который активирует аденилатциклазу. Последний фермент вызывает образование циклического АМФ из АТФ ; две молекулы циклического АМФ связываются с регуляторной субъединицей протеинкиназы A, которая активирует ее, позволяя каталитической субъединице протеинкиназы A диссоциировать от сборки и фосфорилировать другие белки.
Возвращаясь к гликогенфосфорилазе, менее активная форма «b» может сама активироваться без конформационных изменений. 5’АМР действует как аллостерический активатор, тогда как АТФ является ингибитором, как уже было замечено с контролем фосфофруктокиназы , помогая изменять скорость потока в ответ на потребность в энергии.
Адреналин не только активирует гликогенфосфорилазу, но также ингибирует гликогенсинтазу. Это усиливает эффект активации гликогенфосфорилазы.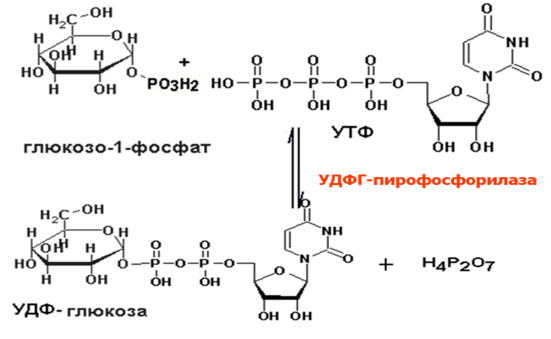 Это ингибирование достигается с помощью аналогичного механизма, так как протеинкиназа А фосфорилирует фермент, что снижает его активность. Это называется координированным взаимным контролем. Обратитесь к гликолизу для получения дополнительной информации о регуляции гликогенеза.
Это ингибирование достигается с помощью аналогичного механизма, так как протеинкиназа А фосфорилирует фермент, что снижает его активность. Это называется координированным взаимным контролем. Обратитесь к гликолизу для получения дополнительной информации о регуляции гликогенеза.
Ионы кальция
Ионы кальция или циклический АМФ (цАМФ) действуют как вторичные посредники. Это пример отрицательного контроля. Ионы кальция активируют киназу фосфорилазы. Это активирует гликогенфосфорилазу и ингибирует гликогенсинтазу.
ГЛИКОГЕНЕЗ это
Читать PDF304.92 кб
Клиническое значение цитохимического теста на гликоген в определении эффективности терапии бактериал
Бадретдинова Ф. Ф., Каюмов Ф. А., Шейда Л. А.
Для выявления бактериального вагиноза и контроля лечения у 53 больныхпроводили рН-метрию вагинального содержимого, аминный тест, исследования вагинальных мазков на «ключевые клетки».
725.76 кб
Гликоген в скелетни мускули, миокард и черен дроб на плъхове, третирани с Flutamide
Ф. Гергинска, С. Делчев, К. Георгиева, И. Коева, М. Шишманова, О. Горансон
Читать PDF455.65 кб
СОСТОЯНИЕ ГЛИКОГЕН-СИНТЕЗИРУЮЩЕЙ ФУНКЦИИ ПЕЧЕНИ КРЫС ПРИ АЛЛОКСАН-ИНДУЦИРОВАННОМ САХАРНОМ ДИАБЕТЕ И
Айзман Роман Иделевич, Гайдарова Анна Павловна
Целью работы является изучение влияния порошка корневища куркумы, его основного действующего компонента куркумина и антиоксиданта селенофана на содержание гликогена в печени крыс с экспериментальной моделью сахарного диабета.
Читать PDF34.28 кб
Цитохимическое определение гликогена при заболеваниях шейки матки у женщин
Богдасаров А.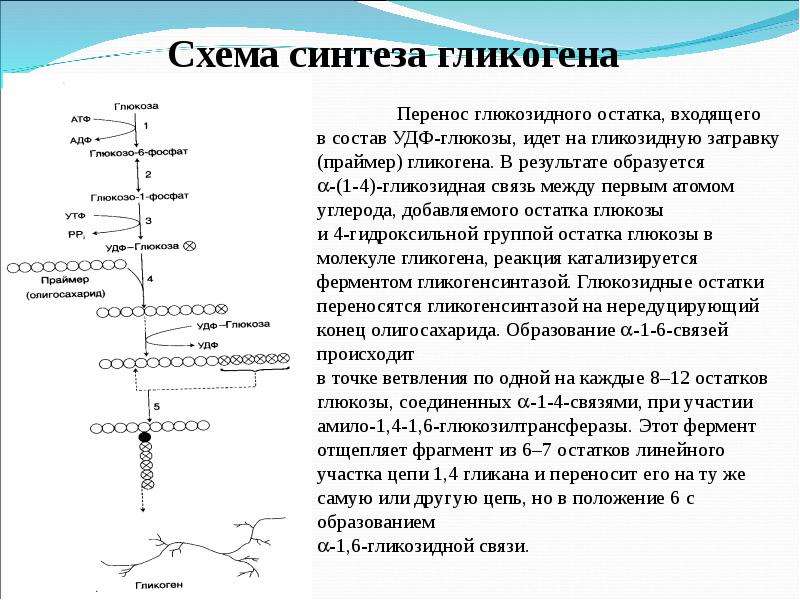 Ю., Родкина Р. А., Давидян Л. Ю., Олейникова Д. В.
Ю., Родкина Р. А., Давидян Л. Ю., Олейникова Д. В.
293.37 кб
Влияние озонирования на содержание гликогена в гепатоцитах и лимфобластах в печени мышей линии AKR
Помаскин О. Б., Иванов С. В., Перминов А. С.
Читать PDF110.79 кб
Витаминный статус у детей с болезнями накопления гликогена
Зубович А.И., Прохорова И.В., Строкова Т.В., Багаева М.Э., Сурков А.Г., Павловская Е.В., Сокольников А.А.
Читать PDF114.35 кб
Витаминный статус у детей с болезнями накопления гликогена
Зубович А.И., Прохорова И.В., Строкова Т.В., Багаева М.Э., Сурков А.Г., Павловская Е.В., Сокольников А.А.
Читать PDF542.
 39 кб
39 кбГликогеновая болезнь и сахарный диабет типа 1
Титович Е. В., Щербачева Л. Н.
Читать PDF125.89 кб
Влияние фонового резонансного излучения на уровень гликогена в печени при хронической описторхозной
Поддубная О. А., Белобородова Э. И., Левицкий Е. Ф.
Хронический описторхоз паразитарное заболевание человека с признаками снижения реактивности организма. Один из способов оценки реактивности заключается в качественном и количественном анализе гликогена в клетках печени.
Читать PDF1.03 мб
Качественные и количественные показатели содержания гликогена в печени крыс в динамике развития токс
Лебедева Е. И., Мяделец О. Д.
Целью исследования явилось определение содержания и распределения гликогена в печени крыс в динамике развития токсического цирроза.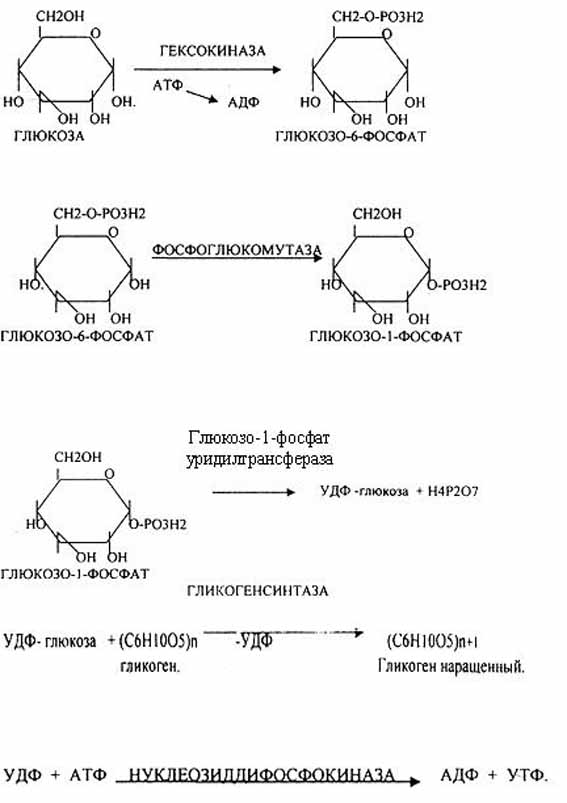
2.53 мб
Гистохимические исследования распределения гликогена в органах и тканях Opisthorchis felineus, взяты
Начева Л.В., Бибик О.И., Нестерок Ю.А.
Гистохимические исследования показывают, что после действия антигельминтиков: азинокса и сочетания мебендазола с празиквантелем гликоген исчезает из паренхимы и общая реакция на присутствие углеводов резко снижается.
Читать PDF565.93 кб
Опыт применения транзиентной эластографии печени у детей с гликогеновой болезнью
Сурков А. Н., Намазова-баранова Л. С., Потапов А. С.
Читать PDF596.01 кб
Качество жизни и клинико-лабораторные параллели у детей с гликогеновой болезнью
Черников В.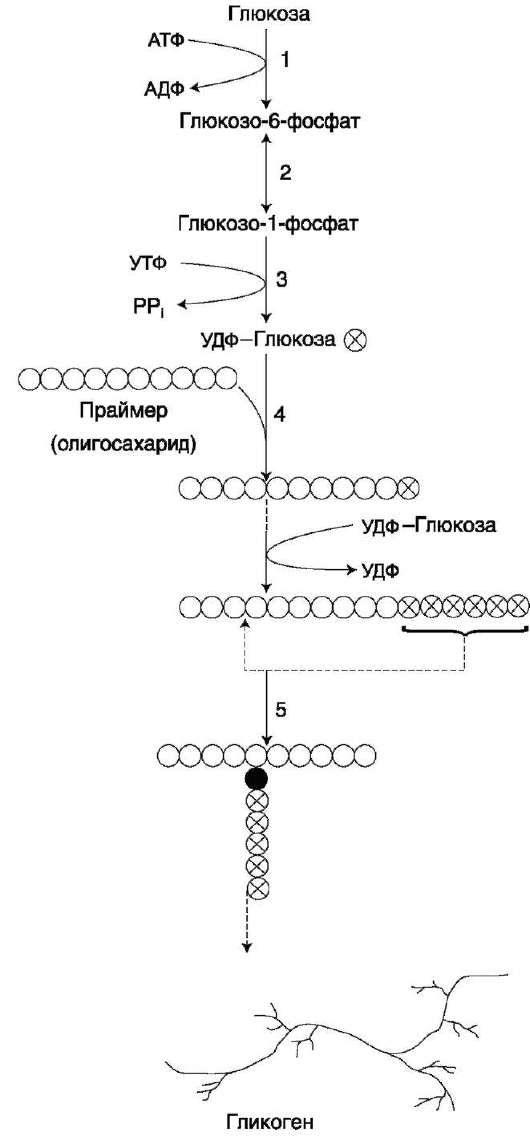 В., Сурков А. Н., Потапов А. С., Винярская И. В.
В., Сурков А. Н., Потапов А. С., Винярская И. В.
22.48 мб
Клинические проявления в дебюте печеночных форм гликогеновой болезни
Прохорова И.В., Строкова Т.В., Сурков А.Г., Багаева М.Э., Павловская Е.В., Зубович А.И., Васильева Е.А.
Читать PDF0.00 байт
Cодержание гликогена в клетках моноцитарного ростка костного мозга и периферической крови
Комарова Татьяна Михайловна
Проведено исследование влияния экспериментального поражения печени матери токсического генеза на морфофункциональные особенности становления моноцитов в костном мозге потомства.
Гликогенез и его роль Синтез гликогена (гликогенез)
Прежде всего глюкоза подвергается фосфорилированию при участии фермента гексокиназы, а в печени – и глюкокиназы. Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фос-фат:
Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фос-фат:
Образовавшийся глюкозо-1-фосфат уже непосредственно вовлекается в синтез гликогена. На первой стадии синтеза глюкозо-1-фосфат вступает во взаимодействие с УТФ (уридинтрифосфат), образуя уридиндифосфатглю-козу (УДФ-глюкоза) и пирофосфат. Данная реакция катализируется ферментом глюкозо-1-фосфат-уридилилтрансферазой (УДФГ-пирофосфорила-за):
Глюкозо-1-фосфат + УТФ < = > УДФ-глюкоза + Пирофосфат.
На второй стадии – стадии обр-ния гликогена – происходит перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена. При этом обр-тся α-(1–>4)-связь между первым атомом углер добавляемого остатка глюкозы и 4-гидроксильной группой остатка глюкозы цепи. Эта реакция катализируется ферментом гликогенсинтазой. Необходимо еще раз подчеркнуть, что реакция, катализируемая гликогенсинтазой, возможна только при условии, что полисахаридная цепь уже содержит более 4 остатков D-глю-козы.
Образующийся УДФ затем вновь фосфорилируется в УТФ за счет АТФ, и таким образом весь цикл превращений глюкозо-1-фосфата начинается сначала.
В целом образование α-1,4-глюкозидной ветви («амилозной» ветви) гликогена можно представить в виде следующей схемы:
Установлено, что гликогенсинтаза не способна кат-вать обр-ние α-(1–>6)-связи, имеющейся в точках ветвления гликогена. Этот проц кат-рует спец фермент, получивший название гли-когенветвящего фермента, или амило-(1–>4)–>(1–>6)-трансглюкозидазы. Последний катализирует перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее 11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи гликогена. В результате образуется новая боковая цепь.
Ветвление повышает раст-сть гликогена. Кроме того, благодаря ветвлению создается большое кол-во невосст-вающих концевых остатков, к-рые явл местами действия гликогенфосфорилазы и гликогенсинтазы.
Т.об., ветвление увеличивает скорость синтеза и расщепления гликогена.
Благодаря способности к отложению гликогена (главным образом в печени и мышцах и в меньшей степени в других органах и тканях) создаются условия для накопления в норме некоторого резерва углеводов. При повышении энерготрат в организме в результате возбуждения ЦНС обычно происходят усиление распада гликогена и образование глюкозы.
Билет 25
Гликофосфолипиды
Гликолипиды широко представлены в тканях, особенно в нервной ткани, в частности в мозге. Главной формой гликолипидов в животных тканях явл гликосфинголипиды. Последние содержат церамид, состоящий из спирта сфингозина и остатка жирной к-ты, и один или несколько остатков сахаров.
Простейшими гликосфинголипидами явл галактозилцерамиды и глюкозилцерамиды.
Галактозилцерамиды – главные сфинголипиды мозга и других нервных тканей, но в небольших количествах встречаются и во многих других тканях.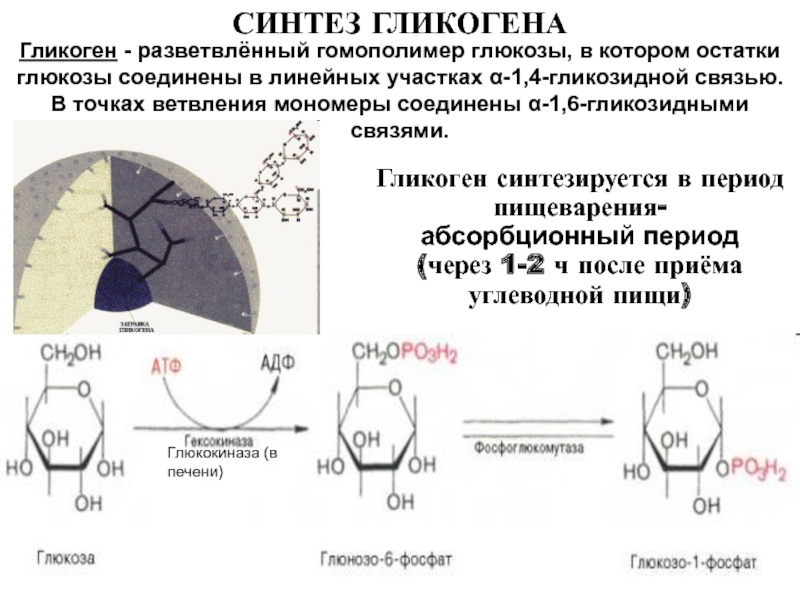 В состав галактозилцерамидов входит гексоза (обычно это D-галактоза), к-рая связана эфирной связью с гидроксильной группой аминоспирта сфингозина. Кроме того, в составе галактозилцерамида имеется жирная к-та. Чаще всего это лигноцериновая, нервоновая или це-реброновая к-та, т.е. ЖКы, имеющие 24 углеродных атома.
В состав галактозилцерамидов входит гексоза (обычно это D-галактоза), к-рая связана эфирной связью с гидроксильной группой аминоспирта сфингозина. Кроме того, в составе галактозилцерамида имеется жирная к-та. Чаще всего это лигноцериновая, нервоновая или це-реброновая к-та, т.е. ЖКы, имеющие 24 углеродных атома.
Сущ-ют сульфогалактозилцерамиды, к-рые отлич от га-лактозилцерамидов наличием остатка серной к-ты, присоединенного к 3-ему углеродному атому гексозы. В мозге млекопит сульфогалактозилцерамиды в осн нах в белом в-ве, при этом содержание их в мозге намного ниже, чем галактозилцерамидов.
Глюкозилцерамиды – простые гликосфинголипиды, представлены в тканях, отличных от нервной, причем главным образом глюкозил-церамидами. В небольших количествах они имеются в ткани мозга. В отличие от галактозилцерамидов у них вместо остатка галактозы им-ся остаток глюкозы.
Более сложными гликосфинголипидами явл ганглиозиды, образующиеся из гликозилцерамидов. Ганглиозиды дополнительно содержат одну или несколько мол-л сиаловой к-ты. В тканях человека доминирующей сиаловой к-той явл нейраминовая. Кроме того, вместо остатка глюкозы они чаще содержат сложный олигосахарид. Ганглиозиды в больших количествах находятся в нервной ткани. Они, по-видимому, выполняют рецепторные и другие функции. Одним из простейших ганглиозидов явл гематозид, выделенный из стромы эритроцитов. Он содержит церамид (ацилсфингозин), одну мол-лу глюкозы, одну мол-лу N-ацетилнейраминовой к-ты.
Ганглиозиды дополнительно содержат одну или несколько мол-л сиаловой к-ты. В тканях человека доминирующей сиаловой к-той явл нейраминовая. Кроме того, вместо остатка глюкозы они чаще содержат сложный олигосахарид. Ганглиозиды в больших количествах находятся в нервной ткани. Они, по-видимому, выполняют рецепторные и другие функции. Одним из простейших ганглиозидов явл гематозид, выделенный из стромы эритроцитов. Он содержит церамид (ацилсфингозин), одну мол-лу глюкозы, одну мол-лу N-ацетилнейраминовой к-ты.
ГЛИКОЛИПИДЫ, соед., построенные из липидного и УГного фрагментов, соединенных ковалентной связью. Гликолипиды широко распространены в природе (они обнаружены в животных, растениях и микроорг-мах) и охватывают разнородные по стр-ре соединения.
В зависимости от природы липидной части гликолипиды можно разделить на четыре группы: 1) гликозилдиглицериды, липидная часть к-рых представляет собой остаток глицерина, ацилированный в положения 1 и 2 высшими жирными к-тами; 2) гликосфинголипиды, в к-рых липидным фрагментом явл церамид-остаток высшего аминоспирта (сфингозинового основания), N-ацилированного высшей жирной к-той; 3) полипренилфосфатсахара, у к-рых липидная часть мол-лы представляет собой остаток полипренола Н(СН2С(СН3)=СНСН2)nОН; 4) гликолипиды микроорг-мов, в состав к-рых входят остатки высших жирных к-т, ацилирующих остатки Сахаров или неУГных компонентов мол-лы.
Подавляющее большинство гликолипидов относится к первым двум группам и явл важными компонентами мембран.
Гликолипиды микроорг-мов включают обширную группу соед., сильно различающихся по строению и св-вам (напр, липид А-компонент липополисах-дов грам-отрицат. бактерий, отвечающ за их эндотоксич. св-ва.
Несмотря на большое разнообразие стр-р, гликолипиды обладают нек-рыми общими св-вами. Гликолипиды явл ПАВ. Благодаря присутствию длинных алифатич. цепочек, они могут раств. в нек-рых орг. р-рителях (напр., в бутаноле, смеси хлороформа и метанола), а наличие УГной части придает им р-римость в воде, возрастающую с увеличением длины УГной цепи. Выбор способов выделения гликолипидов из ткани и разделение их на классы зависит от полярности исследуемых гликолипидов.
Гликогенез | Info-Farm.RU
Гликогенез — процесс биосинтеза гликогена, происходит в клетках тех живых организмов, которые используют этот полисахарид для хранения глюкозы (животных, грибов и многих прокариот).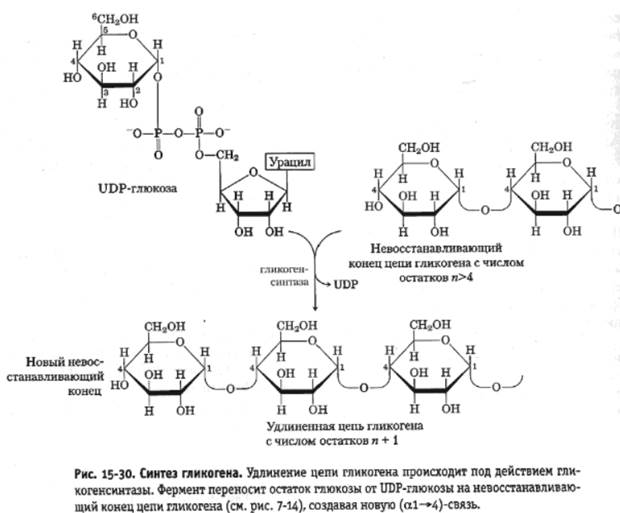 У млекопитающих протекает с разной интенсивностью во всех тканях, но наиболее выражено в печени и скелетных мышцах. Субстратом для гликогенеза является уридиндифосфатглюкоза, то есть он осуществляется путем отличным от деградации гликогена — гликогенолиза, основным продуктом которого является глюкозо-1-фосфат. Ключевым ферментом гликогенеза является гликогенсинтаза.
У млекопитающих протекает с разной интенсивностью во всех тканях, но наиболее выражено в печени и скелетных мышцах. Субстратом для гликогенеза является уридиндифосфатглюкоза, то есть он осуществляется путем отличным от деградации гликогена — гликогенолиза, основным продуктом которого является глюкозо-1-фосфат. Ключевым ферментом гликогенеза является гликогенсинтаза.
Первые свидетельства о различиях в путях биосинтеза и деградации гликогена были получены при изучении болезни Мак-Ардла — редкой формы гликогеноза, что проявляется в болезненных судорогах скелетных мышц во время интенсивной физической нагрузки. У людей, страдающих этим расстройством, не хватает гликогенфосфорилазы — фермента, обеспечивает расщепление гликогена, однако запасания гликогена не нарушено. Таким образом было сделано заключение, что гликогенолиз и гликогенез должны происходить различными путями. Роль УДФ-глюкозы в процессе гликогенеза выяснил аргентинский биохимик Луис Лелуар 1957 года.
Образование УДФ-глюкозы
Процесс биосинтеза гликогена начинается с глюкозо-6-фосфата. В мышцах это соединение образуется путем фосфорилирования свободной глюкозы, транспортируется в клетки из крови. В печени глюкозо-6-фосфат также может синтезироваться в процессе глюконеогенеза, в частности с молочной кислоты, выделяется мышцами во время интенсивных нагрузок.
В мышцах это соединение образуется путем фосфорилирования свободной глюкозы, транспортируется в клетки из крови. В печени глюкозо-6-фосфат также может синтезироваться в процессе глюконеогенеза, в частности с молочной кислоты, выделяется мышцами во время интенсивных нагрузок.
Для использования в процессе гликогенеза глюкозо-6-фосфат превращается в глюкозо-1-фосфат фосфоглюкомутаза, этот фермент общий для путей биосинтеза и расщепления гликогена. Продукт реакции становится субстратом для УДФ-глюкозофосфорилазы (фермент названный по обратной реакцией), что катализирует образование УДФ-глюкозы:
- УТФ + глюкозо-1-фосфат → УДФ-глюкоза + ФФ н
Хотя сама реакция конденсации глюкозо-1-фосфата и УТФ имеет очень незначительную положительную изменение свободной энергии, в ней образуется пирофосфат, который сразу же гидролизуется неорганической пирофосфатазы в сильно екзергоничний реакции (ΔG = -19,2 кДж / моль). В результате суммарный процесс необратимый за клеточных условий.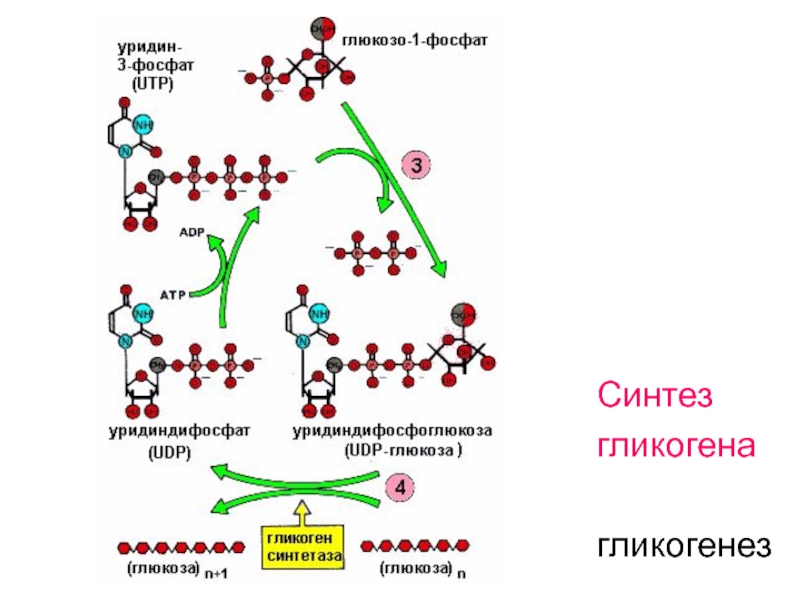
Использование в процессе биосинтеза гликогена УДФ-глюкозы имеет несколько преимуществ. Во-первых, остаток нуклеотида активирует молекулу глюкозы, а именно C-1, к которому он присоединен, и способствует нуклеофильного атаке на него. Урилидмоносфосфат является хорошим отходной группой во время следующей, гликогенсинтазнои, реакции. Во-вторых, хотя остаток нуклеотида непосредственно не участвует в этой реакции, он нековалентно взаимодействует с ферментом и способствует более быстрому прохождению химического преобразования. В-третьих, присоединение нуклеотидов к глюкозе и других моносахаридов, может выполнять роль «метки» этих молекул для нужд биосинтеза, в то время как фосфаты используются для других путей, например гликолиза.
Полимеризация гликогена
УДФ-глюкоза вступает в реакцию, в которой остаток глюкозы переносится на нередукуючий конец одной из ветвей молекулы гликогена. При этом формируется (α1 → 4) -гликозидными связь. Реакцию катализирует гликогенсинтаза:
- УДФ-глюкоза + гликоген n → УДФ + гликоген n + 1;
Изменение свободной энергии для этой реакции составляет ΔG 0 ‘= -13,4 кДж / моль.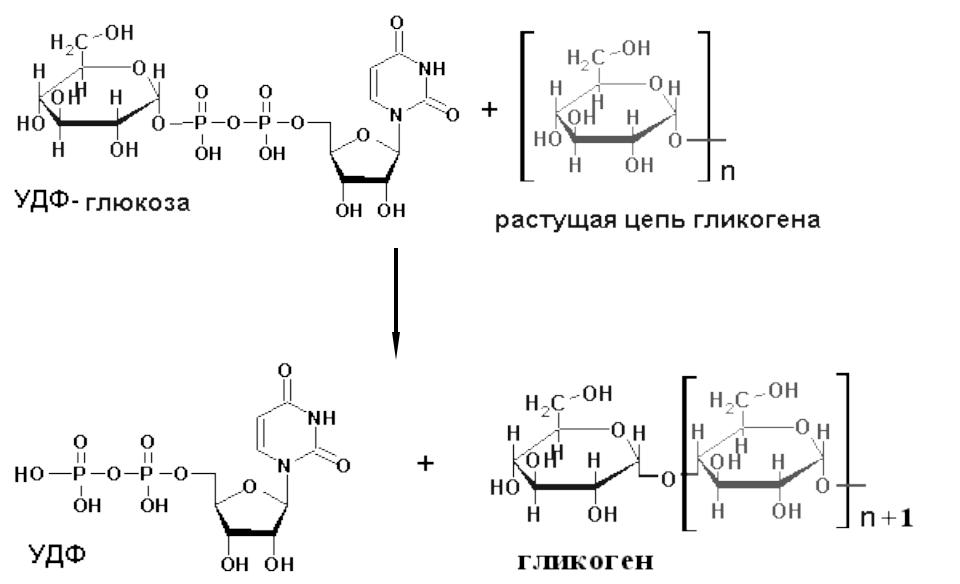 У млекопитающих существует две изоформы гликогенсинтазы, аминокислотные последовательности которых идентичны примерно на 70%, — печеночная и мышечная. Растения и бактерии также имеют крахмал / гликогенсинтазы однако они используют как субстрат АДФ-глюкозу, и мало родственные животными гликогенсинтазамы.
У млекопитающих существует две изоформы гликогенсинтазы, аминокислотные последовательности которых идентичны примерно на 70%, — печеночная и мышечная. Растения и бактерии также имеют крахмал / гликогенсинтазы однако они используют как субстрат АДФ-глюкозу, и мало родственные животными гликогенсинтазамы.
Гликогенсинтаза не может обеспечивать образование мест ветвления — (α1 → 6) -связей. Они формируются ответвительные ферментом (амило- (1,4 → 1,6) -трансгликозилазою). От ветвей не короче одиннадцати остатков глюкозы он отщепляет фрагмент длиной 6-7 мономерных звеньев и переносит его на C-6 гидроксильную группу одного из внутренних глюкозных остатков той же или другой ветви. Новая ветка должна быть удалена от предыдущей как минимум на четыре мономерные звенья. Таким образом образуется вилка, каждая из которой может дальше полимеризоваться под влиянием гликогенсинтазы.
Действие ответвительные фермента не является обратной к действию дерозгалужуючого. Оба белки обладают трансферазною активностью, однако в первой (ответвительные) она проявляется в разрыве (α1 → 4) -связи и формировании (α1 → 6) -связь, тогда как второй (дерозгалужуючий) розщепленнюе одно (α1 → 4) -связь и образует другой, гидролиз (α1 → 6) -связи, что остался здиснюеться благодаря другой ферментативной активности.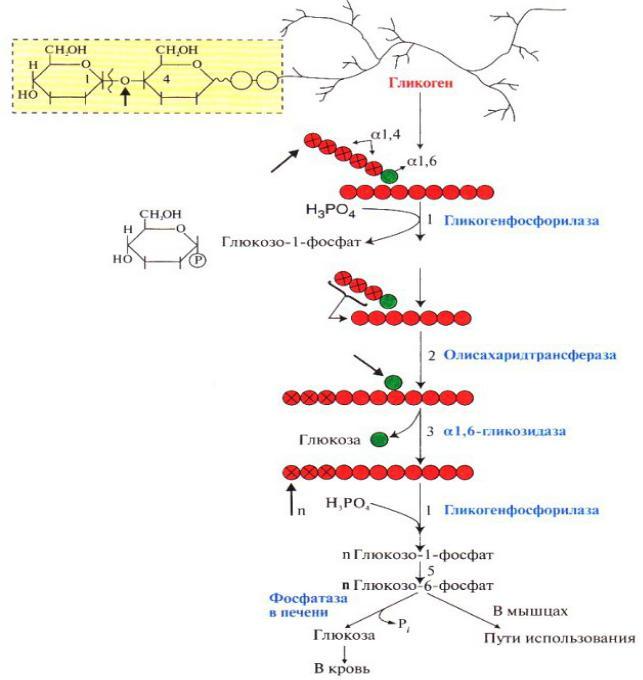 Такая разница вполне объяснима с точки зрения энергетики: поскольку изменение свободной энергии при гидролизе (α1 → 4) -связи составляет -15,5 кДж / моль, а (α1 → 6) — -7,1 кДж / моль, то гидролиз (α1 → 4) -связи может обеспечивать синтез (α1 → 6), но не наоборот.
Такая разница вполне объяснима с точки зрения энергетики: поскольку изменение свободной энергии при гидролизе (α1 → 4) -связи составляет -15,5 кДж / моль, а (α1 → 6) — -7,1 кДж / моль, то гидролиз (α1 → 4) -связи может обеспечивать синтез (α1 → 6), но не наоборот.
Биологическое значение ветвления состоит в том, что оно обеспечивает увеличение растворимости гликогена. Также каждая из образованных ветвей может быть субстратом для гликогенфосфорилазы или гилкогенсинтазы, в результате чего процессы синтеза и деградации существенно ускоряются.
Гликогенин
Гликогенсинтаза способна только присоединять остатки глюкозы в нередукуючих концов молекулы гликогена, уже содержит не менее четырех мономерных звеньев. Она не может начинать синтез de novo, для этого необходимо гликогенин — димерних белок, состоящий из двух идентничинх субъединиц по 37 кДа каждая (332 аминокислотные остатки). Гликогенин не только служит праймером для синтеза новых молекул гликогена, но и сам катализирует его первые реакции. Благодаря своей гликозилтрансферазний активности, одна из его субъединиц переносит остаток глюкозы с УДФ-глюкозы на гидроксильную группу тирозина 194 другой и наоборот. После этого происходит достройку еще шести-восьми мономерных субъединиц к каждому из двух новообразованных цепей. После этого в действие вступает гилкогенсинтаза, которая может использовать уже имеющийся праймер. Таким образом в основе каждой частицы гликогена лежит молекула гликогенину, ковалентно присоединена к ее единственного редуцирующего конца.
Благодаря своей гликозилтрансферазний активности, одна из его субъединиц переносит остаток глюкозы с УДФ-глюкозы на гидроксильную группу тирозина 194 другой и наоборот. После этого происходит достройку еще шести-восьми мономерных субъединиц к каждому из двух новообразованных цепей. После этого в действие вступает гилкогенсинтаза, которая может использовать уже имеющийся праймер. Таким образом в основе каждой частицы гликогена лежит молекула гликогенину, ковалентно присоединена к ее единственного редуцирующего конца.
Энергетический выход
Поскольку УДФ, что выделяется при гликогенсинтазнои реакции, снова превращается в УТФ благодаря переносу фосфатной группы с АТФ ферментом нуклеозиддифосфокиназою, то можно считать, что на включение одного остатка глюкозы в гликоген используется одна молекула АТФ. Суммарное уравнение процесса выглядит так:
- Глюкозо-6-фосфат + АТФ + гликоген n + H 2 O → гликоген n + 1 + АДФ + 2Ф н
Во время расщепления гликогена 90% остатков глюкозы отделяются путем фосфоролиз, в результате чего образуется глюкозо-1-фосфат, который может быть преобразован в глюкозо-6-фосфат без энергетических затрат. Только 10% глюкозных остатков в местах ветвления отсоединяются гидролитически и требуют дальнейшего фосфорилирования, на что используется АТФ. Так что для этих 10% «цена хранения» составляет 2 молекулы АТФ.
Только 10% глюкозных остатков в местах ветвления отсоединяются гидролитически и требуют дальнейшего фосфорилирования, на что используется АТФ. Так что для этих 10% «цена хранения» составляет 2 молекулы АТФ.
Регуляция гликогенеза
Основным регуляторным ферментом гликогенеза является гилкогенсинтетаза. По ее каталитическую активность могут влиять как аллостерические модуляторы, так и ковалентная модификация. Преобразование активной a формы этого фермента в неактивную b происходит вследствие фосфорилирования, в частности такими ферментами как протеинкиназа А, киназа гликогенсинтазы 3 и другими. То есть ее ответ на ковалентную модификацию противоположной таковой у ключевого фермента гликогенолиза — гликогенфосфорилазы. Неактивная гликогенсиназа b может включаться только под воздействием высоких концентраций аллостерического активатора глюкозо-6-фосфата, тогда как a форма не зависит от этого соединения.
Биохимия, гликогенез — StatPearls — Книжная полка NCBI
Введение
Гликоген, основная форма хранения глюкозы и основной источник неокислительной глюкозы для скелетных мышц и печени, вносит значительный вклад в свою деградацию, поддерживая нормальный уровень глюкозы в крови и обеспечивая топливо для сокращения мышц.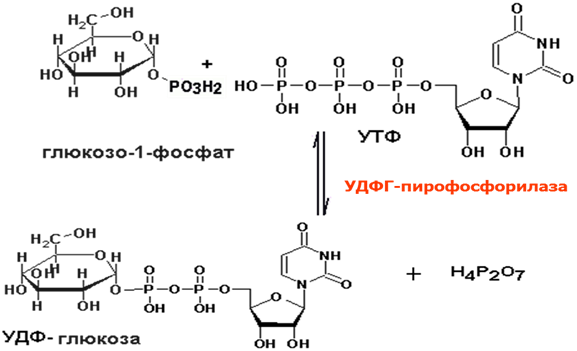 Что касается цитозольной деградации, основные ферменты, участвующие в распаде гликогена, представляют собой гликогенфосфорилазу и фермент разветвления.Гликогенфосфорилаза заботится о разрыве связей в линейной цепи, тогда как фермент разветвления переносит остатки глюкозы в линейную цепь для разрушения разветвлений. Оба фермента работают в скелетных мышцах и печени. Поскольку скелетные мышцы могут использовать фосфорилированную форму глюкозы в качестве топлива, для них не требуется глюкозо-6-фосфатаза.
Что касается цитозольной деградации, основные ферменты, участвующие в распаде гликогена, представляют собой гликогенфосфорилазу и фермент разветвления.Гликогенфосфорилаза заботится о разрыве связей в линейной цепи, тогда как фермент разветвления переносит остатки глюкозы в линейную цепь для разрушения разветвлений. Оба фермента работают в скелетных мышцах и печени. Поскольку скелетные мышцы могут использовать фосфорилированную форму глюкозы в качестве топлива, для них не требуется глюкозо-6-фосфатаза.
С другой стороны, печени требуется глюкозо-6-фосфатаза для дефосфорилирования глюкозы и экспорта глюкозы за пределы клетки. Что касается лизосомальной деградации, кислая альфа-глюкозидаза отвечает за гликогенолиз.Дефицит любого из этих ферментов проявляется в виде уникальных болезненных состояний. Большинство изменений в цитозольной деградации вызывают болезни накопления гликогена, включая болезнь фон Гирке, болезнь Кори и болезнь Херса. Нарушение лизосомальной деградации может привести к болезни Помпе.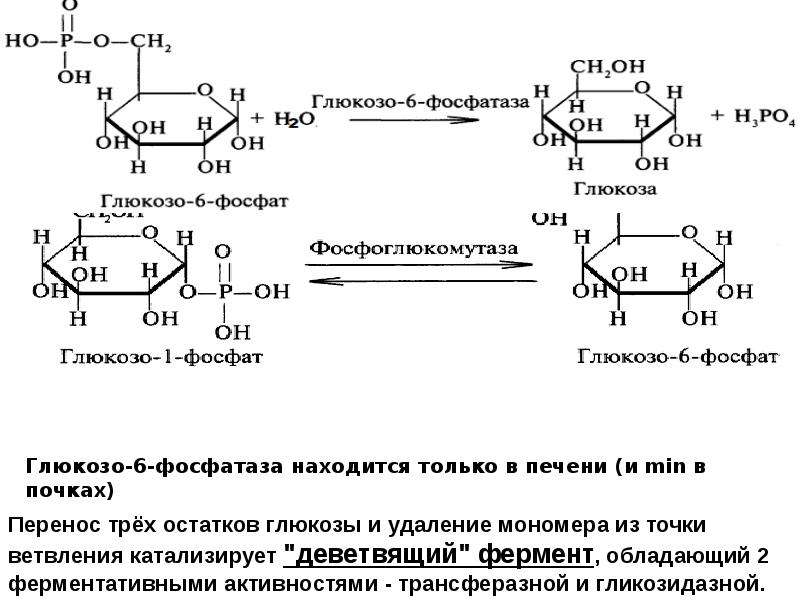 Нарушение роли гликогенолиза в нервном функционировании проявляется в проявлении болезни Лафора. Обнаружение изменений гликогенолиза может быть сделано в основном с помощью анализа ДНК и электронной микроскопии с помощью биопсии печени и скелетных мышц.
Нарушение роли гликогенолиза в нервном функционировании проявляется в проявлении болезни Лафора. Обнаружение изменений гликогенолиза может быть сделано в основном с помощью анализа ДНК и электронной микроскопии с помощью биопсии печени и скелетных мышц.
Основы
Гликоген существует из предшественников глюкозы, полученных из недавно проглоченных углеводов или глюконеогенных предшественников, включая лактат и аланин. Гликогенолиз — это просто процесс, участвующий в расщеплении гликогена для использования в качестве источника энергии, главным образом в скелетных мышцах и печени. Распад гликогена происходит двумя разными путями в зависимости от местоположения. Что касается скелетных мышц, деградация гликогена приводит к образованию глюкозо-1-фосфата, и мышцы сами по себе используют его в качестве топлива для сокращения.Гликогенолиз в скелетных мышцах происходит в условиях физической активности. С другой стороны, гликогенолиз печени генерирует глюкозу для экспорта в кровоток.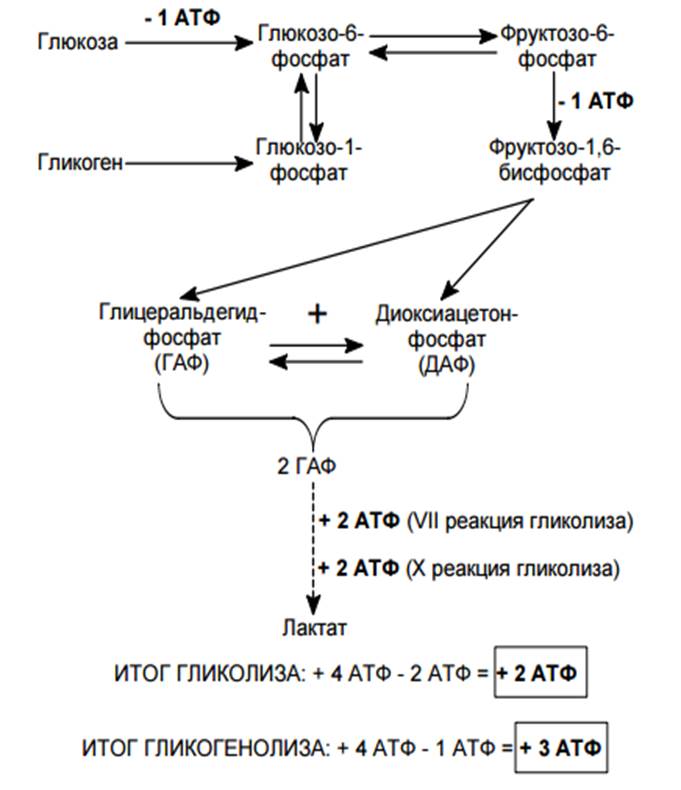 Стимулом для гликогенолиза печени является недостаток питания с соответствующим увеличением гормонов, таких как глюкагон. [1]
Стимулом для гликогенолиза печени является недостаток питания с соответствующим увеличением гормонов, таких как глюкагон. [1]
Проблемы, вызывающие озабоченность
Из-за жизненно важной роли, которую распад гликогена играет в нормальной физиологии, включая поддержание уровня глюкозы в крови и сокращение мышц во время активности, нарушения гликогенолиза вызывают патофизиологические состояния.Хотя исследователи исследовали роль гликогена, определенная информация не совсем понятна. Например, неясна конкретная роль гликогена в сокращении мышц или способ переноса гликогена в лизосомы.
Клеточный
Гликогенолиз, расщепление гликогена, происходит в двух клеточных участках: цитозоле и лизосоме. Различные ферменты осуществляют расщепление гликогена в этих клеточных участках. При разложении гликогена в качестве топлива используется глюкоза или глюкозо-1-фосфат.В скелетных мышцах захват глюкозы опосредуется транспортерами GLUT1 (лежащими на плазматической мембране) и GLUT4 (лежащими внутри внутриклеточных накопительных везикул).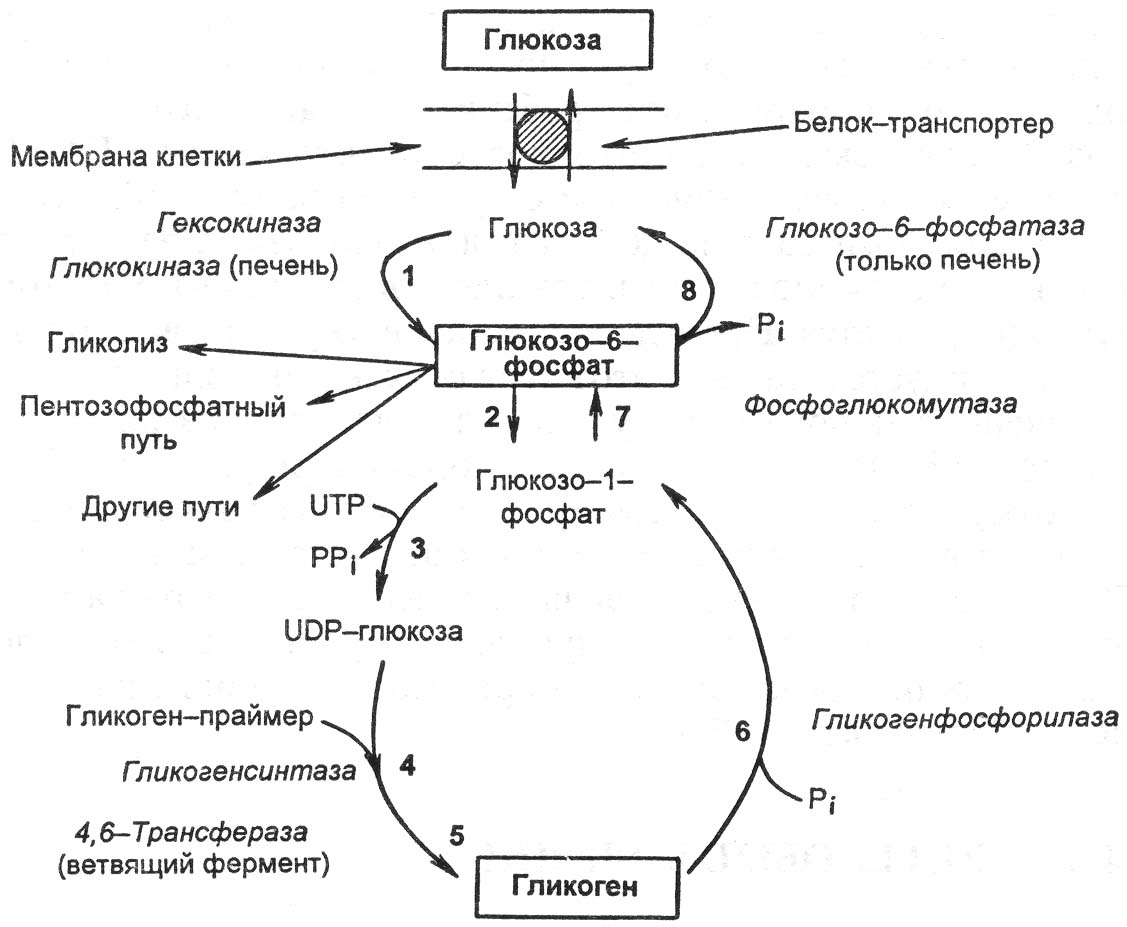 В цитозоле гликогенфосфорилаза сильно активируется АМФ для мышечной ткани. Что касается печени, глюкагон активирует гликогенфосфорилазу за счет увеличения циклического АМФ. Деградация гликогена в лизосомах опосредуется кислой альфа-глюкозидазой через аутофагические вакуоли, которые захватывают часть цитоплазмы и сливаются с органеллами, вмещая содержимое.Конкретные механизмы получают дальнейшее объяснение в следующих разделах. [2]
В цитозоле гликогенфосфорилаза сильно активируется АМФ для мышечной ткани. Что касается печени, глюкагон активирует гликогенфосфорилазу за счет увеличения циклического АМФ. Деградация гликогена в лизосомах опосредуется кислой альфа-глюкозидазой через аутофагические вакуоли, которые захватывают часть цитоплазмы и сливаются с органеллами, вмещая содержимое.Конкретные механизмы получают дальнейшее объяснение в следующих разделах. [2]
Молекулярный
Гликоген — это разветвленный полимер глюкозы. Глюкоза хранится в клетках в виде полимеров, что увеличивает растворимость, занимает меньше места и обеспечивает быструю мобилизацию. Запас гликогена в гепатоците соответствует расчетной концентрации глюкозы 400 мМ. И наоборот, вклад нерастворимого гликогена в осмолярность цитозоля в 40 миллионов раз меньше, чем вклад 40 мМ глюкозы.Следовательно, если бы полимерная форма гликогена не существовала, осмолярность цитозоля была бы достаточно высокой, чтобы вызвать проникновение воды в клетку посредством осмоса и привести к лизису клетки.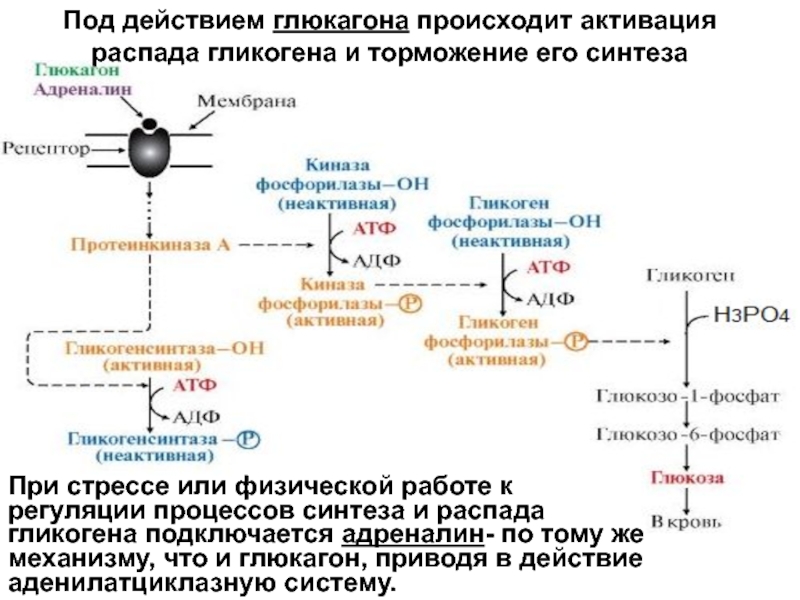 Гликоген приводит к более высокой растворимости, в основном из-за образования разветвлений. С другой стороны, большая часть полимера образует альфа-1-4 гликозидные связи, которые организуются в цепочки, разветвление происходит через каждые 4-8 мономеров глюкозы через альфа-1-6 гликозидные связи. Такое расположение приводит к классической организации гликогена, называемого бета-частицами, с самогликозилирующим белком, называемым гликогенином, в ядре.[3]
Гликоген приводит к более высокой растворимости, в основном из-за образования разветвлений. С другой стороны, большая часть полимера образует альфа-1-4 гликозидные связи, которые организуются в цепочки, разветвление происходит через каждые 4-8 мономеров глюкозы через альфа-1-6 гликозидные связи. Такое расположение приводит к классической организации гликогена, называемого бета-частицами, с самогликозилирующим белком, называемым гликогенином, в ядре.[3]
Важно понимать конформацию гликогена, поскольку гликогенолиз включает распад этого полимера на мономеры глюкозы с помощью отдельных ферментов, которые катализируют разрушение разветвлений и цепей гликогена.
Функция
Распад гликогена происходит во время голодания или при низком соотношении инсулина и глюкагона. Основные запасы энергии для организма — это гликоген и липиды. В то время как липиды приводят к большему количеству молекул АТФ после окисления, гликогенолиз приводит к меньшему количеству молекул АТФ.Однако существуют два существенных преимущества метаболизма гликогена. Первое преимущество соответствует быстрой мобилизации гликогена для удовлетворения метаболических потребностей. Возможна быстрая мобилизация, поскольку ферменты гликогенолиза могут прикрепляться к многочисленным ветвям гликогена и начинать одновременный гидролиз. Второе преимущество заключается в выработке энергии в условиях отложений с низким содержанием липидов, например, при анорексии. [3]
Первое преимущество соответствует быстрой мобилизации гликогена для удовлетворения метаболических потребностей. Возможна быстрая мобилизация, поскольку ферменты гликогенолиза могут прикрепляться к многочисленным ветвям гликогена и начинать одновременный гидролиз. Второе преимущество заключается в выработке энергии в условиях отложений с низким содержанием липидов, например, при анорексии. [3]
Количественно гликоген больше присутствует в скелетных мышцах, чем в печени.Тем не менее гликогенолиз играет важную роль в обеих тканях. В печени метаболизм гликогена играет жизненно важную роль во время голодания, приводя к выработке печеночной глюкозы для поддержания здорового уровня глюкозы в крови и поддержки потребностей в топливе других тканей. С другой стороны, полное проявление гликогена в скелетных мышцах указывает на критическую функцию, которую гликоген играет в скелетных мышцах с точки зрения быстрого образования АТФ. Существует тесная взаимосвязь между хранением гликогена в скелетных мышцах и сопротивлением усталости. Способность мышцы тренироваться в течение первых 30 минут активности, несмотря на обилие других источников энергии, таких как липиды, серьезно ухудшается, когда уровень гликогена в скелетных мышцах снижается. Истощение гликогена приводит к утомлению, потому что мышца не может обеспечить скелетным мышцам достаточное количество энергии для возбуждения и сокращения. Вероятная причина вращается вокруг роли гликогена в высвобождении кальция из саркоплазматической сети. [4] [5]
Способность мышцы тренироваться в течение первых 30 минут активности, несмотря на обилие других источников энергии, таких как липиды, серьезно ухудшается, когда уровень гликогена в скелетных мышцах снижается. Истощение гликогена приводит к утомлению, потому что мышца не может обеспечить скелетным мышцам достаточное количество энергии для возбуждения и сокращения. Вероятная причина вращается вокруг роли гликогена в высвобождении кальция из саркоплазматической сети. [4] [5]
Помимо обеспечения энергией, гликогенолиз может привести к образованию прекурсоров для участия в окислительных реакциях пентозофосфатного пути, помогая генерировать НАДФН, который необходим для синтеза жирных кислот и производства пентозофосфатов, которые необходимы для синтез РНК и ДНК.[3]
Механизм
Гликогенолиз может происходить двумя путями. В то время как первый путь вращается вокруг цитозольной деградации посредством синхронизированного действия гликогенфосфорилазы и фермента, разветвляющего гликоген, второй путь вращается вокруг лизосомальной деградации с помощью фермента альфа-глюкозидазы.
В соответствии с цитозольной деградацией, гликогенфосфорилаза, фермент, ограничивающий скорость гликогенолиза, расщепляет концевой остаток глюкозы, связанный с ответвлением гликогена, при этом замещая фосфорильную группу на связь альфа 1-4.Четыре остатка перед альфа-связью 1-6, соответствующие разветвлению, фермент разветвления гликогена катализирует перенос трех из четырех оставшихся остатков глюкозы в конец другой цепи гликогена, где они снова могут разлагаться гликогенфосфорилазой. Другими словами, разрыв альфа-1-4 гликозидных связей, присутствующих в линейных цепях, катализируется гликогенфосфорилазой, а добавление фосфатной группы в позицию один приводит к образованию глюкозо-1-фосфата. Активность гликогенфосфорилазы модулируется аллостерически и фосфорилированием.Производство гликогена, наоборот, подавляет деградацию гликогена. Затем фосфоглюкомутаза отвечает за преобразование глюкозо-1-фосфата в глюкозо-6-фосфат посредством реакции изомеризации, которая не требует энергии.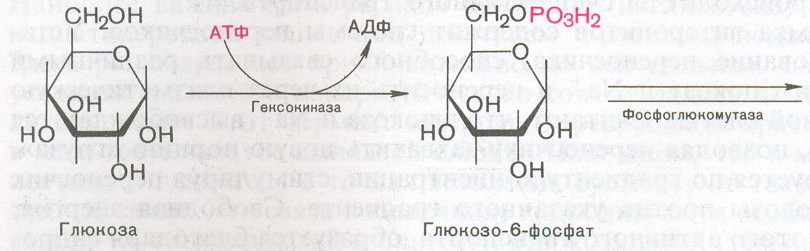 С другой стороны, фермент разветвления имеет дело с альфа-связями 1-6 и переносит ответвление на конец полимера, чтобы гликогенфосфорилаза могла продолжать работать с ним. В большинстве тканей глюкозо-6-фосфат используется внутри организма для гликолиза и выработки энергии путем преобразования в пируват, действуя как критически важный промежуточный продукт метаболизма для других путей, включая цикл TCA, синтез жирных кислот, цикл Кори и цикл аланина.Тем не менее, в глюконеогенных органах, таких как печень, почки и кишечник, глюкозо-6-фосфат необходимо дефосфорилировать до глюкозы с помощью фермента глюкозо-6-фосфатазы, чтобы он мог переноситься из ER в интерстициальную космос. Соответствует деградации лизосомального гликогена, основного фермента, участвующего в кислой мальтазе. Предполагается, что гидролиз гликогена до глюкозы, катализируемый кислой альфа-глюкозидазой, служит защитным механизмом для печени от высоких концентраций гликогена.Из общего количества гликогенолиза, происходящего в скелетных мышцах, только 5% деградации гликогена происходит в лизосомах.
С другой стороны, фермент разветвления имеет дело с альфа-связями 1-6 и переносит ответвление на конец полимера, чтобы гликогенфосфорилаза могла продолжать работать с ним. В большинстве тканей глюкозо-6-фосфат используется внутри организма для гликолиза и выработки энергии путем преобразования в пируват, действуя как критически важный промежуточный продукт метаболизма для других путей, включая цикл TCA, синтез жирных кислот, цикл Кори и цикл аланина.Тем не менее, в глюконеогенных органах, таких как печень, почки и кишечник, глюкозо-6-фосфат необходимо дефосфорилировать до глюкозы с помощью фермента глюкозо-6-фосфатазы, чтобы он мог переноситься из ER в интерстициальную космос. Соответствует деградации лизосомального гликогена, основного фермента, участвующего в кислой мальтазе. Предполагается, что гидролиз гликогена до глюкозы, катализируемый кислой альфа-глюкозидазой, служит защитным механизмом для печени от высоких концентраций гликогена.Из общего количества гликогенолиза, происходящего в скелетных мышцах, только 5% деградации гликогена происходит в лизосомах. Что касается гликогенолиза печени, только 10% происходит в лизосомах. [6] [5] [7]
Что касается гликогенолиза печени, только 10% происходит в лизосомах. [6] [5] [7]
Тестирование
Визуализация молекул гликогена не может быть сделана с помощью световой микроскопии, вместо этого требуется электронная микроскопия. Гистологическое окрашивание и использование световой микроскопии позволит визуализировать только конгломераты частиц гликогена. Молекулы гликогена сами по себе требуют электронной микроскопии.В зависимости от собранного образца ткани гликоген описывается как бета-частицы, похожие на розетки, или более крупные альфа-частицы. Бета-частицы, похожие на розетки, находятся на мышцах, тогда как альфа-частицы, которые представляют собой просто агрегаты бета-частиц, находятся в печени. Бета-частицы соответствуют типичной конфигурации гликогена со средней длиной цепи из 13 остатков, состоящей из внутренних цепей с точками ветвления и внешних цепей без точек ветвления. Встроенный метод гистологического окрашивания — Period Acid Schiff.Однако существуют определенные недостатки этого метода, в том числе отсутствие специфичности и общая несовместимость с методами иммунофлуоресценции.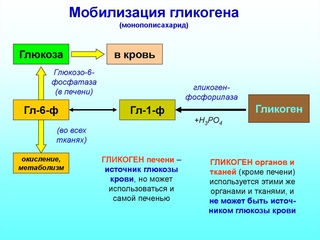 Таким образом, теперь доступен новый метод обнаружения гликогена в клетках, в котором возобновляемый рекомбинантный белок, содержащий углеводсвязывающий модуль из белка 1 крахмал-связывающего домена (Stbd1), впоследствии используется для проведения иммуноферментного анализа [1]. ] [8]
Таким образом, теперь доступен новый метод обнаружения гликогена в клетках, в котором возобновляемый рекомбинантный белок, содержащий углеводсвязывающий модуль из белка 1 крахмал-связывающего домена (Stbd1), впоследствии используется для проведения иммуноферментного анализа [1]. ] [8]
Что касается тестирования на болезни накопления гликогена, современные методы, использующие анализ мутаций ДНК, устранили необходимость выполнять биопсию печени.Этот диагностический тест, например, применяется к болезни фон Гирке и болезни Кори. Диагностические тесты на болезнь Помпе включают анализ активности кислой мальтазы в лейкоцитах или фибробластах. Биопсия мышцы, показывающая вакуолизированную миопатию с чрезмерным накоплением лизосомального гликогена, также может служить диагностическим тестом для болезни Помпе. [5]
Скорость гликогенолиза — это разница между скоростью производства глюкозы и абсолютным глюконеогенезом. Уровни глюконеогенеза определяются с использованием методов, включая радиоактивные и стабильные изотопы. Количественная оценка гликогенолиза также возможна с помощью спектроскопии ядерного магнитного резонанса. [9]
Количественная оценка гликогенолиза также возможна с помощью спектроскопии ядерного магнитного резонанса. [9]
Патофизиология
Нарушения гликогенолиза могут приводить к множеству заболеваний, включая болезни накопления гликогена (GSD), лизосомные болезни накопления и прогрессирующую миоклоническую эпилепсию Lafora. Нарушения гликогенолиза часто приводят к дисфункции органов, включая печень, скелетные мышцы, мозг и почки. В зависимости от пораженного фермента гликогенолиза возможен определенный спектр синдромов.
Нарушение гликогенолиза может привести к заболеваниям накопления гликогена, таким как болезнь фон Гирке, наиболее распространенная GSD. GSD типа I действует из-за дефицита глюкозо-6-фосфатазы, ответственной за дефосфорилирование глюкозо-6-фосфата, так что глюкоза может транспортироваться за пределы клетки для регулирования уровня глюкозы в крови и использования топлива в других тканях за пределами печени. Нарушение способности вырабатывать глюкозу в результате гликогенолиза приводит к тяжелой гипогликемии, гиперурикемии и повышению уровня молочной кислоты и триглицеридов. Из-за отложения жира у пациентов появляется округлое лицо, похожее на куклу. Без лечения у пациентов с этим заболеванием наблюдались нарушение роста, гепатомегалия, аномальные отеки и задержка моторного развития. Из-за накопления гликогена в почках могут развиться долгосрочные осложнения, приводящие к нефропатии, хроническому заболеванию почек и раку почек. Основная форма лечения пациентов с болезнью фон Гирке — поддерживать нормальный уровень глюкозы, избегая гипогликемии за счет частого кормления.[5] [10]
Из-за отложения жира у пациентов появляется округлое лицо, похожее на куклу. Без лечения у пациентов с этим заболеванием наблюдались нарушение роста, гепатомегалия, аномальные отеки и задержка моторного развития. Из-за накопления гликогена в почках могут развиться долгосрочные осложнения, приводящие к нефропатии, хроническому заболеванию почек и раку почек. Основная форма лечения пациентов с болезнью фон Гирке — поддерживать нормальный уровень глюкозы, избегая гипогликемии за счет частого кормления.[5] [10]
В то время как расщепление гликогена фосфорилазой и расщепляющим ферментом может происходить в цитозоле, гликоген также разрушается через лизосомный путь, что приводит к лизосомной болезни накопления, называемой болезнью Помпе (болезнь накопления гликогена типа II). При болезни Помпе развилась мутация лизосомальной альфа-глюкозидазы, также называемой кислой мальтазой. В результате гликоген накапливается в лизосоме и ее пузырьках, что приводит к летальному исходу, включая кардиомиопатию и мышечную гипотонию. Точный путь, по которому гликоген транспортируется в лизосомы, все еще неизвестен, но предполагается, что это происходит через макроаутофагию, при которой поглощение груза внутри двухмембранных везикул, называемых аутофагосомами, сливается с лизосомами. [1]
Точный путь, по которому гликоген транспортируется в лизосомы, все еще неизвестен, но предполагается, что это происходит через макроаутофагию, при которой поглощение груза внутри двухмембранных везикул, называемых аутофагосомами, сливается с лизосомами. [1]
Болезнь накопления гликогена Тип III, также называемая болезнью Кори, возникает из-за дефицита фермента, разветвляющего гликоген. В результате это заболевание проявляется накоплением аномального гликогена, поскольку гликогенолиз останавливается, когда гликогенфосфорилаза встречает точку ветвления.В этом случае гликоген считается ненормальным, поскольку он отражает очень короткие внешние цепи. Пациенты с болезнью Кори имеют кетотическую гипогликемию и гепатомегалию. В редких случаях это может привести к циррозу печени и гепатоцеллюлярной карциноме. [5]
Болезнь накопления гликогена Тип V (болезнь Макардла) развивается из-за дефицита гликогенфосфорилазы в скелетных мышцах. Другими словами, при этом заболевании печень щадит. Пациенты демонстрируют непереносимость физических упражнений, мышечную слабость, спазмы и боли.Уровень креатинкиназы повышается, и может присутствовать миоглобинурия. Типичным для этого заболевания является явление, называемое «второе дыхание», когда пациенты могут возобновить упражнения после кратковременного отдыха. Прием сахарозы перед тренировкой может помочь облегчить симптомы, поскольку она становится источником энергии во время тренировки, прежде чем прибегать к запасам гликогена. При дефиците гликогенфосфорилазы в печени развивается другое заболевание — GSD типа VI. У нее нормальный уровень креатинкиназы и мочевой кислоты.У пациентов наблюдается задержка роста и увеличение печени. Гиперлипидемия и кетотическая гипогликемия могут быть обычным явлением. [5]
Пациенты демонстрируют непереносимость физических упражнений, мышечную слабость, спазмы и боли.Уровень креатинкиназы повышается, и может присутствовать миоглобинурия. Типичным для этого заболевания является явление, называемое «второе дыхание», когда пациенты могут возобновить упражнения после кратковременного отдыха. Прием сахарозы перед тренировкой может помочь облегчить симптомы, поскольку она становится источником энергии во время тренировки, прежде чем прибегать к запасам гликогена. При дефиците гликогенфосфорилазы в печени развивается другое заболевание — GSD типа VI. У нее нормальный уровень креатинкиназы и мочевой кислоты.У пациентов наблюдается задержка роста и увеличение печени. Гиперлипидемия и кетотическая гипогликемия могут быть обычным явлением. [5]
При прогрессирующей миоклонической эпилепсии Lafora повышенное фосфорилирование гликогена присутствует в нескольких тканях, что приводит к токсичности и гибели клеток в нейронах. Симптомы включают атаксию, судороги, миоклонус и слабоумие. Присутствие более высоких уровней фосфорилирования в гликогене приводит к образованию более длинных цепей и нерегулярных точек разветвления, которые делают полимер нерастворимым и устойчивым к деградации.В результате у пациентов с этим заболеванием образуется конгломерат телец включения, называемых тельцами Лафоры. [5]
Клиническая значимость
Важность гликогенолиза демонстрируется через мутации в деградации гликогена, приводящие к генетическим нарушениям у человека, и через неспособность скелетных мышц справляться с физическим стрессом при дефиците гликогена.
Повышение квалификации / обзорные вопросы
Рисунок
Гликогенез. Изображение предоставлено: https: // commons.wikimedia.org/wiki/File:Glycogenesis.png
Биохимия, гликогенез — StatPearls — Книжная полка NCBI
Введение
Гликоген, основная форма хранения глюкозы и основной источник неокислительной глюкозы для скелетных мышц и печени, дает значительные преимущества. способствует его деградации, поддерживая нормальный уровень глюкозы в крови и обеспечивая топливо для сокращения мышц. Что касается цитозольной деградации, основные ферменты, участвующие в распаде гликогена, представляют собой гликогенфосфорилазу и фермент разветвления.Гликогенфосфорилаза заботится о разрыве связей в линейной цепи, тогда как фермент разветвления переносит остатки глюкозы в линейную цепь для разрушения разветвлений. Оба фермента работают в скелетных мышцах и печени. Поскольку скелетные мышцы могут использовать фосфорилированную форму глюкозы в качестве топлива, для них не требуется глюкозо-6-фосфатаза.
С другой стороны, печени требуется глюкозо-6-фосфатаза для дефосфорилирования глюкозы и экспорта глюкозы за пределы клетки. Что касается лизосомальной деградации, кислая альфа-глюкозидаза отвечает за гликогенолиз.Дефицит любого из этих ферментов проявляется в виде уникальных болезненных состояний. Большинство изменений в цитозольной деградации вызывают болезни накопления гликогена, включая болезнь фон Гирке, болезнь Кори и болезнь Херса. Нарушение лизосомальной деградации может привести к болезни Помпе. Нарушение роли гликогенолиза в нервном функционировании проявляется в проявлении болезни Лафора. Обнаружение изменений гликогенолиза может быть сделано в основном с помощью анализа ДНК и электронной микроскопии с помощью биопсии печени и скелетных мышц.
Основы
Гликоген существует из предшественников глюкозы, полученных из недавно проглоченных углеводов или глюконеогенных предшественников, включая лактат и аланин. Гликогенолиз — это просто процесс, участвующий в расщеплении гликогена для использования в качестве источника энергии, главным образом в скелетных мышцах и печени. Распад гликогена происходит двумя разными путями в зависимости от местоположения. Что касается скелетных мышц, деградация гликогена приводит к образованию глюкозо-1-фосфата, и мышцы сами по себе используют его в качестве топлива для сокращения.Гликогенолиз в скелетных мышцах происходит в условиях физической активности. С другой стороны, гликогенолиз печени генерирует глюкозу для экспорта в кровоток. Стимулом для гликогенолиза печени является недостаток питания с соответствующим увеличением гормонов, таких как глюкагон. [1]
Проблемы, вызывающие озабоченность
Из-за жизненно важной роли, которую распад гликогена играет в нормальной физиологии, включая поддержание уровня глюкозы в крови и сокращение мышц во время активности, нарушения гликогенолиза вызывают патофизиологические состояния.Хотя исследователи исследовали роль гликогена, определенная информация не совсем понятна. Например, неясна конкретная роль гликогена в сокращении мышц или способ переноса гликогена в лизосомы.
Клеточный
Гликогенолиз, расщепление гликогена, происходит в двух клеточных участках: цитозоле и лизосоме. Различные ферменты осуществляют расщепление гликогена в этих клеточных участках. При разложении гликогена в качестве топлива используется глюкоза или глюкозо-1-фосфат.В скелетных мышцах захват глюкозы опосредуется транспортерами GLUT1 (лежащими на плазматической мембране) и GLUT4 (лежащими внутри внутриклеточных накопительных везикул). В цитозоле гликогенфосфорилаза сильно активируется АМФ для мышечной ткани. Что касается печени, глюкагон активирует гликогенфосфорилазу за счет увеличения циклического АМФ. Деградация гликогена в лизосомах опосредуется кислой альфа-глюкозидазой через аутофагические вакуоли, которые захватывают часть цитоплазмы и сливаются с органеллами, вмещая содержимое.Конкретные механизмы получают дальнейшее объяснение в следующих разделах. [2]
Молекулярный
Гликоген — это разветвленный полимер глюкозы. Глюкоза хранится в клетках в виде полимеров, что увеличивает растворимость, занимает меньше места и обеспечивает быструю мобилизацию. Запас гликогена в гепатоците соответствует расчетной концентрации глюкозы 400 мМ. И наоборот, вклад нерастворимого гликогена в осмолярность цитозоля в 40 миллионов раз меньше, чем вклад 40 мМ глюкозы.Следовательно, если бы полимерная форма гликогена не существовала, осмолярность цитозоля была бы достаточно высокой, чтобы вызвать проникновение воды в клетку посредством осмоса и привести к лизису клетки. Гликоген приводит к более высокой растворимости, в основном из-за образования разветвлений. С другой стороны, большая часть полимера образует альфа-1-4 гликозидные связи, которые организуются в цепочки, разветвление происходит через каждые 4-8 мономеров глюкозы через альфа-1-6 гликозидные связи. Такое расположение приводит к классической организации гликогена, называемого бета-частицами, с самогликозилирующим белком, называемым гликогенином, в ядре.[3]
Важно понимать конформацию гликогена, поскольку гликогенолиз включает распад этого полимера на мономеры глюкозы с помощью отдельных ферментов, которые катализируют разрушение разветвлений и цепей гликогена.
Функция
Распад гликогена происходит во время голодания или при низком соотношении инсулина и глюкагона. Основные запасы энергии для организма — это гликоген и липиды. В то время как липиды приводят к большему количеству молекул АТФ после окисления, гликогенолиз приводит к меньшему количеству молекул АТФ.Однако существуют два существенных преимущества метаболизма гликогена. Первое преимущество соответствует быстрой мобилизации гликогена для удовлетворения метаболических потребностей. Возможна быстрая мобилизация, поскольку ферменты гликогенолиза могут прикрепляться к многочисленным ветвям гликогена и начинать одновременный гидролиз. Второе преимущество заключается в выработке энергии в условиях отложений с низким содержанием липидов, например, при анорексии. [3]
Количественно гликоген больше присутствует в скелетных мышцах, чем в печени.Тем не менее гликогенолиз играет важную роль в обеих тканях. В печени метаболизм гликогена играет жизненно важную роль во время голодания, приводя к выработке печеночной глюкозы для поддержания здорового уровня глюкозы в крови и поддержки потребностей в топливе других тканей. С другой стороны, полное проявление гликогена в скелетных мышцах указывает на критическую функцию, которую гликоген играет в скелетных мышцах с точки зрения быстрого образования АТФ. Существует тесная взаимосвязь между хранением гликогена в скелетных мышцах и сопротивлением усталости.Способность мышцы тренироваться в течение первых 30 минут активности, несмотря на обилие других источников энергии, таких как липиды, серьезно ухудшается, когда уровень гликогена в скелетных мышцах снижается. Истощение гликогена приводит к утомлению, потому что мышца не может обеспечить скелетным мышцам достаточное количество энергии для возбуждения и сокращения. Вероятная причина вращается вокруг роли гликогена в высвобождении кальция из саркоплазматической сети. [4] [5]
Помимо обеспечения энергией, гликогенолиз может привести к образованию прекурсоров для участия в окислительных реакциях пентозофосфатного пути, помогая генерировать НАДФН, который необходим для синтеза жирных кислот и производства пентозофосфатов, которые необходимы для синтез РНК и ДНК.[3]
Механизм
Гликогенолиз может происходить двумя путями. В то время как первый путь вращается вокруг цитозольной деградации посредством синхронизированного действия гликогенфосфорилазы и фермента, разветвляющего гликоген, второй путь вращается вокруг лизосомальной деградации с помощью фермента альфа-глюкозидазы.
В соответствии с цитозольной деградацией, гликогенфосфорилаза, фермент, ограничивающий скорость гликогенолиза, расщепляет концевой остаток глюкозы, связанный с ответвлением гликогена, при этом замещая фосфорильную группу на связь альфа 1-4.Четыре остатка перед альфа-связью 1-6, соответствующие разветвлению, фермент разветвления гликогена катализирует перенос трех из четырех оставшихся остатков глюкозы в конец другой цепи гликогена, где они снова могут разлагаться гликогенфосфорилазой. Другими словами, разрыв альфа-1-4 гликозидных связей, присутствующих в линейных цепях, катализируется гликогенфосфорилазой, а добавление фосфатной группы в позицию один приводит к образованию глюкозо-1-фосфата. Активность гликогенфосфорилазы модулируется аллостерически и фосфорилированием.Производство гликогена, наоборот, подавляет деградацию гликогена. Затем фосфоглюкомутаза отвечает за преобразование глюкозо-1-фосфата в глюкозо-6-фосфат посредством реакции изомеризации, которая не требует энергии. С другой стороны, фермент разветвления имеет дело с альфа-связями 1-6 и переносит ответвление на конец полимера, чтобы гликогенфосфорилаза могла продолжать работать с ним. В большинстве тканей глюкозо-6-фосфат используется внутри организма для гликолиза и выработки энергии путем преобразования в пируват, действуя как критически важный промежуточный продукт метаболизма для других путей, включая цикл TCA, синтез жирных кислот, цикл Кори и цикл аланина.Тем не менее, в глюконеогенных органах, таких как печень, почки и кишечник, глюкозо-6-фосфат необходимо дефосфорилировать до глюкозы с помощью фермента глюкозо-6-фосфатазы, чтобы он мог переноситься из ER в интерстициальную космос. Соответствует деградации лизосомального гликогена, основного фермента, участвующего в кислой мальтазе. Предполагается, что гидролиз гликогена до глюкозы, катализируемый кислой альфа-глюкозидазой, служит защитным механизмом для печени от высоких концентраций гликогена.Из общего количества гликогенолиза, происходящего в скелетных мышцах, только 5% деградации гликогена происходит в лизосомах. Что касается гликогенолиза печени, только 10% происходит в лизосомах. [6] [5] [7]
Тестирование
Визуализация молекул гликогена не может быть сделана с помощью световой микроскопии, вместо этого требуется электронная микроскопия. Гистологическое окрашивание и использование световой микроскопии позволит визуализировать только конгломераты частиц гликогена. Молекулы гликогена сами по себе требуют электронной микроскопии.В зависимости от собранного образца ткани гликоген описывается как бета-частицы, похожие на розетки, или более крупные альфа-частицы. Бета-частицы, похожие на розетки, находятся на мышцах, тогда как альфа-частицы, которые представляют собой просто агрегаты бета-частиц, находятся в печени. Бета-частицы соответствуют типичной конфигурации гликогена со средней длиной цепи из 13 остатков, состоящей из внутренних цепей с точками ветвления и внешних цепей без точек ветвления. Встроенный метод гистологического окрашивания — Period Acid Schiff.Однако существуют определенные недостатки этого метода, в том числе отсутствие специфичности и общая несовместимость с методами иммунофлуоресценции. Таким образом, теперь доступен новый метод обнаружения гликогена в клетках, в котором возобновляемый рекомбинантный белок, содержащий углеводсвязывающий модуль из белка 1 крахмал-связывающего домена (Stbd1), впоследствии используется для проведения иммуноферментного анализа [1]. ] [8]
Что касается тестирования на болезни накопления гликогена, современные методы, использующие анализ мутаций ДНК, устранили необходимость выполнять биопсию печени.Этот диагностический тест, например, применяется к болезни фон Гирке и болезни Кори. Диагностические тесты на болезнь Помпе включают анализ активности кислой мальтазы в лейкоцитах или фибробластах. Биопсия мышцы, показывающая вакуолизированную миопатию с чрезмерным накоплением лизосомального гликогена, также может служить диагностическим тестом для болезни Помпе. [5]
Скорость гликогенолиза — это разница между скоростью производства глюкозы и абсолютным глюконеогенезом. Уровни глюконеогенеза определяются с использованием методов, включая радиоактивные и стабильные изотопы.Количественная оценка гликогенолиза также возможна с помощью спектроскопии ядерного магнитного резонанса. [9]
Патофизиология
Нарушения гликогенолиза могут приводить к множеству заболеваний, включая болезни накопления гликогена (GSD), лизосомные болезни накопления и прогрессирующую миоклоническую эпилепсию Lafora. Нарушения гликогенолиза часто приводят к дисфункции органов, включая печень, скелетные мышцы, мозг и почки. В зависимости от пораженного фермента гликогенолиза возможен определенный спектр синдромов.
Нарушение гликогенолиза может привести к заболеваниям накопления гликогена, таким как болезнь фон Гирке, наиболее распространенная GSD. GSD типа I действует из-за дефицита глюкозо-6-фосфатазы, ответственной за дефосфорилирование глюкозо-6-фосфата, так что глюкоза может транспортироваться за пределы клетки для регулирования уровня глюкозы в крови и использования топлива в других тканях за пределами печени. Нарушение способности вырабатывать глюкозу в результате гликогенолиза приводит к тяжелой гипогликемии, гиперурикемии и повышению уровня молочной кислоты и триглицеридов.Из-за отложения жира у пациентов появляется округлое лицо, похожее на куклу. Без лечения у пациентов с этим заболеванием наблюдались нарушение роста, гепатомегалия, аномальные отеки и задержка моторного развития. Из-за накопления гликогена в почках могут развиться долгосрочные осложнения, приводящие к нефропатии, хроническому заболеванию почек и раку почек. Основная форма лечения пациентов с болезнью фон Гирке — поддерживать нормальный уровень глюкозы, избегая гипогликемии за счет частого кормления.[5] [10]
В то время как расщепление гликогена фосфорилазой и расщепляющим ферментом может происходить в цитозоле, гликоген также разрушается через лизосомный путь, что приводит к лизосомной болезни накопления, называемой болезнью Помпе (болезнь накопления гликогена типа II). При болезни Помпе развилась мутация лизосомальной альфа-глюкозидазы, также называемой кислой мальтазой. В результате гликоген накапливается в лизосоме и ее пузырьках, что приводит к летальному исходу, включая кардиомиопатию и мышечную гипотонию.Точный путь, по которому гликоген транспортируется в лизосомы, все еще неизвестен, но предполагается, что это происходит через макроаутофагию, при которой поглощение груза внутри двухмембранных везикул, называемых аутофагосомами, сливается с лизосомами. [1]
Болезнь накопления гликогена Тип III, также называемая болезнью Кори, возникает из-за дефицита фермента, разветвляющего гликоген. В результате это заболевание проявляется накоплением аномального гликогена, поскольку гликогенолиз останавливается, когда гликогенфосфорилаза встречает точку ветвления.В этом случае гликоген считается ненормальным, поскольку он отражает очень короткие внешние цепи. Пациенты с болезнью Кори имеют кетотическую гипогликемию и гепатомегалию. В редких случаях это может привести к циррозу печени и гепатоцеллюлярной карциноме. [5]
Болезнь накопления гликогена Тип V (болезнь Макардла) развивается из-за дефицита гликогенфосфорилазы в скелетных мышцах. Другими словами, при этом заболевании печень щадит. Пациенты демонстрируют непереносимость физических упражнений, мышечную слабость, спазмы и боли.Уровень креатинкиназы повышается, и может присутствовать миоглобинурия. Типичным для этого заболевания является явление, называемое «второе дыхание», когда пациенты могут возобновить упражнения после кратковременного отдыха. Прием сахарозы перед тренировкой может помочь облегчить симптомы, поскольку она становится источником энергии во время тренировки, прежде чем прибегать к запасам гликогена. При дефиците гликогенфосфорилазы в печени развивается другое заболевание — GSD типа VI. У нее нормальный уровень креатинкиназы и мочевой кислоты.У пациентов наблюдается задержка роста и увеличение печени. Гиперлипидемия и кетотическая гипогликемия могут быть обычным явлением. [5]
При прогрессирующей миоклонической эпилепсии Lafora повышенное фосфорилирование гликогена присутствует в нескольких тканях, что приводит к токсичности и гибели клеток в нейронах. Симптомы включают атаксию, судороги, миоклонус и слабоумие. Присутствие более высоких уровней фосфорилирования в гликогене приводит к образованию более длинных цепей и нерегулярных точек разветвления, которые делают полимер нерастворимым и устойчивым к деградации.В результате у пациентов с этим заболеванием образуется конгломерат телец включения, называемых тельцами Лафоры. [5]
Клиническая значимость
Важность гликогенолиза демонстрируется через мутации в деградации гликогена, приводящие к генетическим нарушениям у человека, и через неспособность скелетных мышц справляться с физическим стрессом при дефиците гликогена.
Повышение квалификации / обзорные вопросы
Рисунок
Гликогенез. Изображение предоставлено: https: // commons.wikimedia.org/wiki/File:Glycogenesis.png
Гликогенез
Биосинтез глюкозы:
Глюконеогенез:
Глюконеогенез — это процесс синтеза глюкозы. из неуглеводных источников. Отправная точка глюконеогенеза пировиноградная кислота, хотя щавелевоуксусная кислота и дигидроксиацетон фосфаты также обеспечивают точки входа. Молочная кислота, немного амино кислоты из белка и глицерин из жира могут быть преобразованы в глюкоза.Глюконеогенез похож, но не наоборот гликолиза, некоторые этапы идентичны в обратном порядке. направление и три из них новые. Не вдаваясь в В деталях общая последовательность глюконеогенеза приведена в рисунок слева.
Обратите внимание, что щавелевоуксусная кислота синтезируется из пировиноградной кислоты. на первом этапе. Щавелевоуксусная кислота также является первым соединением реагировать с ацетил-КоА в цикле лимонной кислоты.Концентрация ацетил-КоА и АТФ определяет судьбу щавелевоуксусной кислоты. Если концентрация ацетил-КоА низкая и концентрация АТФ высок, тогда продолжается глюконеогенез. Также обратите внимание, что ATP требуется для последовательности биосинтеза глюконеогенеза.
Глюконеогенез происходит в основном в печени с небольшим количеством также происходит в коре почек. Очень слабый глюконеогенез возникает в головном мозге, скелетных мышцах, сердечных мышцах или других ткани тела.Фактически, эти органы очень нуждаются в глюкозе. Следовательно, в печени постоянно происходит глюконеогенез. для поддержания уровня глюкозы в крови для удовлетворения этих требований.
Ссылка на: Интерактивный
Глюконеогенез (наведите курсор на стрелки)
Джим Харди, профессор химии, Университет Акрона.
Ссылка на Родни Бойера — Глюконеогенез —
| Тест: сколько требуется молекул пировиноградной кислоты сделать глюкозу? | Ответ Пировиноградная кислота имеет 3 атома углерода, глюкоза имеет 6 атомов углерода, поэтому 2 пировиноградных молекулы кислоты нужный. |
6.22 Гликогенез и гликогенолиз | Питание Flexbook
Как обсуждалось ранее, гликоген — это форма хранения глюкозы у животных. Если человек находится в анаболическом состоянии, например, после еды, большая часть глюкозо-6-фосфата в миоцитах (мышечных клетках) или гепатоцитах (клетках печени) будет храниться в виде гликогена. Структура показана ниже в качестве напоминания.
Рисунок 6.221 Структура гликогена 1
Гликоген в основном хранится в печени и мышцах.Он составляет ~ 6% от сырого веса печени и только 1% от сырого веса мышц. Однако, поскольку в нашем теле гораздо больше мышечной массы, в мышцах хранится в 3-4 раза больше гликогена, чем в печени2. У нас ограниченная емкость хранения гликогена. Таким образом, после еды с высоким содержанием углеводов наши запасы гликогена исчерпываются. После того, как запасы гликогена будут заполнены, глюкоза должна будет метаболизироваться по-разному, чтобы она могла храниться в другой форме.
Гликогенез
Синтез гликогена из глюкозы — это процесс, известный как гликогенез.Глюкозо-6-фосфат не вставляется непосредственно в гликоген в этом процессе. Прежде чем он будет включен, нужно выполнить несколько шагов. Сначала глюкозо-6-фосфат превращается в глюкозо-1-фосфат, а затем превращается в уридиндифосфат (УДФ) -глюкозу. UDP-глюкоза вставляется в гликоген либо ферментом, гликогенсинтазой (альфа-1,4-связи), либо разветвляющим ферментом (альфа-1,6-связи) в точках ветвления 3 .
Рисунок 6.222 Гликогенез
Гликогенолиз
Процесс выделения глюкозы из гликогена известен как гликогенолиз.Этот процесс по существу противоположен гликогенезу за двумя исключениями: (1) отсутствует стадия UDP-глюкозы и (2) задействован другой фермент, гликогенфосфорилаза. Глюкозо-1-фосфат отщепляется от гликогена ферментом гликогенфосфорилазой, который затем может быть преобразован в глюкозо-6-фосфат, как показано ниже 3 .
Рисунок 6.223 Гликогенолиз
Ссылки и ссылки
1. http://en.wikipedia.org/wiki/File:Glycogen.png
2.Шилс М.Э., Шике М., Росс А.С., Кабальеро Б., Казинс Р.Дж., редакторы. (2006) Современное питание при здоровье и болезнях. Балтимор, Мэриленд: Липпинкотт Уильямс и Уилкинс.
3. Гроппер С.С., Смит Дж. Л., Грофф Дж. Л.. (2008) Продвинутое питание и метаболизм человека. Бельмонт, Калифорния: Издательство Wadsworth.
Метаболизм гликогена — AMBOSS
Последнее обновление: 9 июня 2021 г.
Резюме
Гликоген — это важный сложный полимер, состоящий из нескольких цепей молекул глюкозы.Он присутствует во всех типах клеток, за исключением эритроцитов. Большая часть гликогена в организме хранится в печени и скелетных мышцах. Полностью восполненные запасы гликогена могут обеспечивать уровень глюкозы в крови примерно на 12–48 часов во время голодания. Метаболизм гликогена в первую очередь регулируется инсулином, глюкагоном и адреналином. Инсулин увеличивает гликогенез и снижает гликогенолиз в печени и мышцах; глюкагон и адреналин снижают гликогенез в печени и усиливают гликогенолиз в печени и мышцах.
Обзор
- Функция: гликоген является наиболее важной средой для хранения углеводов в организме и содержится в цитозольных гранулах.
- Общее хранение гликогена: ∼ 400–450 г (обеспечивает глюкозу на 12–48 часов)
- Химическая структура
- Разветвленный полимер, состоящий из нескольких связанных цепей глюкозы
- Разветвления: α-1,6-гликозидные связи
- Связи: α-1,4-гликозидные связи
Периодическая кислота – окраска Шиффа — это иммуногистохимический метод, используемый для визуализации полисахаридов, таких как гликоген.
Гликогенез
2.) Начальное образование цепи
- Гликогенин
- Фермент, состоящий из гомодимерного белка, который находится в ядре каждой единицы гликогена и является отправной точкой синтеза гликогена.
- Катализирует образование коротких цепей гликогена путем полимеризации нескольких молекул UDP-глюкозы
3.) Удлинение цепи
Ферментом, определяющим скорость гликогенеза, является гликогенсинтаза.
4.) Разветвление цепей гликогена
- Фермент разветвления: фермент с активностью глюкозилтрансферазы, который вводит ответвления в цепь гликогена, чтобы обеспечить дальнейшее удлинение цепи во многих участках комплекса гликогена
- Катализирует образование α-1,6-гликозидных связей: гидролизует цепь из 6 единиц глюкозы от исходной цепи → присоединение молекул к атому C6 другой единицы глюкозы в исходной цепи
- Ветви вводят не менее чем на 4 единицы глюкозы друг от друга.
Последовательность синтеза гликогена, начиная с глюкозы: Glc → Glc-6-P → Glc-1-P → UDP-Glc → гликоген
Гликогенолиз
1.) Высвобождение глюкозы
- Расщепление α-1,4-гликозидных связей: гликогенфосфорилаза (кофактор витамина B6) отщепляет глюкозу-1-P; через фосфорную реакцию до тех пор, пока на ответвлении не останется 4 концевых остатка глюкозы (так называемый предельный декстрин).
- Разрыв α-1,6-гликозидных связей
- Ферменты разветвления: фермент, обладающий глюкозилтрансферазной, а также глюкозидазной активностью
- Первый шаг: гликозилтрансфераза; (или 4-α-D-глюканотрансфераза): переносит 3 из 4 оставшихся остатков глюкозы ветви в соседнюю ветвь
- Второй этап: глюкозидаза (или амило-α-1,6-глюкозидаза): отщепляет оставшееся звено глюкозы (связь альфа-1,6) от ветви; через гидролитическую реакцию → высвобождение нефосфорилированных свободных молекул глюкозы и линейной цепи гликогена
- Ферменты разветвления: фермент, обладающий глюкозилтрансферазной, а также глюкозидазной активностью
Часть гликогена не разлагается гликогенфосфорилазой и ферментами, разветвляющими ветвления, а в лизосомах — лизосомальной альфа-глюкозидазой.Дефицит этого фермента приводит к болезни Помпе (болезнь накопления гликогена II).
Болезнь Кори — это тип нарушения накопления гликогена (тип III), вызванный дефицитом фермента, расщепляющего ответвления гликогена (α-1,6-глюкозидазы).
Болезнь МакАрдла — болезнь накопления гликогена, характеризующаяся дефицитом гликогенфосфорилазы в скелетных мышцах.
2) Утилизация глюкозы
После гликогенолиза фосфоглюкомутаза (изомераза) превращает глюкозу-1-P в глюкозу-6-P
- В мышцах
- Мгновенный метаболизм глюкозы-6-P во время упражнений (гликолиз)
- Гексокиназа: превращает свободную глюкозу в глюкозу-6-P
- В печени: глюкозо-6-фосфатаза: глюкоза-6-P → свободная глюкоза → высвобождение в системный кровоток → повышение уровня глюкозы в сыворотке.
Ферментом, определяющим скорость гликогенолиза, является гликогенфосфорилаза.
Болезни накопления гликогена вызваны унаследованной недостаточностью ферментов гликогенолиза, что приводит к накоплению нормального или патологически структурированного гликогена в клетках скелетных мышц и печени, основных запасах гликогена в организме.
Регламент
Повышенное содержание фосфата в клетках является сигналом голодания: все ферменты, повышающие уровень сахара в крови, активны в своей фосфорилированной форме!
Гормональная регуляция
Инсулин стимулирует накопление липидов, белков и гликогена.
Гликогенсинтаза стимулируется глюкозо-6-фосфатом, инсулином и кортизолом. Он ингибируется адреналином и глюкагоном.
Аллостерическая / негормональная регуляция
- Сокращение мышц увеличивает уровень внутриклеточного кальция → ↑ кальмодулин
Эти регуляторные процессы происходят только в скелетных мышцах, но не в печени.
Клиническое значение
Источники
6.3.3: 6.22 Гликогенез и гликогенолиз
- Последнее обновление
- Сохранить как PDF
- Гликогенез
- Гликогенолиз
- Ссылки и ссылки
Как обсуждалось ранее, гликоген является формой хранения глюкозы у животных.Если человек находится в анаболическом состоянии, например, после еды, большая часть глюкозо-6-фосфата в миоцитах (мышечных клетках) или гепатоцитах (клетках печени) будет храниться в виде гликогена. Структура показана ниже в качестве напоминания.
Рисунок 6.221 Структура гликогена 1
Гликоген в основном хранится в печени и мышцах. Он составляет ~ 6% от сырого веса печени и только 1% от сырого веса мышц. Однако, поскольку в нашем теле гораздо больше мышечной массы, в мышцах хранится в 3-4 раза больше гликогена, чем в печени 2 .У нас ограниченная емкость хранения гликогена. Таким образом, после еды с высоким содержанием углеводов наши запасы гликогена исчерпываются. После того, как запасы гликогена будут заполнены, глюкоза должна будет метаболизироваться по-разному, чтобы она могла храниться в другой форме.
Гликогенез
Синтез гликогена из глюкозы — это процесс, известный как гликогенез . Глюкозо-6-фосфат не вставляется непосредственно в гликоген в этом процессе. Прежде чем он будет включен, нужно выполнить несколько шагов.Сначала глюкозо-6-фосфат превращается в глюкозо-1-фосфат, а затем превращается в уридиндифосфат (УДФ) -глюкозу. UDP-глюкоза вставляется в гликоген либо ферментом, гликогенсинтазой (альфа-1,4-связи), либо разветвляющим ферментом (альфа-1,6-связи) в точках ветвления 3 .
Рисунок 6.222 Гликогенез
Гликогенолиз
Процесс выделения глюкозы из гликогена известен как гликогенолиз .Этот процесс по существу противоположен гликогенезу за двумя исключениями: (1) отсутствует стадия UDP-глюкозы и (2) задействован другой фермент, гликогенфосфорилаза. Глюкозо-1-фосфат отщепляется от гликогена ферментом гликогенфосфорилазой, который затем может быть преобразован в глюкозо-6-фосфат, как показано ниже 3 .
Рисунок 6.223 Гликогенолиз
Справочные материалы и ссылки
- ru.Wikipedia.org/wiki/File:Glycogen.png
- Шилс М.Э., Шике М., Росс А.С., Кабальеро Б., Казинс Р.Дж., редакторы. (2006) Современное питание при здоровье и болезнях. Балтимор, Мэриленд: Липпинкотт Уильямс и Уилкинс.
- Гроппер СС, Смит Дж. Л., Грофф Дж. Л. (2008) Продвинутое питание и метаболизм человека. Бельмонт, Калифорния: Wadsworth Publishing
